جواب باهم بیندیشید صفحه 12 درس 1 شیمی یازدهم (قدر هدایای زمینی را بدانیم)
تعداد بازدید : 80.87Mپاسخ باهم بیندیشید صفحه 12 شیمی یازدهم
-گام به گام باهم بیندیشید صفحه 12 درس قدر هدایای زمینی را بدانیم
-باهم بیندیشید صفحه 12 درس 1
-شما در حال مشاهده جواب باهم بیندیشید صفحه 12 شیمی یازدهم هستید. ما در تیم مای درس، پاسخنامههای کاملاً تشریحی و استاندارد را مطابق با آخرین تغییرات کتاب درسی 1404 برای شما گردآوری کردهایم. اگر به دنبال بهروزترین پاسخها برای این صفحه هستید و میخواهید بدون نیاز به اتصال به اینترنت، علاوه بر پاسخهای گام به گام، به گنجینهای از مطالب درسی دسترسی پیدا کنید، حتماً اپلیکیشن مایدرس را نصب نمایید.
📥 دانلود اپلیکیشن مایدرس
برای دسترسی آفلاین، سریع و بدون نیاز به اینترنت به گنجینهای از گامبهگامها و نمونه سوالات، اپلیکیشن را نصب کنید.
1) با توجه به جایگاه عنصرهای لیتیم، سدیم و پتاسیم (فلزهای قلیایی 1) در جدول دوره ای، پیش بینی كنید در واكنش با گاز كلر، اتم های كدام یک آسان تر الكترون از دست خواهد داد؟ چرا؟
2) تصویر زیر واكنش این فلزها با گاز كلر را در شرایط یكسان نشان می دهد. آیا داده های این تصویر پیش بینی شما را تأیید می كند؟ (راهنمایی: هرچه ماده ای سریع تر و شدیدتر واكنش بدهد، فعالیت شیمیایی بیشتری دارد.)

3) به نظر شما آیا جملۀ «هرچه شعاع اتمی یك فلز بزرگتر باشد، آسان تر الكترون از دست می دهد» درست است؟ چرا؟
4) جدول زیر را كامل كنید و توضیح دهید بین شمار لایه های الكترونی با شعاع اتم چه رابطه ای وجود دارد.
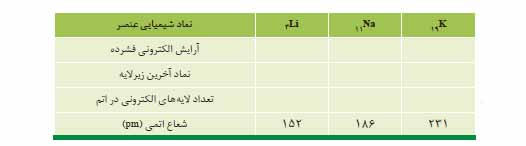
5) با توجه به جدول زیر، پیش بینی كنید اتم كدام یک از فلزهای گروه دوم (فلزهای قلیایی خاکی2) جدول دوره ای در واكنش با نافلزها، آسان تر به كاتیون M2+ تبدیل می شود. چرا؟

1) پتاسیم ، زیرا در گروه پایین تر است و خصلت فلزی یعنی تمایل به از دست دادن الکترون بیشتری دارد و در نتیجه آسان تر الکترون می دهد.
2) بله، در تصویر، (شدت واکنش) بر اساس شدت نور برای پتاسیم بیشتر است.
3) بله شعاع اتمی پتاسیم بزرگ تر از سدیم و لیتیم است و طبق تصویر بالا واکنش پذیری آن نیز بیشتر است. بنابراین با بزرگتر شدن اندازه اتم ، خاصیت فلزی بیشتر و تمایل به از دست دادن الکترون بیشتر می شود. با بزرگتر شدن اتم جاذبه هسته بر روی الکترون کم تر می شود.
4) رابطه مستقیم وجود دارد و با افزایش تعداد لایه های الکترونی شعاع اتمی و اندازه اتم بزرگتر می شود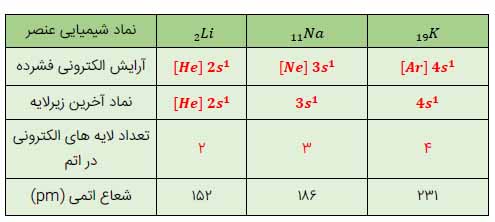 5) استرانسیم - چون شعاع اتمی بزرگتری دارد پس تمایل به از دست دادن الکترون بیشتر است..
5) استرانسیم - چون شعاع اتمی بزرگتری دارد پس تمایل به از دست دادن الکترون بیشتر است..
مای درس ، برترین اپلیکیشن کمک درسی ایران
پوشش تمام محتواهای درسی پایه چهارم تا دوازدهم- آزمون آنلاین تمامی دروس
- گام به گام تمامی دروس
- ویدئو های آموزشی تمامی دروس
- گنجینه ای از جزوات و نمونه سوالات تمامی دروس
- فلش کارت های آماده دروس
- گنجینه ای جامع از انشاء های آماده
- آموزش جامع آرایه های ادبی، دستور زبان، قواعد زبان انگلیسی و ... ویژه



1736019749.png)















