جواب تمرین های دوره ای صفحه 83 درس 2 شیمی دهم (ردِّ پای گازها در زندگی)
تعداد بازدید : 80.72Mپاسخ تمرین های دوره ای صفحه 83 شیمی دهم
-گام به گام تمرین های دوره ای صفحه 83 درس ردِّ پای گازها در زندگی
-تمرین های دوره ای صفحه 83 درس 2
-شما در حال مشاهده جواب تمرین های دوره ای صفحه 83 شیمی دهم هستید. ما در تیم مای درس، پاسخنامههای کاملاً تشریحی و استاندارد را مطابق با آخرین تغییرات کتاب درسی 1404 برای شما گردآوری کردهایم. اگر به دنبال بهروزترین پاسخها برای این صفحه هستید و میخواهید بدون نیاز به اتصال به اینترنت، علاوه بر پاسخهای گام به گام، به گنجینهای از مطالب درسی دسترسی پیدا کنید، حتماً اپلیکیشن مایدرس را نصب نمایید.
📥 دانلود اپلیکیشن مایدرس
برای دسترسی آفلاین، سریع و بدون نیاز به اینترنت به گنجینهای از گامبهگامها و نمونه سوالات، اپلیکیشن را نصب کنید.
1) در هریک از واکنش های زیر نام مواد شرکت کننده را بنویسید و آن را موازنه کنید.
\(\begin{array}{l}1)\,\,NaB{H_4} + {H_2}S{O_4} \to {H_2} + N{a_2}S{O_4} + {B_2}{H_6}\\\\2)\,{H_2}S + {O_2} \to S{O_2} + {H_2}O\\\\3)\,Au + NaCN + {O_2} + {H_2}O \to NaAu{(CN)_2} + NaOH\\\\4)\,N{H_3} + {O_2} \to NO + {H_2}O\\\\5)\,CaC{l_2} + NaF \to NaCl + Ca{F_2}\end{array}\)
2) معادله موازنه شده واکنش تولید آمونیاک به صورت زیر است:
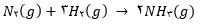
آ) برای تهیه 42/5 کیلوگرم آمونیاک به چند مول گاز هیدروژن نیاز است؟
ب) برای تولید ٣٣٦٠ لیتر آمونیاک در STP به چند گرم گاز هیدروژن و چند گرم گاز نیتروژن نیاز است؟
3) شتر جانوری است که می تواند چندین روز را بدون نوشیدن آب در هوای گرم بیابان سپری کند. در این شرایط، چربی ذخیره شده در کوهان این جانور مطابق واکنش زیر اکسایش یافته و افزون بر تولید انرژی، آب مورد نیاز جانور را نیز تأمین می کند:
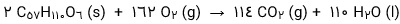
جرم آب تولید شده از اکسایش یک کیلوگرم چربی را حساب کنید.
4) واکنش آلومینیم با آمونیوم پرکلرات مطابق معادله شیمیایی زیر انجام می شود.
\(Al + N{H_4}Cl{O_4} \to A{l_2}{O_3} + AlC{l_3} + {H_2}O + {N_2}\)
(معادله شیمیایی، موازنه نشده است.)
آ) از واکنش 2/16 کیلوگرم آلومینیوم با مقدار کافی از آمونیوم پرکلرات چند لیتر گاز نیتروژن در STP تولید می شود؟
ب) نسبت جرمی آلومینیم کلرید تولید شده به آلومینیم اکسید تولید شده چند است؟
5) گاز شهری به طور عمده از متان تشکیل شده و در محیطی که اکسیژن کم است به صورت ناقص می سوزد و بخار آب، کربن مونوکسید، نور و گرما تولید می کند.
آ) معادله واکنش سوختن ناقص متان را بنویسید و موازنه کنید.
ب) حجم گاز CO حاصل از سوختن ناقص ٤٨ گرم متان در STP چند لیتر است؟
6) در برخی کشورها از اتانول (C2H5OH) به عنوان سوخت سبز به جای سوخت های فسیلی ( گازوئیل، بنزین و... ) استفاده می شود.
آ) معادله واکنش سوخنت کامل اتانول را بنویسید و موازنه کنید.
ب) استفاده از اتانول به جای سوخت های فسیلی چه اثری بر میزان آلایندههایی دارد که به هواکره وارد می شود؟ توضیح دهید.
7) جدول زیر داده هایی را درباره خودروهای یک کشور توسعه یافته نشان می دهد.
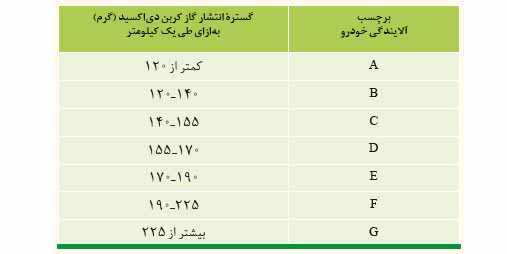
آ) نوعی خودرو در این کشور به ازای طی یک کیلومتر، ١٠٥ گرم گاز کربن دی اکسید منتشر می کند. برچسب این خودرو را تعیین کنید.
ب) هر خودرو به طور میانگین سالانه مسافتی حدود ١٨٠٠٠ کیلومتر طی می کند. حساب کنید سالانه چند کیلوگرم گاز کربن دی اکسید بر اثر استفاده از هر خودرو وارد هواکره می شود؟
پ) فرض کنید این کشور در راستای توسعه پایدار سالانه دو نوع مالیات از مالکان خودرو دریافت می کند. مالیات سالانه برابر با ١٠٠ یورو و مالیات متغیر که به میزان گاز کربن دی اکسید تولید شده از خودرو بستگی دارد. اگر خودروهای دارای برچسب A از پرداخت مالیات متغیر معاف باشند، خودرو با برچسب E سالانه چند یورو مالیات می پردازد؟ (راهنمایی: هر خودرو به ازای تولید هر صد کیلوگرم کربن دی اکسید اضافی دو یورو مالیات متغیر می پردازد.)
1) پاسخ به صورت زیر خواهد بود:
1)
\(\begin{array}{l}NaB{H_4} + {H_2}S{O_4} \to {H_2} + N{a_2}S{O_4} + {B_2}{H_6}\\\\2NaB{H_4} + 1{H_2}S{O_4} \to 2{H_2} + 1N{a_2}S{O_4} + 1{B_2}{H_6}\end{array}\)
2)
\(\begin{array}{l}{H_2}S + {O_2} \to S{O_2} + {H_2}O\\\\2{H_2}S + 3{O_2} \to 2S{O_2} + 2{H_2}O\end{array}\)
3)
\(\begin{array}{l}Au + NaCN + {O_2} + {H_2}O \to NaAu{(CN)_2} + NaOH\\\\4Au + 8NaCN + 1{O_2} + 2{H_2}O \to 4NaAu{(CN)_2} + 4NaOH\end{array}\)
4)
\(\begin{array}{l}N{H_3} + {O_2} \to NO + {H_2}O\\\\4N{H_3} + 5{O_2} \to 4NO + 6{H_2}O\end{array}\)
5)
\(\begin{array}{l}CaC{l_2} + NaF \to NaCl + Ca{F_2}\\\\1CaC{l_2} + 2NaF \to 2NaCl + 1Ca{F_2}\end{array}\)
2) آ) پاسخ به صورت زیر خواهد بود:
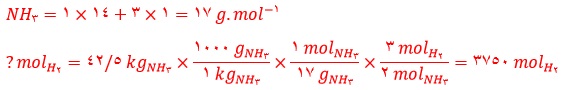
ب)
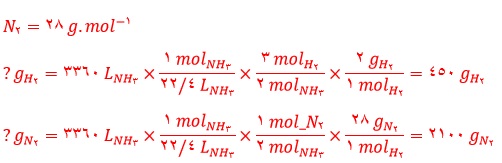
3)
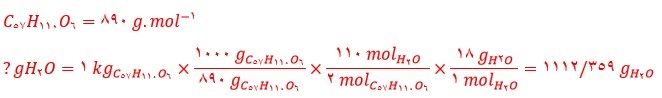
4) آ) ابتدا معادله شیمیایی را موازنه می کنیم:
\(10Al + 6N{H_4}Cl{O_4} \to 4A{l_2}{O_3} + 2AlC{l_3} + 12{H_2}O + 3{N_2}\)
حال مقدار خواسته شده را طبق معادله موازنه شده بدست می آوریم:
\(\begin{array}{l}Al = 27\,\frac{g}{{mol}}\,\,\,,\,\,\,N = 14\,\frac{g}{{mol}}\\\\ \Rightarrow {N_2} = 2 \times 14\,\frac{g}{{mol}} = 28\,\,\frac{g}{{mol}}\\\\ \Rightarrow 2/16\,\,k{g_{Al}} \times \frac{{1000\,\,{g_{Al}}}}{{1\,\,k{g_{Al}}}} \times \frac{{1\,\,mo{l_{Al}}}}{{27\,\,{g_{Al}}}} \times \frac{{3\,\,mo{l_{{N_2}}}}}{{10\,\,mo{l_{Al}}}} \times \frac{{22/4\,\,{L_{{N_2}}}}}{{1\,\,mo{l_{{N_2}}}}}\\\\ = 537/6\,\,{L_{{N_2}}}\end{array}\)
ب) نسبت جرم مولی یک ترکیب به جرم مولی یک ترکیب دیگر را نسبت جرمی گویند:
\(\begin{array}{l}Al = 27{\raise0.5ex\hbox{$\scriptstyle g$} \kern-0.1em/\kern-0.15em \lower0.25ex\hbox{$\scriptstyle {mol}$}}\,\,,\,\,Cl = 35/5{\raise0.5ex\hbox{$\scriptstyle g$} \kern-0.1em/\kern-0.15em \lower0.25ex\hbox{$\scriptstyle {mol}$}}\,\,,\,\,O = 16{\raise0.5ex\hbox{$\scriptstyle g$} \kern-0.1em/\kern-0.15em \lower0.25ex\hbox{$\scriptstyle {mol}$}}\\\\ \Rightarrow \left\{ \begin{array}{l}AlC{l_3} = Al + 3Cl = 27 + 3 \times 35/5 = 133/5{\raise0.5ex\hbox{$\scriptstyle g$} \kern-0.1em/\kern-0.15em \lower0.25ex\hbox{$\scriptstyle {mol}$}}\\\\A{l_2}{O_3} = 2Al + 3O = 2 \times 27 + 3 \times 16 = 102{\raise0.5ex\hbox{$\scriptstyle g$} \kern-0.1em/\kern-0.15em \lower0.25ex\hbox{$\scriptstyle {mol}$}}\end{array} \right.\\\\ \Rightarrow \frac{{\frac{{133/5{g_{AlC{l_3}}}}}{{1mo{l_{AlC{l_3}}}}}}}{{\frac{{102{g_{A{l_2}{O_3}}}}}{{1mo{l_{A{l_2}{O_3}}}}}}} = \frac{{133/5}}{{102}} \simeq 1/31\end{array}\)
5) پاسخ به صورت زیر خواهد بود:
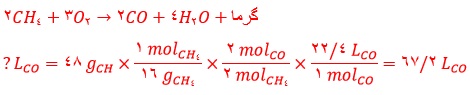
6) آ)
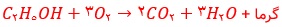
ب) آلاینده ای به همراه ندارد مانند گوگرد و نیتروژن – در تهیه اتانول، کربن دی اکسید که یک گاز گلخانه ایست مصرف می شود از طرف دیگر هنگام سوختن به اکسیژن کمتری نیاز دارد چون در ساختار خود اکسیژن دارد.
7) آ) برچسب این خودرو A خواهد بود.
ب) به عنوان مثال خودرو با برچسب B با میانگین انتشار 130 گرم کربن دی اکسید به ازای یک کیلومتر در نظر گرفته شده است.

پ)

مای درس ، برترین اپلیکیشن کمک درسی ایران
پوشش تمام محتواهای درسی پایه چهارم تا دوازدهم- آزمون آنلاین تمامی دروس
- گام به گام تمامی دروس
- ویدئو های آموزشی تمامی دروس
- گنجینه ای از جزوات و نمونه سوالات تمامی دروس
- فلش کارت های آماده دروس
- گنجینه ای جامع از انشاء های آماده
- آموزش جامع آرایه های ادبی، دستور زبان، قواعد زبان انگلیسی و ... ویژه



1736019749.png)















