درسنامه کامل علوم تجربی هفتم فصل 3 اتم ها؛ الفبای مواد
تعداد بازدید : 7.25Mخلاصه نکات علوم تجربی هفتم فصل 3 اتم ها؛ الفبای مواد - درسنامه شب امتحان علوم تجربی هفتم فصل 3 اتم ها؛ الفبای مواد - جزوه شب امتحان علوم تجربی هفتم نوبت اول فصل 3 اتم ها؛ الفبای مواد
مادّه
مادّه:
به تمام چیزهایی که در اطراف ما وجود دارد و یا هر چیزی که جرم و حجم دارد ماده می گویند. مثل گچ، چوب، فلز، شیشه، چرم، انواع خوراکی ها و … . هر روز با مواد گوناگونی سر و کار داریم که کاربردهای مختلفی در زندگی روزانه اعم از کشاورزی، داروسازی و صنایع دیگر دارند. در زیر مواردی از استفاده های بعضی مواد آمده است:
1- چند مورد از استفاده سنگ مرمر:
در ساخت کف و نمای ساختمان ها، به عنوان سنگ های زینتی در اماکن مذهبی، در مجسمه سازی.
2- چند مورد از استفاده نفت خام :
ساخت مواد گوناگونی مثل انواع داروها، مواد شیمیایی مثل حشره کش ها و همچنین به عنوان سوخت خودروها
3- چند مورد از استفاده نمک خوراکی:
استفاده در صنایع غذایی، ذوب کردن یخ جاده ها، تهیه محلول های سرم.
مای درس ، برترین اپلیکیشن کمک درسی ایران
پوشش تمام محتواهای درسی پایه هفتم- آزمون آنلاین تمامی دروس پایه هفتم
- گام به گام تمامی دروس پایه هفتم
- ویدئو های آموزشی تمامی دروس پایه هفتم
- گنجینه ای از جزوات و نمونه سوالات تمامی دروس پایه هفتم
- فلش کارت های آماده دروس پایه هفتم
- گنجینه ای جامع از انشاء های آماده پایه هفتم
- آموزش جامع آرایه های ادبی، دستور زبان، قواعد زبان انگلیسی و ... ویژه پایه هفتم
اتم و عنصر
اتم:
به ذره های ریز سازنده ی مواد اتم می گویند. اتم ها اصلی ترین ذره های سازنده ی مواد هستند.
نمی توان مستقیما به مشاهده ی اتم ها پرداخت؛ زیرا اتم ها آنقدر ریز هستند که حتی با میکروسکوپ های قوی نیز دیده نمی شوند. دانشمندان چگونه اتم ها را با مطالعه غیر مستقیم اتم ها و اجزای آن ها و بررسی خواص آن ها بررسی می کنند.
اتم ها کنار هم قرار می گیرند و مواد را می سازند. هر ماده از یک یا چند نوع اتم تشکیل شده است. همه مواد موجود در جهان هستی تقریبا از ۹۰ نوع اتم یعنی ۹۰ عنصر ساخته شده اند.
عنصر:
عنصر شکل خاصی از ماده است که یک نوع اتم دارد. برای نمونه عنصر آهن از اتم های آهن و عنصر کربن از اتم های کربن به وجود آمده است. عنصرها به دو گروه تقسیم می شوند: عناصر فلزی و عناصر نا فلزی.
ویژگی عناصر فلزی به صورت زیر است:
۱- سطح براق و درخشانی دارند.
2- از آب سنگین ترند (چگالی شان بیشتر از آب است).
٣- رسانای جریان برق و گرما هستند.
۴- چکش خوارند (بر اثر ضربه نمی شکنند و می توان آن ها را به صورت ورقه ورقه در آورد).
5- در دمای اتاق اکثراً جامدند ( به جز جيوه که مایع است )؛ مانند آهن ، طلا ، نقره ، مس ، جیوه ، آلومینیوم ، سرب و ... .
ویژگی عناصر نافلزی به صورت زیر است:
۱- سطح کدری دارند (براق نیستند ).
۲- از آب سبک ترند ( چگالی شان کمتر از آب است ).
۳- نارسانا یا عایق جریان برق و گرما هستند (به جز کربن یا ذغال).
4- چکش خوار نیستند (بر اثر ضربه می شکنند).
5- همگی در دمای اتاق به صورت گاز یا جامد می باشند ( به جز برم که مایع است ).
عناصر نافلزی مانند هیدروژن، اکسیژن، نیتروژن، گوگرد، کربن و … .
جزوات جامع پایه هفتم
جزوه جامع علوم تجربی هفتم فصل 1 تفکر و تجربه
جزوه جامع علوم تجربی هفتم فصل 2 اندازه گیری در علوم و ابزارهای آن
جزوه جامع علوم تجربی هفتم فصل 3 اتم ها؛ الفبای مواد
جزوه جامع علوم تجربی هفتم فصل 4 موادّ پیرامون ما
جزوه جامع علوم تجربی هفتم فصل 5 از معدن تا خانه
جزوه جامع علوم تجربی هفتم فصل 6 سفر آب روی زمین
جزوه جامع علوم تجربی هفتم فصل 7 سفر آب درون زمین
جزوه جامع علوم تجربی هفتم فصل 8 انرژی و تبدیل های آن
جزوه جامع علوم تجربی هفتم فصل 9 منابع انرژی
جزوه جامع علوم تجربی هفتم فصل 10 گرما و بهینه سازی مصرف انرژِی
جزوه جامع علوم تجربی هفتم فصل 11 یاخته و سازمان بندی آن
جزوه جامع علوم تجربی هفتم فصل 12 سفره ی سلامت
جزوه جامع علوم تجربی هفتم فصل 13 سفر غذا
جزوه جامع علوم تجربی هفتم فصل 14 گردش مواد
جزوه جامع علوم تجربی هفتم فصل 15 تبادل با محیط
مولکول و ترکیب
مولکول:
هنگامی که دو یا چند اتم با یکدیگر پیوند برقرار کنند مولکول را به وجود می آورند.
ترکیب:
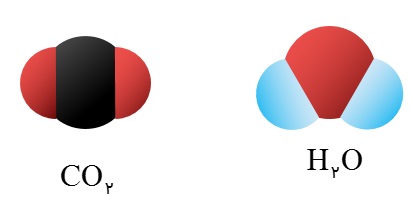
به موادی که ذرات سازنده ی آن مولکول هایی با دو یا چند نوع اتم متفاوت باشند، ترکیب می گویند. به طور مثال مولکول آب یک نوع ترکیب است که از دو نوع اتم هیدروژن و اکسیژن تشکیل شده است و یا مولکول کربن دی اکسید ترکیبی است که از دو نوع اتم کربن و اکسیژن تشکیل شده است.
تقسیم بندی مولکول ها:
الف ) مولکول هایی که از اتصال ۲ یا چند اتم يکسان تشکیل شده اند( عناصر نافلزی یا عناصر مولکولی )؛ مثل اکسیژن، هیدروژن، کلر و نیتروژن ( ۲ اتمی )، فسفر (۴ اتمی) و گوگرد (۸ اتمی).
ب) مولکول هایی که از اتصال ۲ یا چند اتم متفاوت تشکیل شده اند ( ترکیب ها )؛ مثل کربن دی اکسید (۲ اتم اکسیژن و یک اتم کربن ) و آب ( ۲ اتم هیدروژن و یک اتم اکسیژن).
تفاوت های فلز و نافلز
تفاوت های بین ذرات سازنده عناصر فلزی و عناصر نافلزی:
ذرات سازنده عناصر فلزی اتم ها هستند. به طور مثال عنصر فلزی مس از اتم های مس تشکیل شده است .

ولی ذرات سازنده ی عناصر نافلز، مولکول ها می باشند؛ به طور مثال عنصر اکسیژن از مولکول اکسیژن (پیوند بین ۲ اتم اکسیژن) و عنصر گوگرد از مولکول گوگرد (پیوند بین ۸ اتم گوگرد ) ساخته شده اند.

نکته:
به فلزها «عناصر اتمی» و به نافلزها «عناصر مولکولی» نیز گفته می شود. دانشمندان برای درک رفتار مواد و بررسی آن ها، مدلی برای نمایش مواد ارائه می دهند . در این مدل ها اتم ها به صورت گلوله هایی کروی نشان داده می شوند.

مای درس ، برترین اپلیکیشن کمک درسی ایران
پوشش تمام محتواهای درسی پایه هفتم- آزمون آنلاین تمامی دروس پایه هفتم
- گام به گام تمامی دروس پایه هفتم
- ویدئو های آموزشی تمامی دروس پایه هفتم
- گنجینه ای از جزوات و نمونه سوالات تمامی دروس پایه هفتم
- فلش کارت های آماده دروس پایه هفتم
- گنجینه ای جامع از انشاء های آماده پایه هفتم
- آموزش جامع آرایه های ادبی، دستور زبان، قواعد زبان انگلیسی و ... ویژه پایه هفتم
ذره های سازنده اتم
ذره های سازنده ی اتم:
الكترون با نماد e
پروتون با نماد p
نوترون با نماد n
نکاتی درباره اتم ها و ذره های سازنده ی آن ها:
1) اندازه اتم ها با هم برابر نیست.
2) اتم ها دارای هسته می باشند.
3) تعداد الکترون ها، پروتون ها و نوترون ها در اتم های مختلف با هم متفاوت است.
4) پروتون ها و نوترون ها در داخل هسته و الکترون ها در اطراف هسته واقع شده اند.
5) در هر اتم تعداد الکترون ها و پروتون ها با هم برابر است.
6) هر چه ذرات سازنده اتم بیشتر باشند، آن اتم و هسته آن بزرگتر خواهند بود.
7) مواد در طبیعت به سه حالت جامد ، مایع و گاز وجود دارند.
جزوات جامع پایه هفتم
جزوه جامع علوم تجربی هفتم فصل 1 تفکر و تجربه
جزوه جامع علوم تجربی هفتم فصل 2 اندازه گیری در علوم و ابزارهای آن
جزوه جامع علوم تجربی هفتم فصل 3 اتم ها؛ الفبای مواد
جزوه جامع علوم تجربی هفتم فصل 4 موادّ پیرامون ما
جزوه جامع علوم تجربی هفتم فصل 5 از معدن تا خانه
جزوه جامع علوم تجربی هفتم فصل 6 سفر آب روی زمین
جزوه جامع علوم تجربی هفتم فصل 7 سفر آب درون زمین
جزوه جامع علوم تجربی هفتم فصل 8 انرژی و تبدیل های آن
جزوه جامع علوم تجربی هفتم فصل 9 منابع انرژی
جزوه جامع علوم تجربی هفتم فصل 10 گرما و بهینه سازی مصرف انرژِی
جزوه جامع علوم تجربی هفتم فصل 11 یاخته و سازمان بندی آن
جزوه جامع علوم تجربی هفتم فصل 12 سفره ی سلامت
جزوه جامع علوم تجربی هفتم فصل 13 سفر غذا
جزوه جامع علوم تجربی هفتم فصل 14 گردش مواد
جزوه جامع علوم تجربی هفتم فصل 15 تبادل با محیط
مقایسه ویژگی های انواع مواد
مقایسه ویژگی های انواع مواد:
|
ویژگی - حالت |
جامد |
مایع |
گاز |
|
شکل |
شکل معینی دارد |
به شکل ظرف در می آید (شکل معینی ندارد) |
به شکل ظرف در می آید (شکل معینی ندارد) |
|
حجم |
حجم معینی دارد |
حجم معینی دارد |
همه حجم ظرف را پر می کند (حجم معینی ندارد) |
|
آرایش ذره ها |
ثابت و بسیار نزدیک به هم (بسیار فشرده) |
تقریباً فشرده |
بسیار دور از هم |
|
نیروی جاذبه بین ذره ها |
بسیار قوی |
قوی |
خیلی کم (تقریباً وجود ندارد) |
|
سرعت و نوع حرکت ذره ها |
بسیار کند و حرکت در حد لرزیدن |
سرعت کم و حرکت در حد لغزیدن |
بسیار سریع و حرکت آزادانه |
|
مثال |
یخ، شکر و آهن |
آب، روغن و سرکه |
بخار آب و هوا |
|
مدل |
|
|
|
در مواد گازی شکل فاصله ی بین ذره ها بیشتر از جامدها و مایع ها است، به طوری که اگر یک نمونه گاز را وارد ظرف کوچکتری کنیم، اتم ها یا مولکول ها به یکدیگر نزدیک می شوند و فاصله ی بین آن ها کاهش می یابد. به همین دلیل می توان یک گاز را به راحتی متراکم کرد و حجم آن را تا حد زیادی کاهش داد.
نکته:
یک مایع یا جامد را به آسانی و به مقدار زیاد نمی توان متراکم کرد.
انبساط و انقباض
انبساط:
حجم مواد در اثر گرم شدن، افزایش می یابد؛ زیرا با گرم شدن ماده، انرژی جنبشی (حرکتی) ذره های سازنده بیشتر می شود و در نتیجه فاصله ی بین آن ها افزایش می یابد. افزایش حجم مواد در اثر گرم شدن را «انبساط» گویند. وقتی به جسمی گرما می دهیم ، جنبش ذره های سازنده ی آن بیشتر شده و در اثر برخورد به یکدیگر از هم دورتر می شوند و فضای بیشتری را اشغال می کنند. مقایسه میزان انبساط در مواد با یکدیگر با ارائه مثال در زیر آمده است:
جامد های نافلزی < جامدهای فلزی < مایع ها < گازها
مثال:
شیشه < آلومينيوم < آب < گاز اکسیژن
نکته : میزان انبساط آب از الکل بیشتر است.
میزان انبساط آلومینیوم از مس بیشتر است و مس نیز از آهن بیشتر است.
انقباض:
کاهش حجم مواد در اثر گرفتن گرما ( سرد کردن ) را «انقباض» گویند. وقتی از جسمی گرما می گیریم (سردش می کنیم)، جنبش ذره های سازنده ی آن کمتر شده و به یکدیگر نزدیک تر می شوند و فضای کمتری را اشغال می کنند.
تأثیر انتقال گرما به یک ماده جامد در ساختار مولکولی آن:
یخ را به عنوان یک ماده جامد در نظر بگیرید. وقتی به یخ گرما می دهیم، انرژی مولکول های یخ افزایش یافته و جنبش آن بیشتر می شود. اگر این عمل را ادامه دهیم، یخ به آهستگی ذوب و به آب مایع تبدیل می شود.
تأثیر انتقال گرما به یک ماده مایع در ساختار مولکولی آن:
آب را به عنوان یک ماده مایع در نظر بگیرید. اگر به آب گرما بدهیم، جنبش مولکول های آب افزایش می یابد و فاصله بین آن ها نیز بیشتر می شود. اگر مقدار انرژی حرکتی مولکول های آب افزایش پیدا کند، آب تغییر حالت می دهد و به بخار تبدیل می شود.
مای درس ، برترین اپلیکیشن کمک درسی ایران
پوشش تمام محتواهای درسی پایه هفتم- آزمون آنلاین تمامی دروس پایه هفتم
- گام به گام تمامی دروس پایه هفتم
- ویدئو های آموزشی تمامی دروس پایه هفتم
- گنجینه ای از جزوات و نمونه سوالات تمامی دروس پایه هفتم
- فلش کارت های آماده دروس پایه هفتم
- گنجینه ای جامع از انشاء های آماده پایه هفتم
- آموزش جامع آرایه های ادبی، دستور زبان، قواعد زبان انگلیسی و ... ویژه پایه هفتم
انواع حالت های مادّه
انواع حالت های ماده:
1) ذوب:
تبدیل جامد به مایع ( با گرم کردن جامد)؛ مثل ذوب شدن یخ و تبدیل آن به آب.
2) انجماد:
تبدیل مایع به جامد ( با گرما گرفتن یا سرد کردن مایع)؛ مثل : یخ بستن آب.
3) تبخیر:
تبدیل مایع به گاز (با گرم کردن مایع)؛ مثل بخار شدن آب.
4) میعان:
تبدیل گاز به مایع (با گرما گرفتن یا سرد کردن گاز)؛ مثل تشکیل شبنم و بارش باران.
5) تصعید یا فرازش:
تبدیل مستقیم جامد به گاز ( با گرم شدن برخی جامدها در شرایطی خاص ) مثل ناپدید شدن بوگیر دستشویی
6) چگالش:
تبدیل مستقیم گاز به جامد (با گرفتن گرما یا سرد کردن برخی از گازها در شرایطی خاص)؛ مثل تشکیل برفک در یخچال و بارش برف و تگرگ.



1736019749.png)


















