درسنامه کامل فیزیک دهم ریاضی
تعداد بازدید : 515.07kخلاصه نکات فیزیک دهم ریاضی - درسنامه شب امتحان فیزیک دهم ریاضی - جزوه شب امتحان فیزیک دهم ریاضی نوبت اول
مدل سازی
فصل 1 : فیزیک و اندازه گیری
مدل سازی
در ابتدا به تعاریف مورد نیاز در این فصل می پردازیم.
فیزیک چیست؟
واژه ی فیزیک، ریشه در یونان باستان دارد و به معنای شناخت طبیعت است.
فیزیک پایه و اساس تمامی مهندسی ها و فناوری ها است.
نظریه
نتیجه پژوهش درباره علت رخداد یک پدیده که می تواند به کمک آزمایش ثابت و یا باطل شود.
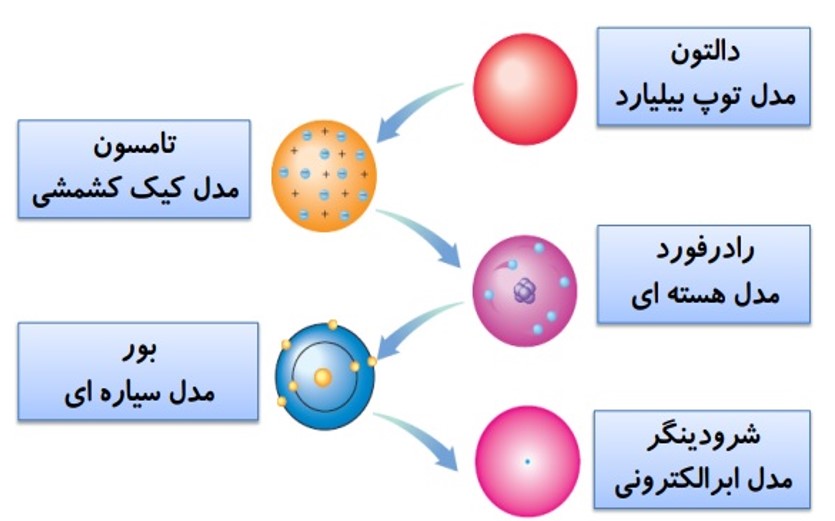
مدل اتمی
نتیجه نظریات دانشمندان مختلف درباره ساختار درون اتم است.
نظریه اتمی که دنیای درون اتم را توصیف می کند چندین بار به خاطر بدست آوردن اطلاعات جدید از رفتار اتم ها اصلاح شد.
قانون های فیزیکی
به گزاره های کلی که دانشمندان رابطه بین برخی از کمیت های فیزیکی را توصیف می کنند، قانون های فیزیکی می گویند. مانند قوانین نیوتون
اصل
به گزاره های مختصری که دانشمندان برای توصیف دامنه محدود تری از پدیده های فیزیکی، که عمومیت کمتری دارند.
مانند اصل پاسکال
مدل سازی در فیزیک
فرایندی است که طی آن یک پدیده فیزیکی، آنقدر ساده و آرمانی می شود تا امکان برسی و تحلیل آن فراهم شود.
مدل سازی تحلیل حرکت توپ بسکتبال در هوا
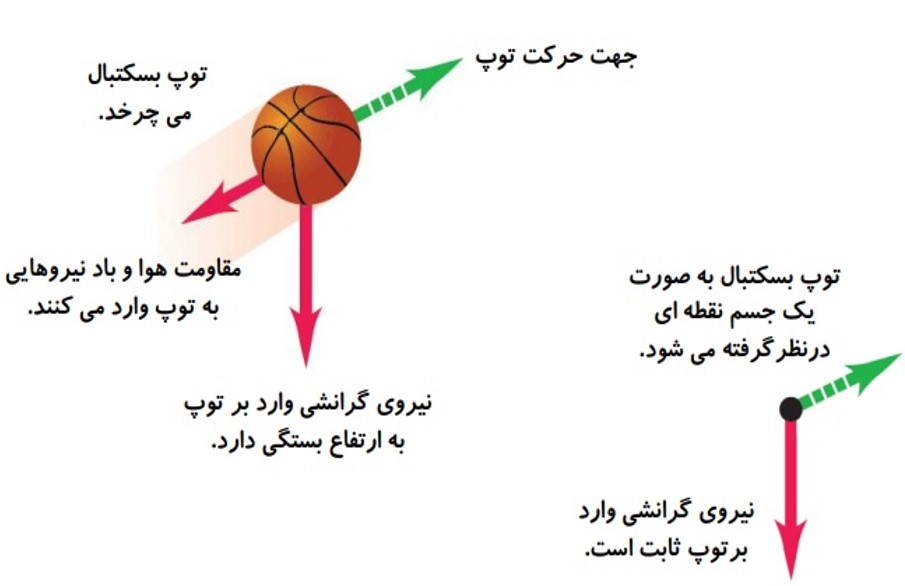
تحلیل حرکت مدل سازی توپ بسکتبال در هوا
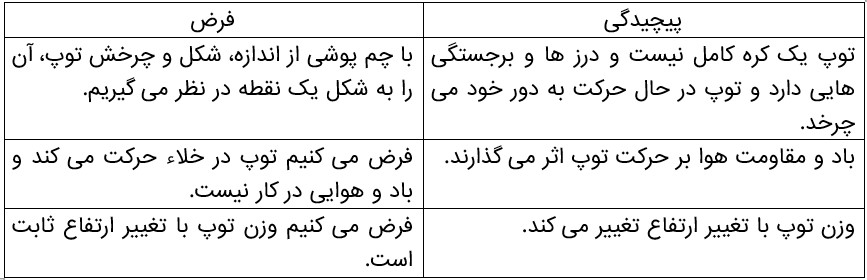
هنگام مدل سازی یک پدیده فیزیکی، باید اثر های جزئی تر را نادیده بگیریم نه اثر های مهم و تعیین کننده را.
فرق کیفیت و کمیت چیست؟
کیفیت:
آنچه را که نتوان اندازه گیری کرد.
مانند زیبایی، مهربانی، بد اخلاقی، کثیفی و ......
کمیت:
آنچه را که بتوان اندازه گیری کرد.
مانند ارتفاع، عمق، حجم، زمان، جرم و .....
یکا یا واحد اندازه گیری:
به مقدار مشخصی از هر کمیت گفته می شود که به عنوان مقیاس انتخاب شده است.
به طور مثال برای طول، یکاهای مختلفی وجود دارد، مانند یک متر، یک کیلومتر و ......
ویژگی های یکای هر کمیت فیزیکی
- تغییر نکنند.
- قابلیت باز تولید در مکان های مختلف داشته باشند.
کمیت های فیزیکی
کمیت های نرده ای:
کمیت هایی که، تنها دارای یک عدد و یکا باشد.
مانند: انرژی، دما، حجم، جرم و زمان و.......
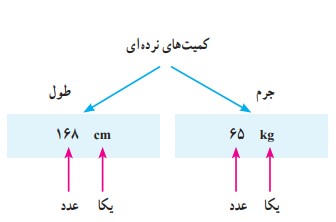
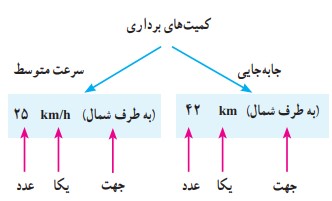
کمیت های برداری:
کمیت هایی که علاوه بر عدد و یکا، دارای جهت باشد.
مانند: جا به جایی، سرعت، شتاب و نیرو و .....
دانشمندان در نشست های بین المللی توافق کرده اند که برای هر کمیت، یکای معینی تعریف کنند.
سیستم SI:
سیستمی است بین المللی که همه کمیت ها در آن دارای واحد مشخص و ثابتی هستند.
کمیت های فیزیکی از نظر یکا به دو دسته تقسیم می شوند:
کمیت های اصلی:
به کمیت هایی که یکای آنها به صورت مستقل تعریف می شود، کمیت های اصلی و به یکاهایشان، یکاهای اصلی گفته می شود.
مانند: طول، جرم، زمان، دما، شدت جریان و مقدار ماده
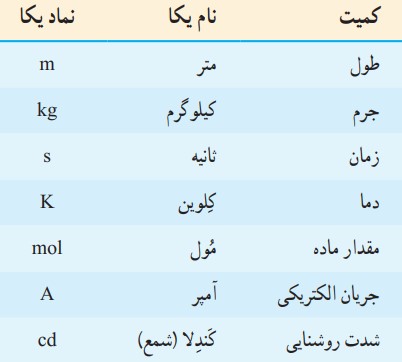
کمیت های اصلی و یکاهای اصلی دستگاه بین المللی (SI)
کمیت های فرعی:
به کمیت هایی که یکاهای آنها بر حسب یکاهای اصلی مشخص می گردد، کمیت های فرعی گفته می شود و به یکاهایشان، یکاهای فرعی می گویند. مانند: مساحت، حجم، انرژی، سرعت، شتاب، چگالی، فشار و ....
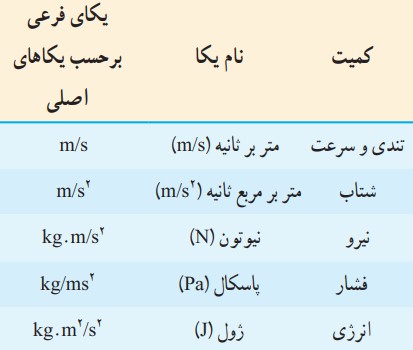
چند مثال از یکاهای فرعی دستگاه بین المللی (SI)
تعریف واحد طول:
یک ده میلیونیم (\(\frac{1}{{10000000}}\) ) فاصله استوا تا قطب شمل است.
واحد طول: یک متر
فاصله میان دو خط نازک حک شده در نزدیکی دو سر میله ای از جنس پلاتین ایریدیوم، وقتی میله در دمای صفر درجه سلسیوس قرار داشت، برابر یک متر تعریف شده بود.
یکای زمان: 1 ثانیه است.
(\(\frac{1}{{86400}}\) ) طول یک شبانه روز
یکای استاندارد جرم
جرم استوانه ای فلزی از جنس پلاتین و ایریدیوم است که در اداره ی بین المللی وزن ها و مقیاس نگه داری می شود.
برخی یکاهای غیر SI طول
یکاهای قدیمی
ذرع
فرسنگ
فوت (پا)
مایل (mi)
اینچ (in)
یکای نجومی (AU): میانگین فاصله زمین تا خورشید (\(1AU \approx 1/5 \times {10^{11}}m\) ) است.
سال نوری (ly): مسافتی است که نور در مدت یکسال طی می کند.
برخی یکاهای غیر SI جرم
یکاهای قدیمی
خروار
من تبریز
مثقال
سیر
نخود
گندم
قیراط
بازه زمانی: \(\Delta t\)
مدت زمان بین شروع و پایان یک رویداد را بازه زمانی می نامیم.
\(\Delta t = {t_2} - {t_1}\)
آهنگ
تغییر هر کمیت را نسبت به زمان، معمولا آهنگ آن کمیت می نامیم.
- آزمون آنلاین تمامی دروس پایه ریاضی
- گام به گام تمامی دروس پایه ریاضی
- ویدئو های آموزشی تمامی دروس پایه ریاضی
- گنجینه ای از جزوات و نمونه سوالات تمامی دروس پایه ریاضی
- فلش کارت های آماده دروس پایه ریاضی
- گنجینه ای جامع از انشاء های آماده پایه ریاضی
- آموزش جامع آرایه های ادبی، دستور زبان، قواعد زبان انگلیسی و ... ویژه پایه ریاضی
تبدیل واحد
فصل 1 : فیزیک و اندازه گیری
تبدیل واحد
1) تبدیل واحد به روش زنجیره ای:
از ریاضیات می دانیم عدد 1 عضو خنثی ضرب است. بر این اساس می توان در فیزیک یکاها را به یکدیگر تبدیل کرد.
در این روش یکای اولیه با ضرب شدن در کسرهایی که صورت و مخرج آن معادل هم هستند، به یکای مورد نظر تبدیل می شوند.
(\(\frac{{100cm}}{{1m}} = 1\) ) و (\(\frac{{1m}}{{100cm}} = 1\) )
مثال
میزی 230 سانتی متر است، طول میز را برحسب متر بیان کنید.
\(230cm = xm \to 230cm \times \frac{{1m}}{{100cm}} = 2/3m\)
نماد گذاری علمی
هر مقدار را به صورت حاصل ضرب عددی بین 1 تا 10 و توان صحیحی از 10 می نویسند.
در بعضی از اندازه گیری ها با مقادیر بسیار بزرگ یا بسیار کوچک سر و کار داریم.
مثال
فاصله ی زمین تا خورشید 150،000،000،000 متر است.
\(150,000,000,000m = 1/5 \times {10^{11}}m\)
جرم یک ذره برابر 0/0000012 گرم می باشد.
\(0/0000012g = 1/2 \times {10^{ - 6}}g\)
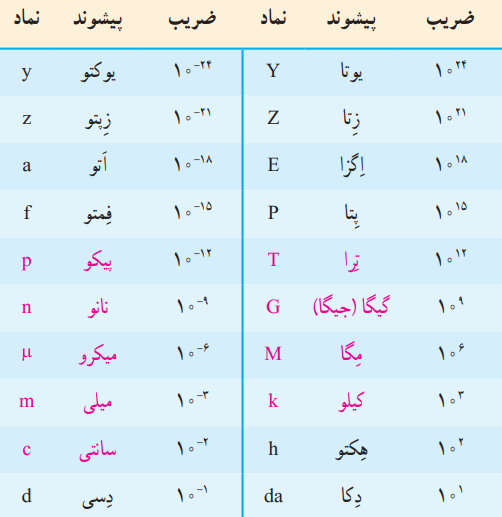
2) حذف پیشوند در تبدیل واحد:
نماد پیشوند را برداشته معادل عددی آن را جای گذاری می کنیم.
مثال
مضرب مگا (\({10^6}\) ) است، نمایش 20 مگاژول برحسب ژول به صورت زیر می باشد.
\(20MJ = X \to X = 20 \times {10^6}J\)
3) حل مسائل با تناسب گیری:
ابتدا زبان فارسی مسئله را به زبان ریاضی در آورده، سپس مجهول را پیدا می کنیم.
مثال
1389 دکا متر چند دسی متر است.
\(1389dam = Xdm \to X = \frac{{1389dam}}{{1dm}} = \frac{{1389 \times {{10}^1}}}{{1 \times {{10}^{ - 1}}}} = 1/389 \times {10^5}\)
1 نماد بعضی از پیشوند ها مشابه نماد بعضی از یکاها است.
2 به طور مثال m برای یکای متر و پیشوند میلی به کار می رود. به چنین تشابهاتی کاملا دقت کنید.
3 اگر در یک اندازه گیری، یکا به توان رسیده باشد، در این گونه موارد پیشوند یکا نیز به توان می رسد.
مثال
305 دکا متر مربع چند دسی متر مربع است؟
\(305{\left( {dam} \right)^2} = X{\left( {dm} \right)^2} \to X = \frac{{305{{\left( {dam} \right)}^2}}}{{{{\left( {dm} \right)}^2}}} = \frac{{305{{\left( {{{10}^1}} \right)}^2}}}{{{{\left( {{{10}^{ - 1}}} \right)}^2}}} = 3/05 \times {10^6}\)
1 1 متر مکعب = 1000 لیتر
2 1 لیتر = 1 دسی متر مکعب
3 1 سی سی = 1 سانتی متر مکعب
4 1 سی سی = 1 میلی لیتر
دقت و خطا
فصل 1 : فیزیک و اندازه گیری
دقت و خطا
دقیق بودن یک اندازه گیری به سه عامل زیر بستگی دارد.
- دقت و حساسیت وسیله اندازه گیری
- مهارت شخص آزمایشگر
- تعداد دفعات اندازه گیری
با انتخاب وسیله های دقیق و روش صحیح اندازه گیری می توان مقدار خطا را کاهش و دقت اندازه گیری را افزایش داد.
1) دقت و حساسیت وسیله اندازه گیری
حداقل مقداری است که یک ابزار اندازه گیری می تواند اندازه گیری کند.
یا کمینه تقسیم بندی مقیاس آن وسیله است.
2) مهارت شخص آزمایشگر
نحوه خواندن نتیجه اندازه گیری است.
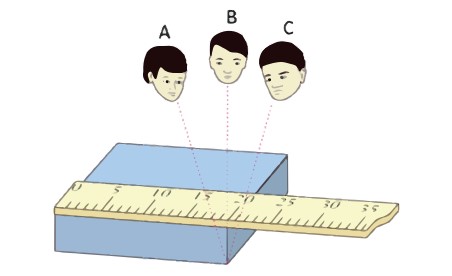
گزارش شخصی که از منظر B نتیجه اندازه گیری را می خواند دقیق تر است.
3) تعداد دفعات اندازه گیری
اندازه گیری آن را چند بار تکرار می کنند. میانگین عدد های حاصل از اندازه گیری به عنوان نتیجه اندازه گیری گزارش می شود.
مثال
در آزمایشی، عدد های 0/3، 2/10، 1/10، 4/10، 0/18 و 7/9 به عنوان نتیجه به دست آمده است. جواب نهایی برای آزمایش چه عددی است؟
اعداد 3 و 18 به علت اختلاف زیادی که با سایر اعداد دارند از میانگین گیری حذف می شوند و نتیجه نهایی به صورت زیر است:
نتیجه نهایی =\(\frac{{9/7 + 10/1 + 10/2 + 10/4}}{4} = 10/1\)
چگالی
فصل 1 : فیزیک و اندازه گیری
چگالی
جرم یکای حجم هر ماده را چگالی آن ماده می نامند:
چگالی \(\rho \) (رو)
\(\rho = \frac{m}{V}\)
که در این فرمول
\(\rho \) به معنای چگالی است.
M به معنای جرم است.
V به معنای حجم است.
در SI، یکای چگالی، \(\frac{{Kg}}{{{m^3}}}\) است.
یکاهای (\(\frac{g}{{c{m^3}}}\) ) و (\(\frac{g}{{lit}}\) ) هم رایج اند.
چگالی جامدات از چگالی مایعات بیشتر و چگالی مایعات از چگالی جامدات از چگالی گاز ها بیشتر است.
هرچه فاصله بین مولکول های یک جسم کمتر باشد، چگالی جسم بیشتر است (چگال تر است).
مثال
چگالی جیوه (\(13600\frac{{Kg}}{{{m^3}}}\) ) است، یعنی چه؟
یعنی هر یک متر مکعب جیوه،\(13600Kg\) جرم دارد.
به چگالی اجسام جرم حجمی نیز گفته می شود.
جرم:
مقدار ماده تشکیل دهنده یک جسم را جرم می گویند.
جرم را معمولا با ترازو اندازه می گیرند.
حجم:
فضایی که یک جسم اشغال می کند.
حجم را با روابط هندسی یا استوانه مدرج اندازه می گیرند.
نحوه محاسبه حجم اشکال:
1) اگر جسم شکل هندسی مشخصی داشته باشد (مکعب، مکعب مستطیل، استوانه و ......) به کمک فرمول های هندسی محاسبه می کنیم.
2) اگر جسم شکل هندسی مشخصی نداشته باشد.
جسم را داخل استوانه مدرجی که حاوی مقدار مشخصی آب است می اندازیم؛ حجم بالا آمده، حجم جسم است (با کم کردن حجم ثانویه از حجم اولیه، حجم بالا آمده محاسبه می شود).
مثال
چگالی کره ای همگن به جرم 2Kg و به شعاع 20cm، چند کیلوگرم بر متر مکعب است؟(\(\pi \cong 3\) )
\(\begin{array}{l}m = 2Kg\\r = 20cm = 0/2m \to V = \frac{4}{3}\pi {r^3} \to V = \frac{4}{3} \times 3 \times {0/2^3} = 4 \times 0/008 = 32 \times {10^{ - 3}}{m^3}\\\rho = ?\\ \to \rho = \frac{m}{V} \to \rho = \frac{2}{{32 \times {{10}^{ - 3}}}} = 62/5\frac{{Kg}}{{{m^3}}}\end{array}\)
1 چگالی اجسامی که دارای حفره (قسمتی از جسم توخالی) است. به شرح زیر محاسبه می گردد:
حجم حفره (فضای خالی) = حجم ظاهری – حجم واقعی
2 اگر دو مایع را مخلوط کنیم و هیچ تغییر حجمی صورت نگیرد، چگالی مخلوط با توجه به تعریف چگالی از رابطه ی زیر بدست می آید:
\(\rho = \frac{{{m_1} + {m_2}}}{{{V_1} + {V_2}}}\)
- آزمون آنلاین تمامی دروس پایه ریاضی
- گام به گام تمامی دروس پایه ریاضی
- ویدئو های آموزشی تمامی دروس پایه ریاضی
- گنجینه ای از جزوات و نمونه سوالات تمامی دروس پایه ریاضی
- فلش کارت های آماده دروس پایه ریاضی
- گنجینه ای جامع از انشاء های آماده پایه ریاضی
- آموزش جامع آرایه های ادبی، دستور زبان، قواعد زبان انگلیسی و ... ویژه پایه ریاضی
حالات ماده
فصل 2 : ویژگی های فیزیکی مواد
حالات ماده
ساختار ماده
ابعاد
- اتم (\({10^{ - 10}}m\)) است.
- مولکول (\({10^{ - 9}}m\)) است.
- هسته اتم در حدود (\({10^{ - 15}}m\)) است.
حالت ماده به چگونگی حرکت ذره های سازنده مواد و اندازه نیروی بین آنها بستگی دارد.
حالت های ماده
جامد ها
مایع ها
گاز ها
پلاسما
جامد
نیروی بین مولکولی در جامد ها، مانند فنر عمل می کند. این نیرو نمی گذارد تا مولکول ها از یک فاصله ی معین نسبت به هم دورتر یا نزدیک تر شوند.
وقتی جامد مانند یک تکه آهن، گرما می گیرد محدوده و دامنه این نوسان ها بیشتر می شود و جسم جامد منبسط می شود.
جامد ها در دو نوع تقسیم بندی می شوند:
الف) جامد بلورین
ب) جامد بی شکل (آمورف)
الف) جامد بلورین:
اتم های برخی از جامد ها در طرح های منظمی کنار هم قرار می گیرند. جامد هایی را که در یک الگوی سه بعدی تکرار شونده از این واحد های منظم ساخته می شود.
نحوه تشکیل جامدات بلورین:
وقتی مایع به آرامی سرد شود، مولکول های مایع فرصت پیدا می کنند که به شکل منظم و ثابتی به خود بگیرند.
مانند: فلزات، نمک ها، الماس، یخ و بیشتر مواد معدنی
ب) جامد بی شکل (آمورف)
مولکول های این جامد در طرح های منظمی قرار نمی گیرند و اصطلاحا به صورت درهم و بی شکل هستند.
نحوه تشکیل جامدات بی شکل:
وقتی مایعی به سرعت سرد شود مولکول های مایع دیگر فرصت ندارند که شکل منظم و ثابتی به خود بگیرند.
مانند: شیشه، چوب، پنبه، عاج
ویژگی مایع ها
1) فاصله مولکول ها در حالت مایع نسبت به حالت جامد آن بیشتر است.
2) مولکول های مایع آزادانه با اطراف حرکت می کنند. همچنین بر روی هم می لغزند.
3) مایع ها تقریبا تراکم ناپذیرند و در نتیجه حجم آنها ثابت است.
اگر فاصله مولکول ها از حدی کمتر شوند نیروی بین مولکولی، دافعه و اگر از حدی بیشتر باشد جاذبه می شوند.
ویژگی گازها
- فاصله مولکول ها حدود چند ده برابر (A35) فاصله مولکول ها در مایع و جامد است. و مولکول ها آزادانه به اطراف حرکت می کنند.
- تراکم پذیرند.
- انرژی جنبشی مولکول های گاز بسیار زیاد است.
علت پخش محلول (نمک و جوهر)
به دلیل حرکت های نامنظم و کاتوره ای (تصادفی) مولکول های آب و برخورد آنها با ذرات سازنده نمک و جوهر، این گونه مواد در آب پخش می شوند.
حرکت بروانی:
حرکت ذره های دود به طور نامنظم و درهم و برهم (کاتوره ای) و در یک مسیر زیگزاگی را حرکت براونی می نامند.
نیروی بین مولکولی در جامدات بیشتر از مایعات و نیروی بین مولکولی در مایعات بیشتر از گاز ها است.
نیروی بین مولکولی
فصل 2 : ویژگی های فیزیکی مواد
نیروی بین مولکولی
انواع نیروی بین مولکولی:
- نیروی هم چسبی
- نیروی دگر چسبی
1) نیروی هم چسبی
نیروی جاذبه بین مولکول های همسان است.
مانند نیروی بین مولکول های یک قطره آب یا جیوه
2) نیروی دگر چسبی
نیروی جاذبه بین مولکول های ناهمسان است.
مانند نیروی بین مولکولی بین سطح شیشه و آبی که روی آن ریخته شده است.
نیروی کشش سطحی
به علت هم چسبی مولکول های سطح مایع، سطح یک ماده مانند یک پوسته تحت کشسان عمل می کند، این رفتار سطح را کشش سطحی می گویند.
1 در سطح مایع به دلیل تغییر از وضعیت مایع به بخار فاصله بین مولکول ها افزایش و نیرو های بین مولکولی به صورت جاذبه (سطح مایع تحت کشش) ظاهر می شود.
2 افزایش دما موجب کاهش نیروی هم چسبی و دگر چسبی می شود.
لوله های مویین:
لوله هایی معمولا از جنس شیشه با قطر های مختلف بسیار نازک که هر دو سر آنها باز می باشد. (قطر داخلی آنها حدود یک میلی متر است.)
مویینگی:
به بالا رفتن وپایین آمدن مایع ها از لوله های بسیار باریک را مویینگی می گوییم.
1 چون جهت نیرویی که سطح لوله مویین به آب وارد می کند به سمت بالا است. در نتیجه آب درون لوله بالا می رود و سطح آب درون لوله به صورت فرورفتگی است.
2 ارتفاع مایع درون لوله با شعاع لوله و چگالی مایع نسبت وارون دارد.
3 چون جهت نیرویی که سطح لوله مویین به جیوه وارد می کند به سمت پایین است. در نتیجه جیوه درون لوله پایین می رود و سطح آب درون لوله به صورت برآمدگی است.
فشار در شاره های ساکن
فصل 2 : ویژگی های فیزیکی مواد
فشار در شاره های ساکن
فشار متوسط:
بزرگی نیروی عمودی که بر واحد سطح جسم وارد می شود.
فرمول فشار (P)
\(P = \frac{{{F_ \bot }}}{A}\)
که در فرمول (P) به معنای فشار
(\({F_ \bot }\)) به معنای نیروی عمودی
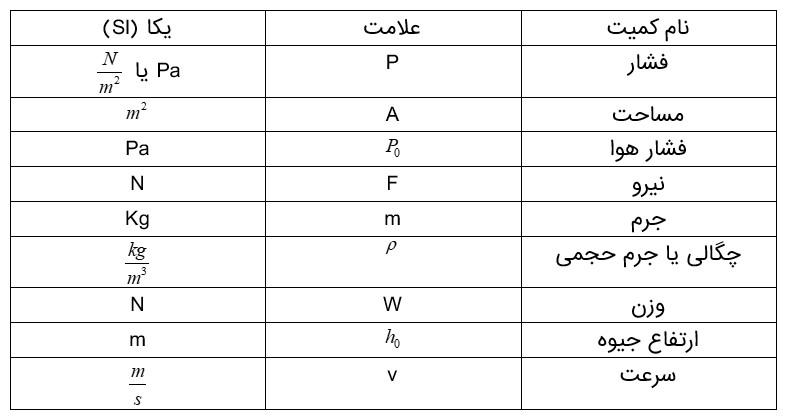
و (A) به معنای مساحت سطح است.
1 یکای فشار در SI به صورت نیوتن بر متر مربع (\(\frac{N}{{{m^2}}}\)) است که به آن در اصطلاح پاسکال، (Pa) گفته می شود.
2 فشار کمیتی نرده ای می باشد و فاقد جهت و راستا است.
مثال
اگر انگشتتان را روی سطح میز طوری قرار دهیم که سطح تماس حدود\(1c{m^2}\) باشد، چه نیروی باید وارد کنیم تا فشار در محل انگشتتان تقریبا \(1 \times {10^5}Pa\) باشد؟
\(\begin{array}{l}A = 1c{m^2} = 1 \times {10^{ - 4}}{m^2}\\F = ?\\P = {10^5}Pa\\ \to P = \frac{F}{A} \to F = PA \to F = {10^5} \times {10^{ - 4}} = 10N\end{array}\)
اختلاف فشار ستون شاره در دو سطح شاره های یکسان:
نیروی وارد بر سطح 2 برابر با حاصل جمع وزن مایع بین دو سطح و نیروی وارد از ظرف سطح 1 می باشد.
\({P_2} = {P_1} + \rho gh\)
فشار در مایع ها به شکل ظرف بستگی ندارد.
قانون هم فشاری:
فشار نقاط هم تراز درون یک مایع یکسان است.
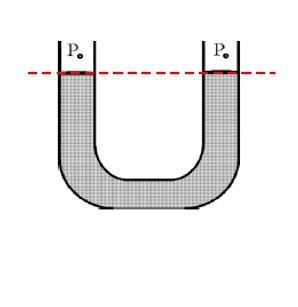
اختلاف فشار مایع در دو سطح به عوامل زیر بستگی دارد:
- با عمق مایع (ارتفاع از سطح آب) نسبت مستقیم دارد.
- با چگالی مایع نسبت مستقیم دارد.
- با شتاب گرانش (زمین، ماه) رابطه ی مستقیم دارد.
فشار مایع ها به چه عواملی بستگی ندارد:
- با وزن مایع
- به اندازه ی مساحت قاعده ظرف
- به شکل ظرف
مثال
جسمی مکعبی به طول ضلع \(20cm\) درون شاره ای غوطه ور و در حال تعادل است. فشار در بالا و زیر جسم برابر 105 و \(106/8\) کیلو پاسکال است. چگالی شاره چند کیلوگرم بر متر مکعب است؟
\(\begin{array}{l}h = 20cm = 0/2m\\{P_1} = 105KPa = 105000Pa\\{P_2} = 106/8KPa = 106000Pa\\g = 10\frac{N}{{Kg}}\\\rho = ?\\{P_2} = {P_1} + \rho gh \to 106000 = 105000 + \rho \times 10 \times 0/2\\ \to 1800 = 2\rho \to \rho = 900\frac{{Kg}}{{{m^3}}}\end{array}\)
عامل وجود فشار هوا
1) بر جسم های روی زمین:
نیروی وزن هوای اطراف زمین است.
2) در ظرف بسته:
عامل فشار، جنبش مولکولی گاز است.
فشار کل در عمق h درون یک شاره، از جمع فشار هوا با فشار ارتفاع ستون مایع، فشار کل درون ظرف، بدست می آید.
\(P = \rho gh + {P_0}\)
در این فرمول:
(P) فشار کل در مایع،
(\(\rho \)) چگالی مایع،
(g) شتاب گرانش،
(h) ارتفاع ستون مایع
و (\({P_0}\)) فشار هوا است.
مثال
فشار آب در عمق 3 متری از سطح آزاد آن، چند پاسکال است؟
\(\begin{array}{l}P = ?\\\rho = 1000\frac{{Kg}}{{{m^3}}}\\g = 10\frac{N}{{Kg}}\\h = 3m\\{P_0} = {10^5}Pa\\ \to P = \rho gh + {P_0} \to P = 1000 \times 10 \times 3 + {10^5}\\ \to P = 130000Pa\end{array}\)
1 هرچه از سطح زمین بالاتر برویم، به علت رقیق شدن هوا و کاهش تعداد ذره ها، فشار هوا کاهش می یابد و هرچه به سطح دریا نزدیک تر می شویم، فشار هوا افزایش می یابد.
2 تا ارتفاع 2000 متری از سطح زمین: به ازای هر 10m که از سطح زمین بالا می رویم فشار هوا تقریبا یک میلی متر جیوه کاهش می یابد.
3 چگالی آب بسیار کمتر از چگالی جیوه است.
- آزمون آنلاین تمامی دروس پایه ریاضی
- گام به گام تمامی دروس پایه ریاضی
- ویدئو های آموزشی تمامی دروس پایه ریاضی
- گنجینه ای از جزوات و نمونه سوالات تمامی دروس پایه ریاضی
- فلش کارت های آماده دروس پایه ریاضی
- گنجینه ای جامع از انشاء های آماده پایه ریاضی
- آموزش جامع آرایه های ادبی، دستور زبان، قواعد زبان انگلیسی و ... ویژه پایه ریاضی
فشار سنج توریچلی
فصل 2 : ویژگی های فیزیکی مواد
فشار سنج توریچلی
چگونه با استفاده از جو سنج جیوه ای (بارو متر) می توان فشار هوای محیط را اندازه گرفت؟(آزمایش توریچلی)
- ابتدا یک لوله شیشه ای به طول حدود 80cm را که یک سر آن بسته است، از جیوه پر می کنیم.
- سپس دهانه لوله را محکم با انگشت گرفته و آن را درون یک ظرف محتوی جیوه واژگون می کنیم.
- با برداشتن انگشت، جیوه درون لوله کمی پایین می آید و در ارتفاعی (که متناسب با فشار هوا در محل آزمایش است) ثابت می ماند، ارتفاع ستون جیوه ی درون لوله، نشان دهنده ی فشار هوای محیط است.
فرمول برای پیدا کردن فشار هوا:
\({P_0} = \rho g{h_0}\)
با اندازه گیری ارتفاع ستون جیوه در آزمایش توریچلی \({h_0}\)، می توان فشار هوا را در محل آزمایش از رابطه ی زیر به دست می آورد.
مثال
آزمایش توریچلی را در محلی که در کنار سطح دریای آزاد است، انجام داده ایم. ارتفاع ستون جیوه 76 سانتی متر شده است. فشار هوا چند پاسکال است؟ (\(g = 9/8\frac{N}{{Kg}}\) و چگالی جیوه \(\rho = 13600\frac{{Kg}}{{{m^3}}}\))
\(\begin{array}{l}{h_0} = 76cm = 0/76m\\{\rho _{Hg}} = 13600\frac{{Kg}}{{{m^3}}}\\g = 9/8\frac{N}{{Kg}}\\{P_0} = ?\\{P_0} = {\rho _{Hg}}g{h_0} \to {P_0} = 13600 \times 9/8 \times 0/76 \to {P_0} = 101292Pa\end{array}\)
فشار هوای درون لوله به ارتفاع عمودی مایع درون لوله بستگی دارد.
فشار گازهای مخزن
فصل 2 : ویژگی های فیزیکی مواد
فشار گازهای مخزن
علت فشار گاز ها:
به علت برخورد مداوم مولکول های گاز به جداره ظرف، فشار ایجاد می شود و هر چقدر دمای گاز بیشتر باشد، انرژی جنبشی مولکول های گاز نیز بیشتر شده و فشار آن افزایش پیدا می کند.
فشار پیمانه ای (سنجه ای) \({P_g}\)
به اختلاف فشار گاز درون مخزن و فشار هوا، فشار پیمانه ای می گویند.
فشار سنج، فشارپیمانه ای را اندازه می گیرد.
\({P_g} = P - {P_0}\)
فشار گاز ها را با فشار سنج U شل اندازه گیری می کنند.
اندازه گیری فشار گاز درون مخزن (مانومتر):
فشار سنج: لوله U شکل محتوی یک مایع است که یک سر لوله U شکل را به مخزن متصل نموده و سر دیگر آن در تماس با هوای آزاد قرار می دهند.
پس از باز کردن شیر مخزن، گاز به مایع درون لوله فشار آورده و آن را پایین می راند، در نتیجه سطح مایع در دو شاخه لوله به اندازه ارتفاع h بالا می رود. از روی همین اختلاف ارتفاع، می توان فشار گاز را حساب کرد.
فشار گاز
چون در سطح های هم تراز فشار یکسان است، خواهیم داشت:
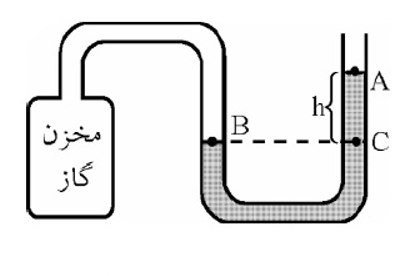
فشار نقطه B = فشار نقطه C
فشار در نقطه C = فشار ستون مایع + فشار هوا
\(\begin{array}{l}{P_B} = {P_C}\\{P_C} = \rho gh + {P_0}\\{P_B} = P\\P = \rho gh + {P_0}\\{P_g} = \rho gh\end{array}\)
در این فرمول
(P) فشار گاز
(\(\rho \)) چگالی مایع (جیوه)
(g) شتاب گرانش
(h) ارتفاع ستون مایع
(\({P_g}\)) فشار پیمانه ای
(\({P_0}\)) فشار هوا
اگر فشار مخزن کمتر از فشار هوا باشد، مایع درون لوله سمت چپ به سمت بالا می رود. در نتیجه سطح مایع در دو شاخه لوله به اندازه ارتفاع h بالا می رود، از روی همین اختلاف ارتفاع، می توان فشار گاز را حساب کرد.
\(\begin{array}{l}{P_C} = {P_B}\\{P_0} = \rho gh + P\\P = {P_0} - \rho gh\end{array}\)
اصل ارشمیدس
فصل 2 : ویژگی های فیزیکی مواد
اصل ارشمیدس
وقتی تمام یا قسمتی از یک جسم در شاره ای فرو رود، شاره نیرویی بالاسو بر آن وارد می کند که با وزن شاره جا به جا شده توسط جسم برابر است.
به جسم های درون یک شاره یا غوطه ور در آن، همواره نیروی بالاسوی خالصی به نام نیروی شناوری از طرف شاره وارد می شود.
عامل نیروی شناوری چیست؟
چون فشار شاره در قسمت های عمیق تر بیشتر است؛ نیرویی که از طرف شاره به بخش های عمیق تر وارد می شود نیز بیش تر است در نتیجه نیروی خالصی که به جسم وارد می شود به سمت بالا خواهد بود.
نیروی شناوری \({F_b}\)
به نیروی بالا سوی خالصی که به جسم درون شاره وارد شده و با وزن شاره جا به جا شده برابر است؛ نیروی شناوری می گویند.
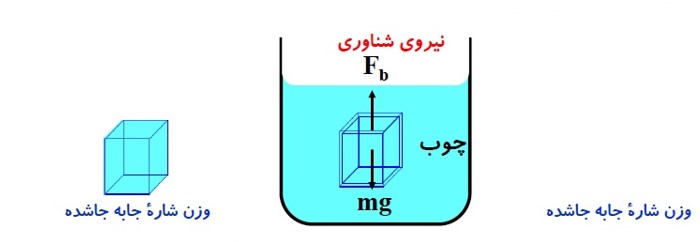
حالت های ممکن برای جسم قرار گرفته در شاره:
1) شناوری: حجم جسم بیشتر از حجم شاره جا به جا شده برابر است.
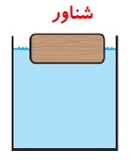
2) غوطه ور: حجم جسم و حجم شاره جا به جا شده برابر است.
3) فرورفته: حجم جسم با حجم شاره جا به جا شده برابر است.
1 شرط غوطه وری و فرو رفتن این است که چگالی جسم بزرگتر یا برابر چگالی شاره باشد.
2 شناور ماندن روی آب ربطی به وزن اجسام ندارد و فقط به چگالی آنها بستگی دارد.
نیروی شناوری
جسمی مکعبی شکل به ضلع L را در نظر بگیرید که درون شاره ساکنی با چگالی \(\rho \) غوطه ور است. شکل زیر نیروهایی را نشان می دهد که شاره به سطح این جسم وارد می کند.
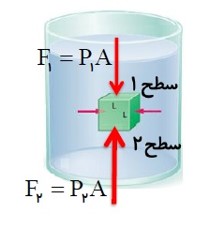
نیروی های افقی وارد به جسم یکدیگر را خنثی می کنند.
\({F_b} = \rho vg\)
در این فرمول
(\(\rho \)) چگالی شاره
(v) حجم شاره جا به جا شده است.
نیروی شناوری به عوامل زیر بستگی دارد:
- چگالی شاره
- حجم شاره جا به جا شده
- شتاب گرانش در آن محل
- جرم شاره جا به جا شده
نیروی شناوری به عوامل زیر بستگی ندارد:
- وزن جسم
- چگالی جسم
- عمق شاره
- آزمون آنلاین تمامی دروس پایه ریاضی
- گام به گام تمامی دروس پایه ریاضی
- ویدئو های آموزشی تمامی دروس پایه ریاضی
- گنجینه ای از جزوات و نمونه سوالات تمامی دروس پایه ریاضی
- فلش کارت های آماده دروس پایه ریاضی
- گنجینه ای جامع از انشاء های آماده پایه ریاضی
- آموزش جامع آرایه های ادبی، دستور زبان، قواعد زبان انگلیسی و ... ویژه پایه ریاضی
اصل برنولی
فصل 2 : ویژگی های فیزیکی مواد
اصل برنولی
اصل برنولی، برای شاره ای که به طور لایه ای و در امتداد افق حرکت می کند:
در مسیر حرکت شاره، با افزایش تندی شاره، فشار داخل شاره کاهش می یابد.
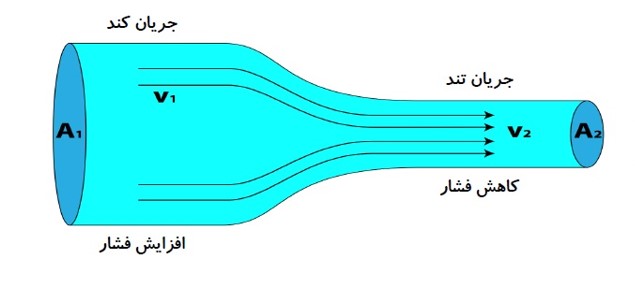
جریان پایا:
به جریانی که در آن تندی همه ذراتی که از یک نقطه می گذرند، ثابت باشد.
1 اصل برنولی بر طبق این فرضیات است:
2 شاره تراکم ناپذیر است.
3 هنگام حرکت شاره اصطکاک داخلی وجود ندارد.
4 حرکت شاره پایا است (متلاطم نیست).
آهنگ جریان شاره:
نسبت حجم شاره جا به جا شده به زمان سپری شده
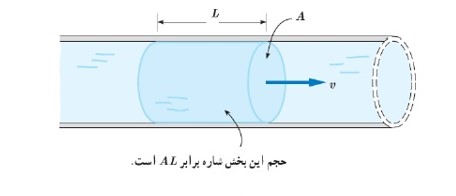

\(\frac{{AL}}{t} = Av\)
در این فرمول
(A) سطح مقطه لوله
(v) تندی شاره است.
معادله پیوستگی
در یک شاره تراکم ناپذیر، مقدار شاره ای که در زمان t از سطح مقطع \({A_1}\) می گذرد. درست برابر مقدار شاره ای است که در همین زمان از سطح مقطع \({A_2}\) می گذرد.
\({A_1}{v_1} = {A_2}v{}_2\)
در معادله پیوستگی باید یکاهای A و v در دو طرف معادله یکسان باشد.
مثال
سطح مقطع یک سرنگ پر از آب \(0/4c{m^2}\) و سطح مقطع دهانه خروجی آن \(0/4m{m^2}\) است. اگر سرنگ با تندی \(1/5\frac{{cm}}{s}\) فشرده شود، تندی خروجی آب از دهانه آن چقدر است؟
\(\begin{array}{l}{A_1} = 0/4c{m^2}\\{A_2} = 0/4m{m^2} = 0/4 \times {10^{ - 2}}c{m^2}\\{v_1} = 1/5\frac{{cm}}{s}\\{v_2} = ?\\1mm = 0/1cm\\{A_1}{v_1} = {A_2}{v_2}\\0/4 \times 1/5 = 0/4 \times {10^{ - 2}} \times {v_2} \to {v_2} = \frac{{1/5}}{{{{10}^{ - 2}}}} = 150\frac{{cm}}{s}\end{array}\)
کاربرد های اصل برنولی:
- باریک شدن ستون آب وقتی شیر آّ را کمی باز می کنیم.
- حرکت ورق کاغذ وقتی در دهان خود بر سطح بالایی کاغذ به سرعت بدمیم.
- پف کردن پوشش برزنتی روی اتاقک عقب کامیون هنگام حرکت
- طراحی بال هواپیما
- دستگاه سمپاش
رابطه مقایسه ای اصل برنولی:
\(\begin{array}{l}{A_1}{v_1} = {A_2}{v_2} \to \frac{{{v_2}}}{{{v_1}}} = \frac{{{A_1}}}{{{A_2}}}\\A = \pi {r^2}\\r = \frac{D}{2} \to A = \pi \frac{{{D^2}}}{4}\\ \to \frac{{{v_2}}}{{{v_1}}} = {(\frac{{{D_1}}}{{{D_2}}})^2}\end{array}\)
شناسنامه ویژگی های فیزیکی مواد
انرژی جنبشی
فصل 3 : کار، انرژی و توان
انرژی جنبشی
به انرژی که یک جسم صرفا (فقط) به علت حرکت دارد، انرژی جنبشی می گویند.
1 هرچه جسمی جرم بیشتری داشته باشد، انرژی جنبشی آن نیز بیشتر خواهد بود.
2 هرچه جسم در حال حرکت تندی بیشتری داشته باشد، انرژی جنبشی آن نیز بیشتر خواهد بود.
انرژی جنبشی به عوامل زیر بستگی دارد:
- با جرم جسم m رابطه مستقیم دارد.
- با مجذور تندی v رابطه مستقیم دارد.
اگر تندی جسمی 3 برابر شود، انرژی جنبشی آن 9 برابر می شود.
فرمول انرژی جنبشی:
\(K = \frac{1}{2}m{V^2}\)
در این فرمول
(K) انرژی جنبشی است و بر حسب ژول است،
(m) جرم است و بر حسب کیلوگرم است،
(V) تندی است و بر حسب متر بر ثانیه است.
مثال
گلوله ای به جرم 200 گرم با تندی 108 کیلومتر بر ساعت در حال حرکت است، انرژی جنبشی آن چند ژول می باشد؟
\(\begin{array}{l}m = 200g \div 1000 = \frac{2}{{10}}Kg\\V = 108\frac{{Km}}{h} \div 3/6 = 30\frac{m}{s}\\K = ?\\K = \frac{1}{2}m{V^2} \to K = \frac{1}{2} \times \frac{2}{{10}} \times {(30)^2} = \frac{1}{{10}} \times 900 \to K = 90J\end{array}\)
تغیرات انرژی جنبشی
\({K_1}\): انرژی جنبشی در نقطه اول
\({K_2}\): انرژی جنبشی جسم در نقطه دوم
تغییر انرژی جنبشی:
\(\Delta K = {K_2} - {K_1}\)
رابطه مقایسه انرژی دو جسم با جرم و تندی های متفاوت:
\(K = \frac{1}{2}m{V^2} \to \frac{{{K_2}}}{{{K_1}}} = \frac{{{m_2}}}{{{m_1}}} \times {\left( {\frac{{{V_2}}}{{{V_1}}}} \right)^2}\)
در تمرینات انرژی جنبشی اگر خواسته شود:
انرژی جنبشی چقدر می شود.
\(K = \frac{1}{2}m{V^2}\)
انرژی جنبشی چقدر تغییر می کند.
\(\Delta K = {K_2} - {K_1}\)
انرژی جنبشی چند برابر می شود.
\(\frac{{{K_2}}}{{{K_1}}}\)
انرژی جنبشی چند درصد تغییر می کند.
\(\frac{{{K_2} - {K_1}}}{{{K_1}}} \times 100\% \)
فرمول کار
فصل 3 : کار، انرژی و توان
فرمول کار
مفهوم جا به جایی نقطه اثر نیرو چیست؟
یعنی با جا به جایی نقطه اثر نیرو، هم جسم جا به جا شده، هم نیروی متصل به جسم جا به جا می شود.
تعریف کار از دید فیزیک:
جا به جایی نقطه اثر نیرو که برابر است با:
کار = حاصل ضرب (نیرو در راستای جا به جایی) در جا به جایی
بردار یکه
I برداری است به طول واحد و در جهت محور x ها
J برداری است به طول واحد و در جهت محور y ها
فرمول کار نیروی F:
\(W = Fd\cos \theta \)
در این فرمول
(W) کار نیروی F
(F) نیرو
(d) جا به جایی جسم
(\(\cos \theta \)) زاویه بین نیرو و جا به جایی است.
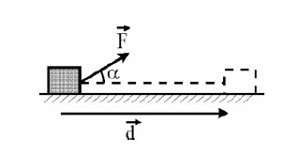
کار جهت و راستا ندارد بنابراین کمیتی نرده ای است.
مثال
نیروی \(100N\) که با سطح افق زاویه 60 درجه می سازد، جسمی را به اندازه \(20m\) در سطح افقی جا به جا می کند. کار انجام شده چقدر است؟ (\(\cos {60^0} = 0/5\))
\(\begin{array}{l}F = 100N\\d = 20m\\\theta = {60^0}\\\cos {60^0} = 0/5\\W = Fd\cos \theta \to W = 100 \times 20 \times 0/5 = 1000J\end{array}\)
کار وارد بر جسم در شرایط زیر برابر صفر است:
- نیرو وارد شود ولی جسم جا به جا نشود.
- بر یک جسم نیرو وارد نشود.
- راستای نیرو و جا به جایی بر هم عمود باشند. (\(\cos {90^0} = 0\))
کار وارد بر جسم در شرایط زیر منفی است:
- کار نیرویی اصطکاک
- کار نیروی مقاومت هوا
- کار نیروی مقاومت شاره
هرگاه به جسمی بیش از یک نیرو اثر نماید؛ کل کار بر طبق زیر بدست می آید:
\({W_T} = {W_1} + {W_2} + {W_3} + ...\)
همچنین برابر با کار نیروی برآیند وارد بر جسم است:
\({W_T} = {F_T}d\cos \theta \)
- آزمون آنلاین تمامی دروس پایه ریاضی
- گام به گام تمامی دروس پایه ریاضی
- ویدئو های آموزشی تمامی دروس پایه ریاضی
- گنجینه ای از جزوات و نمونه سوالات تمامی دروس پایه ریاضی
- فلش کارت های آماده دروس پایه ریاضی
- گنجینه ای جامع از انشاء های آماده پایه ریاضی
- آموزش جامع آرایه های ادبی، دستور زبان، قواعد زبان انگلیسی و ... ویژه پایه ریاضی
معرفی چند نیرو و کار آنها
فصل 3 : کار، انرژی و توان
معرفی چند نیرو و کار آنها
انواع نیرو ها:
1) نیروی محرک: F
2) نیروی وزن: W
3) نیروی عمودی تکیه گاه: \({F_N}\)
4) نیروی اصطکاک:
اصطکاک ایستایی \({f_s}\)
اصطکاک جنبشی \({f_k}\)
1) نیروی محرک:
نیرو هایی که باعث حرکت یک جسم می شوند. نیروی محرک نام دارد.
1 تمام نیرو هایی که در جهت حرکت اند، محرک محسوب می شوند.
2 تمام نیروی هایی که در خلاف جهت حرکت اند مقاوم محسوب می شوند.
2) نیروی وزن:
نیروی گرانشی که زمین به جسم وارد می کند، نیروی وزن جسم نام دارد.
حهت نیروی وزن همیشه به سمت مرکز زمین است.
3) نیروی عمودی تکیه گاه:
نیروی قائمی که از طرف تکیه گاه بر جسم اثر می کند.
1 این نیرو ناشی از تغییر شکل سطح تماس دو جسم است.
2 جهت نیروی عمودی تکیه گاه بستگی به طرز قرار گرفتن جسم روی سطح جسم دیگر دارد.
4) نیروی اصطکاک:
نیرویی در سطح تماس دو جسم، که با حرکت جسم نسبت به جسم دیگر مخالفت می کند که به آن نیروی اصطکاک می گوییم.

نیروی اصطکاک در خلاف جهت حرکت نسبی اثر می کند که:
موازی با سطح
عمود بر نیروی قائم N است.
انواع نیروی اطکاک:
- نیروی اصطکاک ایستایی: به اصطکاک جسم در حال سکون می گویند.
- نیروی اصطکاک جنبشی: به اصطکاک جسم در حال حرکت می گویند.
کار نیرو های مختلف
1) کار نیروی محرک (نیروی موتوری)
2) کار نیروی وزن
الف) در جا به جایی افقی
ب) در جا به جایی قائم
3) کار نیروی عمودی تکیه گاه
الف) در جا به جایی افقی
ب) در جا به جایی قائم
4) کار نیروی اصطکاک
الف) ایستایی
ب) جنبشی
1) کار نیروی محرک (نیروی موتوری)
اگر نیروی جلوران با راستای جا به جایی موازی باشد، کار نیروی جلوران ماکزیمم است.
\(\begin{array}{l}{W_F} = F \times d \times \cos {0^0}\\{W_F} = F \times d \times 1\\{W_F} = Fd\end{array}\)
2) کار نیروی وزن
الف) در جا به جایی افقی:
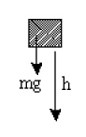
چون نیروی وزن بر راستای جا به جایی عمود می باشد، کار نیروی وزن صفر است.
\(\begin{array}{l}{W_{mg}} = mg \times d \times \cos \alpha \\{W_{mg}} = mg \times d \times \cos {90^0}\\ \to \cos {90^0} = 0 \to {W_{mg}} = 0j\end{array}\)
2) کار نیروی وزن
ب) در جا به جایی قائم (به سمت بالا):
چون در راستای نیروی وزن با جا به جایی در خلاف جهت هم هستند، پس \(\alpha = {180^0}\) می باشد و کار نیروی وزن در این جا به جایی از رابطه زیر محاسبه می شود:
\(\begin{array}{l}{W_{mg}} = mg \times d \times \cos \alpha \\{W_{mg}} = mg \times d \times \cos {180^0}\\ \to \cos {180^0} = - 1 \to {W_{mg}} = - mg \times h\end{array}\)
2) کار نیروی وزن
ج) در جا به جایی قائم (به سمت پایین):
\(\begin{array}{l}{W_{mg}} = mg \times d \times \cos \alpha \\{W_{mg}} = mg \times d \times \cos {0^0}\\ \to \cos {0^0} = 1 \to {W_{mg}} = mgh\end{array}\)
3) کار نیروی عمودی تکیه گاه
الف) در جا به جایی افقی
چون نیروی عمودی تکیه گاه N همیشه عمود بر سطح است، بنابراین زاویه آن با جا به جایی روی هر سطحی برابر \({90^0}\) است، در نتیجه کار نیروی عمودی تکیه گاه \({W_N}\) برابر صفر می باشد.
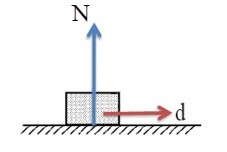
\(\begin{array}{l}{W_N} = {F_N} \times d \times \cos \alpha \\{W_N} = {F_N} \times d \times \cos {90^0}\\ \to \cos {90^0} = 0 \to {W_N} = 0\end{array}\)
3) کار نیروی عمودی تکیه گاه
ب) در جا به جایی قائم (به سمت بالا)
چون زاویه ی نیروی عمودی تکیه گاه با جا به جایی \({0^0}\) است، در نتیجه کار نیروی عمودی تکیه گاه \({W_N}\) مثبت می باشد.
مانند حرکت آسانسور یا حرکت بالون
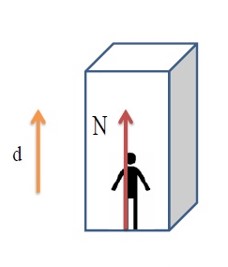
\(\begin{array}{l}{W_N} = {F_N} \times d \times \cos \alpha \\{W_N} = {F_N} \times d \times \cos {0^0}\\ \to \cos {0^0} = 1 \to {W_N} = {F_N}d\end{array}\)
3) کار نیروی عمودی تکیه گاه
ج) در جا به جایی قائم (به سمت پایین)
چون زاویه نیروی عمودی تکیه گاه با جا به جایی \({180^0}\) است، در نتیجه کار نیروی عمودی تکیه گاه \({W_N}\) منفی می باشد.
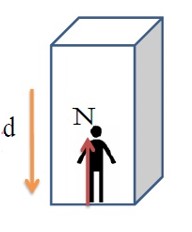
\(\begin{array}{l}{W_N} = {F_N} \times d \times \cos \alpha \\{W_N} = {F_N} \times d \times \cos {180^0}\\ \to \cos {180^0} = - 1 \to {W_N} = - {F_N}d\end{array}\)
4) کار نیروی اصطکاک
الف) ایستایی
در این حالت جسم ساکن می باشد، بنابراین کار نیروی اصطکاک ایستایی صفر است.
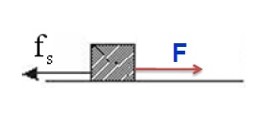
\(\begin{array}{l}{W_{{f_s}}} = {f_s} \times d \times \cos \alpha \\{W_{{f_s}}} = {f_s} \times d \times \cos {180^0}\\ \to d = 0 \to {W_{{f_s}}} = 0j\end{array}\)
هنگامی که یک جسم روی جسم دیگر قرار گیرد نیروی اصطکاک ایستایی روی جسم بالایی می تواند کار مثبت انجام دهد.
4) کار نیروی اصطکاک
ب) جنبشی
چون نیروی اصطکاک جنبشی همیشه در خلاف جهت حرکت است، پس زاویه \(\alpha \) برای هر سطحی برابر \({180^0}\) می باشد؛ در نتیجه کار آن همیشه منفی است.
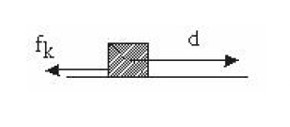
\(\begin{array}{l}{W_f}_{_k} = {f_k} \times d \times \cos \alpha \\{W_f}_{_k} = {f_k} \times d \times \cos {180^0}\\ \to \cos {180^0} = - 1 \to {W_f}_{_k} = - {f_k}d\end{array}\)
هنگامی که یک جسم روی جسم دیگر قرار گیرد نیروی اصطکاک جنبشی روی جسم بالایی می تواند کار مثبت انجام دهد.
رابطه کار و انرژی جنبشی
فصل 3 : کار، انرژی و توان
رابطه کار و انرژی جنبشی
مجموع کار های نیرو های وارد جسم در یک جا به جایی معین، برابر تغییر انرژی جنبشی جسم در همان جا به جایی است.
\({W_T} = {K_2} - {K_1} \to {W_F} + {W_N} + {W_{mg}} + {W_f}_{_K} = {K_2} - {K_1}\)
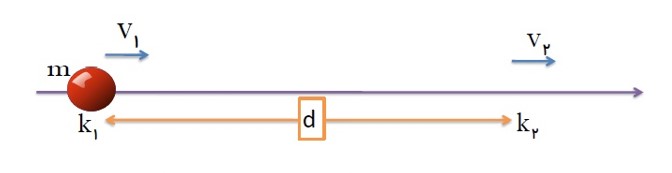
قضیه ی کار – انرژی جنبشی نه تنها برای حرکت یک جسم روی مسیر مستقیم معتبر است، بلکه اگر جسم روی مسیر خمیده نیز حرکت کند می توان از آن استفاده کرد.
1 هنگامی که \({W_T}\rangle 0\) است، انرژی جنبشی آن افزایش می یابد \({K_2}\rangle {K_1}\)، بنابراین تندی جسم در پایان جا به جایی بیشتر از تندی آن در ابتدای حرکت است. \({V_2}\rangle {V_1}\)
2 هنگامی که \({W_T}\langle 0\) است، انرژی جنبشی آن کاهش می یابد \({K_2}\langle {K_1}\)، بنابراین تندی جسم در انتهای جا به جایی کمتر از تندی آن در آغاز حرکت است. \({V_2}\langle {V_1}\)
3 هنگامی که \({W_T} = 0\) است، انرژی جنبشی جسم در آغاز و پایان جا به جایی یکسان است \({K_2} = {K_1}\)، بنابراین تندی جسم در این دو نقطه یکسان است. \({V_2} = {V_1}\)
رابطه کار و انرژی پتانسیل
فصل 3 : کار، انرژی و توان
رابطه کار و انرژی پتانسیل
انرژی پتانسیل، به معنی انرژی ذخیره شده در سامانه (دستگاه یا سیستم) است.
وقتی دو یا چند جسم به یکدیگر نیرو وارد می کنند به دلیل موقعیت مکانی شان در سامانه، انرژی پتانسیل دارند.
وقتی جسم از ارتفاع \({h_1}\) به ارتفاع \({h_2}\) از سطح زمین می رسد، کار نیروی وزن در این جا به جایی برابر است با:
\(\begin{array}{l}{W_W} = mg \times d \times \cos {0^0}\\ \to \cos {0^0} = 1\\{W_W} = mg\left( {{h_1} - {h_2}} \right)\\{W_W} = - \left( {mg{h_2} - mg{h_1}} \right)\\{W_W} = - \left( {{U_2} - {U_1}} \right)\\{W_W} = - \Delta U\end{array}\)
در این فرمول \({W_W}\) به معنی کار نیروی وزن است.
1 کار نیروی وزن برابر با منفی تغییر انرژی پتانسیل گرانشی است.
\({W_W} = - \Delta U\)
2 چون کار نیروی وزن در مسیر های افقی صفر است، پس به شکل مسیر حرکت بستگی ندارد.
3 کار نیروی وزن فقط به اندازه جا به جایی جسم در راستای قائم بستگی دارد.
4 کار نیروی وزن در یک مسیر بسته صفر است.
انرژی پتانسیل گرانش بین دو نقطه:
جسمی را از ارتفاع \({y_1}\) پایین سطح زمین تا ارتفاع \({y_2}\) بالا می بریم، کار انجام شده در این جا به جایی به صورت انرژی پتانسیل گرانشی ظاهر می شود.
\(\Delta U = mg\left( {{y_2} - {y_1}} \right) = mg\Delta h\)
تغییر انرژی پتانسیل گرانش بین دو نقطه بستگی به مسیر افقی ندارد.
انرژی پتانسیل کشسانی فنر:
وقتی جسمی را به سوی فنری پرتاب می کنیم، پس از برخورد، فنر فشرده می شود و انرژی پتانسیل آن افزایش می یابد. در مدت تماس جسم با فنر، فنر نیرویی در خلاف جهت جا به جایی به جسم وارد می کند.
رابطه کار و انرژی پتانسیل کشسانی فنر:
در مورد تغییر انرژی پتانسیل کشسانی سامانه جسم – فنر نیز مشابه تغییر انرژی پتانسیل گرانشی می توانیم بگوییم:
\({W_f}_{_e} = - \Delta U\)
- آزمون آنلاین تمامی دروس پایه ریاضی
- گام به گام تمامی دروس پایه ریاضی
- ویدئو های آموزشی تمامی دروس پایه ریاضی
- گنجینه ای از جزوات و نمونه سوالات تمامی دروس پایه ریاضی
- فلش کارت های آماده دروس پایه ریاضی
- گنجینه ای جامع از انشاء های آماده پایه ریاضی
- آموزش جامع آرایه های ادبی، دستور زبان، قواعد زبان انگلیسی و ... ویژه پایه ریاضی
اصل پایستگی انرژی مکانیکی
فصل 3 : کار، انرژی و توان
اصل پایستگی انرژی مکانیکی
انرژی مکانیکی جسم:
مجموع انرژی های پتانسیل و جنبشی هر جسم را انرژی مکانیکی آن جسم می نامند.
\(E = K + U\)
انرژی پتانسیل جسم ممکن است به صورت انرژی پتانسیل گرانشی، انرژی پتانسیل کشسانی یا هر دوی آن ها باشد.
اثبات اصل پایستگی انرژی مکانیکی
با چشم پوشی از نیروی مقاومت هوا، انرژی مکانیکی جسم ثابت باقی می ماند.
\(\begin{array}{l}{W_T} = {K_2} - {K_1} \to {W_F} + {W_N} + {W_{mg}} + {W_f}_{_k} = {K_2} - {K_1}\\{W_F},{W_N},{W_f}_{_k} = 0\\{W_{mg}} = - \Delta U\\ \to \Delta K = - \Delta U\\{K_2} - {K_1} = - {U_2} + {U_1} \to {K_2} + {U_2} = {K_1} + {U_1} \to {E_2} = {E_1}\end{array}\)
1 این رابطه نشان می دهد مجموع انرژی پتانسیل و جنبشی جسم در نقطه های مختلف مسیر حرکت با هم برابر است.
2 پایستگی انرژی مکانیکی، به جرم جسم، زاویه پرتاب، شکل مسیر حرکت و نحوه حرکت جسم بستگی ندارد.
مثال
جسمی به جرم \(1Kg\) از ارتفاع \(5m\) سطح زمین با سرعت \(3\frac{m}{s}\) عبور می کند. انرژی مکانیکی جسم را در این نقطه محاسبه کنید. \(g = 10\frac{N}{{Kg}}\)
\(\begin{array}{l}m = 1Kg\\h = 5m\\V = 3\frac{m}{s}\\E = ?\\E = U + K\\ \to E = mgh + \frac{1}{2}m{V^2} \to E = 1 \times 10 \times 5 + \frac{1}{2} \times 1 \times {\left( 3 \right)^2} = 54/5J\end{array}\)
قانون پایستگی انرژی
فصل 3 : کار، انرژی و توان
قانون پایستگی انرژی
انرژی درونی
مجموع انرژی ذرات تشکیل دهنده آن جسم را می گویند.
معمولا با گرم تر شدن یک جسم، انرژی درونی آن بالا می رود.
انرژی درونی یک جسم به عوامل زیر بستگی دارد:
- به تعداد ذرات جسم
- به انرژی هر ذره بستگی دارد.
به طوری که هرچه تعداد ذرات سازنده یک جسم و انرژی هر ذره آن بیشتر باشد، انرژی درونی آن نیز بیشتر است.
قانون پایستگی انرژی:
در یک سامانه منزوی، مجموع کل انرژی ها پایسته می ماند. انرژی را نمی توان خلق یا نابود کرد و تنها می توان آن را از یک شکل به شکل دیگر تبدیل کرد.
توان
فصل 3 : کار، انرژی و توان
توان
توان متوسط:
کار انجام شده، در واحد زمان (\(1s\)) \(P = \frac{W}{{\Delta t}}\)
یکای توان \(\frac{J}{s}\) است که آن را وات می نامیم: \(1\frac{J}{s} = 1W\)
1 یکای رایج و متداول برای توان خودرو اسب بخار است.
2 هر اسب بخار برابر با 746 وات است.
3 در فیزیک، سریع انجام گرفتن کار بر حسب توان توصیف می شود.
4 بنابراین توان یک ماشین معیاری برای توصیف کند تر یا سریع تر انجام گرفتن یک کار است.
کار موتور (بالابر، جرثقیل، پمپ و ...):
\({W_m} = mgh\)
در این فرمول m به معنای موتور است.
حالات توان دستگاه: یا توان خروجی مفید دستگاه:
برای جا به جایی جسم در راستای قائم:
\(\begin{array}{l}W = mgh\\P = \frac{W}{{\Delta t}}\\ \to P = \frac{{mgh}}{{\Delta t}}\end{array}\)
برای جا به جایی جسم در راستای افقی:
\(\begin{array}{l}{W_T} = {K_2} - {K_1}\\P = \frac{W}{{\Delta t}}\\ \to P = \frac{{{K_2} - {K_1}}}{{\Delta t}}\end{array}\)
هر وسیله ای مانند اتوموبیل، آسانسور، تلمبه و ... که کاری را انجام می دهد، انرژی مصرف می کند.
انرژی ورودی:
آسانسور، پمپ: انرژی الکترکی
اتوموبیل: انرژی سوختی (شیمیایی)
بازده: Ra
نسبت کار مفید گرفته شده به کار داده شده (انرژی ورودی) است.
بازده بر حسب درصد:
\(Ra = \frac{{{W_{out}}}}{{{W_{in}}}} \times 100\% \)
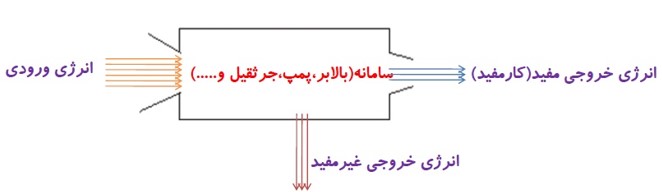
بازده بالابری \(Ra = 60\% \) یعنی چه؟
یعنی دستگاه بالابر از \(100j\) انرژی الکتریکی دریافتی فقط \(60j\) آن را به کار (باعث بالا بردن اجسام) تبدیل می کند.
فرمول دیگر بازده:
نسبت توان خروجی مفید به توان ورودی دستگاه است.
\(Ra = \frac{{{P_{out}}}}{{{P_{in}}}} \times 100\% \)

بازده وسایل بالابر (آسانسور، پمپ، جرثقیل و ...):
\(Ra = \frac{{\frac{{mgh}}{{\Delta t}}}}{{{P_1}}} \times 100\% \)
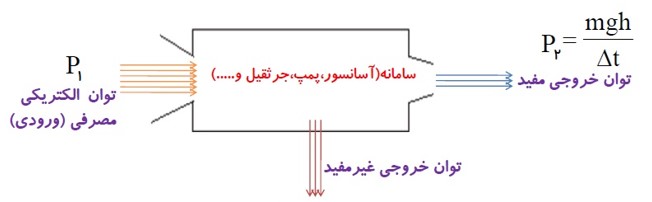
بازده توربین های تولید برق (آبشار ها):
\(Ra = \frac{{{P_2}}}{{\frac{{mgh}}{{\Delta t}}}} \times 100\% \)
- آزمون آنلاین تمامی دروس پایه ریاضی
- گام به گام تمامی دروس پایه ریاضی
- ویدئو های آموزشی تمامی دروس پایه ریاضی
- گنجینه ای از جزوات و نمونه سوالات تمامی دروس پایه ریاضی
- فلش کارت های آماده دروس پایه ریاضی
- گنجینه ای جامع از انشاء های آماده پایه ریاضی
- آموزش جامع آرایه های ادبی، دستور زبان، قواعد زبان انگلیسی و ... ویژه پایه ریاضی
انواع دماسنج
فصل 4 : دما و گرما
انواع دماسنج
دما چیست؟
دما کمیتی است که میزان گرمی و سردی اجسام را مشخص می کند.
ساده ترین و رایج ترین نوع دماسنج، دماسنج های جیوه ای و الکلی است.
کمیت دماسنجی:
هر مشخصه قابل اندازه گیری که با گرمی و سردی جسم تغییر می کند. کمیت دماسنجی می گویند.
چند مثال از کمیت دماسنجی
ارتفاع مایع، فشار، حجم، رنگ، جریان الکتریکی و ... .
تعبیر مولکولی دما و انرژی درونی
انرژی درونی:
به مجموع انرژی های جنبشی و پتانسیل مولکولی تمام ذره های جسم، انرژی درونی گفته می شود.
دمای هر جسم:
متناسب با انرژی جنبشی متوسط مولکول های سازنده ی آن است.
انرژی درونی به جرم و دمای جسم وابسته است.
وقتی دمای جسمی کاهش یا افزایش می یباد، انرژی درونی آن کاهش یا افزایش یافته است.
در تغییر حالت های جسم (ذوب، تبخیر) انرژی درونی جسم تغییر می کند، اما دمای جسم تغییر نمی کند.
دماسنج های معمولی بر اساس انبساط و انقباض مایع درون دماسنج (جیوه و الکل) است.
نقاط ثابت دماسنجی در مقیاس سلسیوس:
دمای یخ خالص در حال ذوب و دمای جوش آب خالص، هر دو در فشار یک اتمسفر به عنوان نقاط ثابت دماسنجی در مقیاس سلسیوس انتخاب شده اند و به آن ها به ترتیب دمای صفر و صد نسبت داده شده است. درجه ی سلسیوس را با نماد (\({}^0C\) ) نشان می دهیم.
در SI یکای دما برحسب کلوین است که با نماد K نمایش داده می شود، دما برحسب کلوین را با نماد (T) و برحسب درجه سلسیوس را با نماد (\(\theta \)) (تتا) نشان می دهیم.
رابطه بین دما در مقیاس های کلوین و سلسیوس
\({T_{\left( k \right)}} = {\theta _{\left( {{}^0C} \right)}} + 273\)
صفر کلوین معادل \( - 273{}^0C\) است.
صفر مطلق
پایین ترین دمای ممکن که برابر \( - 273{}^0C\) است را صفر مطلق می گویند.
مقایسه سه یکای دماسنجی: سلسیوس، فارنهایت و کلوین
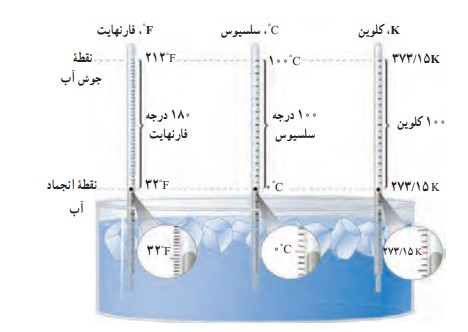
مقایسه یکاهای فارنهایت، سلسیوس و کلوین
رابطه بین یکای سلسیوس و یکای فارنهایت
\({F_{\left( F \right)}} = 1/8{\theta _{\left( {{}^0C} \right)}} + 32\)
مثال
\(27{}^0C\) چند کلوین و چند درجه فارنهایت است؟
\(\begin{array}{l}\theta = {27_{\left( {{}^0C} \right)}}\\T = ?\\F = ?\\{T_{\left( K \right)}} = {\theta _{\left( {{}^0C} \right)}} + 273 \to T = 27 + 273 \to T = 300K\\{F_{\left( F \right)}} = 1/8{\theta _{\left( {{}^0C} \right)}} + 32 \to F = 1/8 \times 27 + 32 \to F = 80/6F\end{array}\)
ویژگی های مقیاس کلوین:
1) صفر کلوین کمترین دمای ممکن است یعنی در مقیاس کلوین دمای منفی ندارد.
2) تغییر دما در مقیاس سلسیوس با تغیر دما در مقیاس کلوین برابر است:
\(\Delta {T_K} = \Delta {\theta _{{}^0C}}\)
3) در دمای صفر کلوین انرژی جنبشی و انرژی درونی ذرات به کمترین مقدار خود می رسد. اما برابر صفر نیست.
1 اگر دما یک درجه سلسیوس تغییر کند. در درجه بندی فارنهایت \(1/8{}^0F\) تغییر خواهد کرد.
2 در دمای \(F \approx - 12/3{}^0F\) یکای فارنهایت نصف عدد دمای سلسیوس است.
مدرج ساختن دماسنج با یک مقیاس دلخواه:
اگر دماسنجی وجود داشته باشد که نقطه ذوب یخ را با a و نقطه جوش آب را با b نشان دهد. برای مدرج کردن آن بایستی فاصله بین این دو مقدار را به b-a قسمت مساوی تقسیم کنیم. حال می خواهیم بدانیم این دماسنج دمایی را که دماسنج سلسیوس برابر \(\theta \) نشان می دهد، چقدر (X) نشان خواهد داد؟
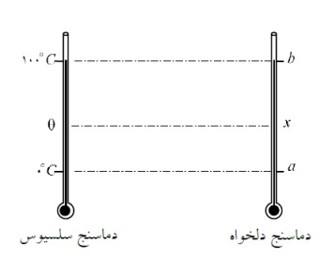
\(\frac{{x - a}}{{b - a}} = \frac{{{\theta _{\left( {{}^0C} \right)}} - 0}}{{100 - 0}}\)
مثال
دماسنجی که دمای نقطه ی ذوب یخ را 20- و دمای نقطه ی جوش آب را 105 درجه نشان می دهد، دمای یک محیط را 5 درجه نشان می دهد. دماسنجی که برحسب درجه ی سلسیوس درجه بندی شده است. دمای این محیط را چند درجه نشان می دهد؟
\(\frac{{x - {x_1}}}{{{x_2} - {x_1}}} = \frac{{\theta - {\theta _1}}}{{{\theta _2} - {\theta _1}}} \to \frac{{5 + 20}}{{105 + 20}} = \frac{{\theta - 0}}{{100 - 0}} \to \frac{{25}}{{125}} = \frac{\theta }{{100}} \to \theta = 20{}^0c\)
دماسنج های معیار
- دماسنج گازی: اساس کار این دماسنج ها بر مبنای قانون گاز های کامل است.
- دما سنج های مقاومت پلاتینی: اساس کار این دماسنج ها بر مبنای تغییر مقاومت باد ما است.
- تف سنج (پیرومتر): اساس کار این دماسنج ها بر مبنای تابش گرمایی است.
علت نام گذاری دماسنج های معیار:
- کاربرد این دماسنج ها در صنعت و آزمایشگاه زیاد است.
- دقت اندازه گیری این دماسنج ها زیاد است، یعنی در محدوده ی یک هزارم درجه و کمتر از آن دما را می توانند اندازه بگیرند.
ترموکوپل:
وسیله ای برای اندازه گیری دماست که بر اساس تغییر ولتاژ ناشی از اختلاف دمای دو سر دار تشکیل دهنده ی آن کار می کند.
ساختمان ترموکوپل
دو سیم فلزی غیر همجنس مانند مس و کنستانتان از یک و در ظرف مخلوط آب و یخ با دمای ثابت صفر درجه نگه داشته شده اند و از طرف دیگر به جسمی با دمای مجهول متصل اند. و به وسیله دو سیم مسی به ولت سنج بسته می شوند. با افزایش دمای مجهول ولتاژ دو سر سیم های غیر هم جنس افزایش می یابد. با اندازه گیری ولتاژ مربوط به هر دما می توان دمای مجهول را مشخص کرد.
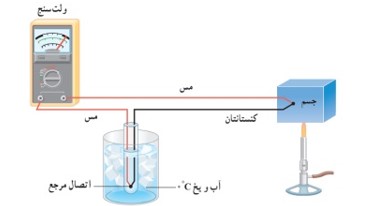
برتری های داسنج ترموکوپل نسبت به دماسنج های دیگر:
- دقت اندازه گیری آن زیاد است. (اما دقت آن کمتر از دما سنج های معیار است.)
- تغیرات ناگهانی دما را خیلی سریع و پیوسته نشان می دهد.
- گستره ی دماسنج ترموکوپل به جنس سیم ها بستگی دارد، مثلا برای جنس سیم از آلیاژ خاص گستره ی دماسنجی \( - 270{}^0C\) تا \(1372{}^0C\) است.
- در بسیاری از وسایل صنعتی، گرمایشی و سرمایشی یافت می شود.
انبساط طولی، سطحی و حجمی
فصل 4 : دما و گرما
انبساط طولی، سطحی و حجمی
انبساط جامد ها:
با افزایش دما، دامنه ی نوسان مولکول ها و اتم های ماده و ئر نتیجه فاصله متوسط آنها از یکدیگر افزایش یافته و جسم جامد منبسط می شود.
انواع انبساط ها
اکثر اجسام در اثر افزایش دما، منبسط می شود. این انبساط به صورت های زیر است:
1) انبساط جامد ها
الف) طولی
ب) سطحی
ج) حجمی
2) انبساط مایع ها
3) انبساط گاز ها (قانون گاز ها)
1) انبساط جامد ها
الف) طولی
افزایش دما باعث افزایش طول جامد ها می شود. انبساط طولی اجسام مختلف به دلیل تفاوت جنسشان با یکدیگر متفاوت است.
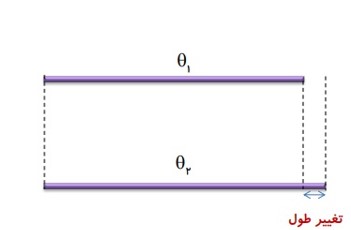
تغییر طول یک میله ی جامد، به عوامل زیر بستگی دارد:
- به طول اولیه \({L_1}\)
- تغیرات دما \(\Delta \theta \)
- جنس میله (ضریب انبساط طولی) \(\alpha \)
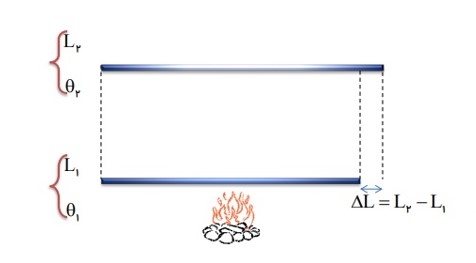
ضریب انبساط طولی (آلفا \(\alpha \))
افزایش طول واحد طول (\(1m\) ) یک جسم جامد وقتی که دمای آن یک کلوین (یا سانتی گراد) بالا رود.
\(\alpha = \frac{{\Delta L}}{{{L_1}\Delta \theta }} \to \alpha = \frac{{\Delta L}}{{1m \times 1{}^0C}}\)
فرمول انبساط طولی
\(\begin{array}{l}\Delta L = \alpha {L_1}\Delta \theta \to {L_2} - {L_1} = \alpha {L_1}\Delta \theta \to {L_2} = {L_1} + \alpha {L_1}\Delta \theta \\1)\Delta L = \alpha {L_1}\Delta \theta \\2){L_2} = {L_1}\left( {1 + \alpha \Delta \theta } \right)\end{array}\)
جنبه های مختلف انبساط گرمایی در زندگی
جنبه های مفید: اساس کار دماسنج ها و ترموستات ها، انبساط گرمایی است.
جنبه های دردسر ساز انبساط طولی:
انبساط طولی در ساختن پل ها، ساختمان ها، خط راه آهن، خطوط نیرو و سوخت مشکل ایجاد می کند.
مثال
ارتفاع برج ایفل در یک روز از سال \(301m\) است اگر اختلاف دما در آن روز \(22{}^0C\) باشد. افزایش طول این برج چقدر است؟ (\(\alpha = 10/5 \times {10^{ - 6}}{\textstyle{1 \over {{}^0C}}}\) )
\(\begin{array}{l}{L_1} = 301m\\\Delta \theta = 22{}^0C\\\alpha = 10/5 \times {10^{ - 6}}{\textstyle{1 \over {{}^0C}}}\\\Delta L = ?\\\Delta L = \alpha {L_1}\Delta \theta \\\Delta L = 10/5 \times {10^{ - 6}} \times 301 \times 22 \to \Delta L \approx 0/07m = 7cm\end{array}\)
دماپا (ترموستات):
وسیله ای برای تنظیم دماست که از دو فلز غیر هم جنس با میزان انبساط متفاوت که به یک دیگر پرچ یا لحیم شده اند، ساخته شده است.
در اتوی برقی
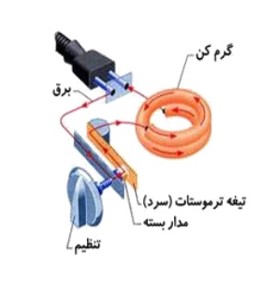
1 اگر دماپا (نوار دو فلز) در یک مدار الکتریکی قرار دهیم با بر قراری جریان نوار دو فلز گرم می شود و نوار خم شده و اتصال قطع می شود و اگر دماپا سرد شود دوباره طول دو فلز یک اندازه می شود و نقاط اتصال وصل می شوند و دستگاه روشن می شود.
2 هرچه آلفا (ضریب انبساط طولی) بزرگتر باشد افزایش طول میله به علت افزایش دما بیشتر است.
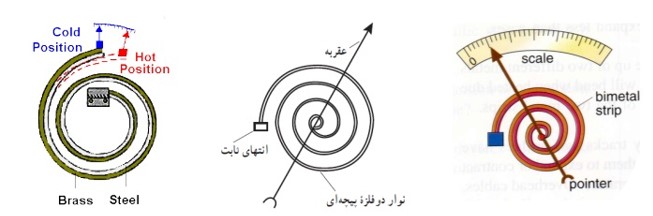
دماسنج نواری دو فلز (بی متال)
این نوع دماسنج مثل ترموستات از دو تیغه ی فلزی با ضریب انبساط متفاوت که سر تا سر به هم جوش داده شده اند، می سازند.
در دماسنج بی متال تیغه های فلزی به شکل یک نوار حلزونی است. در ن جا هم تیغه ی فلزی که ضریب انبساط بیشتری دارد کمان خارجی را تشکیل می دهد به همین دلیل با افزایش دما، نوار بی متال حلزونی، خمیده شده و عقربه به سمت راست می چرخد.
1) انبساط جامد ها
ب) انبساط سطحی:
افزایش دما باعث افزایش سطح جامد ها نیز می شود.
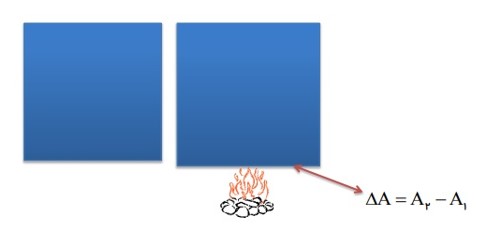
تغییر مساحت یک ورقه فلزی به عوامل زیر بستگی دارد:
- به مساحت اولیه \({A_1}\)
- تغییرات دما \(\Delta \theta \)
- ضریب انبساط سطحی ورقه \(2\alpha \)
فرمول ضریب انبساط سطحی
\(\begin{array}{l}1)\Delta A = 2\alpha {A_1}\Delta \theta \\2){A_2} = {A_1}\left( {1 + 2\alpha \Delta \theta } \right)\end{array}\)
ضریب انبساط سطحی: (\(2\alpha \) )
افزایش مساحت واحد سطح (\(1{m^2}\) ) یک جسم جامد وقتی که دمای آن یک کلوین (یا سانتی گراد) بالا رود.
\(2\alpha = \frac{{\Delta A}}{{{A_1}\Delta \theta }} \to 2\alpha = \frac{{\Delta A}}{{1{m^2} \times 1{}^0C}}\)
مثال
دمای یک صفحه فلزی \( - 10{}^0C\) است. دمای آن را به چند درجه سلسیوس برسانیم تا مساحتش به اندازه ی \(0/003\) سطح اولیه کاهش می یابد؟ (\(\alpha = 3 \times {10^{ - 5}}{\textstyle{1 \over {{}^0C}}}\) )
\(\begin{array}{l}{\theta _1} = - 10{}^0C\\{\theta _2} = ?\\\Delta A = - 0/003{A_1}\\\alpha = 3 \times {10^{ - 5}}{\textstyle{1 \over {{}^0C}}}\\\Delta A = 2\alpha {A_1}\Delta \theta \\ \to - 0/003{A_1} = 2 \times 3 \times {10^{ - 5}} \times {A_1} \times \Delta \theta \\ \to - 3 \times {10^{ - 3}} = 6 \times {10^{ - 5}} \times \Delta \theta \to \Delta \theta = \frac{{ - 3 \times {{10}^{ - 3}}}}{{6 \times {{10}^{ - 5}}}} = - 50\\{\theta _2} - {\theta _1} = - 50 \to {\theta _2} + 10 = - 50 \to {\theta _2} = - 50 - 10 = - 60{}^0C\end{array}\)
1) انبساط جامد ها
ج) انبساط حجمی
افزایش دما باعث افزایش حجم جامد ها نیز می شود.
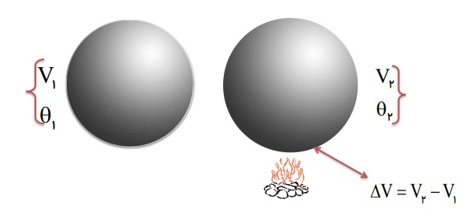
تغییر حجم یک جسم جامد به عوامل زیر بستگی دارد:
1) به حجم اولیه ی \({V_1}\)
2) تغیرات دما \(\Delta \theta \)
3) ضریب انبساط حجمی جسم \(3\alpha \)
فرمول انبساط حجمی جامدات
\(\begin{array}{l}1)\Delta V = 3\alpha {V_1}\Delta \theta \\2){V_2} = {V_1}\left( {1 + 3\alpha \Delta \theta } \right)\end{array}\)
ضریب انبساط حجمی: (\(3\alpha \) )
افزایش حجم واحد حجم (\(1{m^3}\) ) یک ماده وقتی که دمای آن یک کلوین (یا سانتی گراد) بالا رود.
\(3\alpha = \frac{{\Delta V}}{{{V_1}\Delta \theta }} \to 3\alpha = \frac{{\Delta V}}{{1{m^3} \times 1{}^0C}}\)
محاسبه درصد تغییرات طول، سطح و جسم:
درصد تغیرات طول
\(\frac{{\Delta L}}{{{L_1}}} \times 100\% = \left( {\alpha \times \Delta \theta } \right) \times 100\% \)
درصد تغیرات سطح
\(\frac{{\Delta A}}{{{A_1}}} \times 100\% = \left( {2\alpha \times \Delta \theta } \right) \times 100\% \)
درصد تغیرات حجم
\(\frac{{\Delta V}}{{{V_1}}} \times 100\% = \left( {3\alpha \times \Delta \theta } \right) \times 100\% \)
درصد تغییرات سطح دو برابر درصد تغییرات طولش و درصد تغییرات حجم سه برابر درصد تغییرات طولش است.
2) انبساط حجمی مایع ها
با افزایش دمای مایع، حرکت کاتوره ای اتم ها و مولکول ها افزایش می یابد. در نتیجه اتم ها و مولکول ها از هم دور شده و حجم مایع بیشتر می شود.
انبساط و انقباض مایعات تنها از نوع انبساط و انقباض حجمی است.
انبساط واقعی مایع = انبساط ظاهری مایع + انبساط ظرف
1 همیشه انبساط واقعی مایع از انبساط ظاهری مایع بیشتر است.
2 ضریب انبساط حجمی مایعات بسیار بزرگتر از ضریب انبساط حجمی جامدات است، بنابراین انبساط مایع بیشتر از انبساط ظرف است.
انبساط واقعی مایع
اگر حجم اولیه ی مایع را \({V_1}\) بنامیم تغییر حجم واقعی مایع در اثر تغییر دمای \(\Delta \theta \) از رابطه ی رو به رو محاسبه می شود:
\(\begin{array}{l}1)\Delta V = \beta {V_1}\Delta \theta \\2){V_2} = {V_1}\left( {1 + \beta \Delta \theta } \right)\end{array}\)
در فرمول دوم
(\({V_2}\)) حجم نهایی مایع
(\({V_1}\)) حجم اولیه مایع
(\(\beta \)) ضریب انبساط حجمی مایع
(\(\Delta \theta \) ) تغیرات دما است.
انبساط ظاهری مایع
تفاضل انبساط واقعی مایع از انبساط ظرف (انبساط ظاهری مایع) بدست می آید.
\(\begin{array}{l}1)\Delta V = \beta '{V_1}\Delta \theta \\2)\beta ' = \beta - 3\alpha \end{array}\)
در این فرمول
(\(\beta '\) ) ضریب انبساط ظاهری مایع
(\(\beta \)) ضریب انبساط واقعی مایع
(\(3\alpha \) ) ضریب انبساط حجمی ظرف
با افزایش دما، جرم جسم ثابت و حجم آن افزایش می یابد. بنابراین طبق رابطه \(\rho = \frac{m}{v}\) چگالی جسم کاهش می یابد.
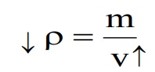
رابطه چگالی اجسام با دما:
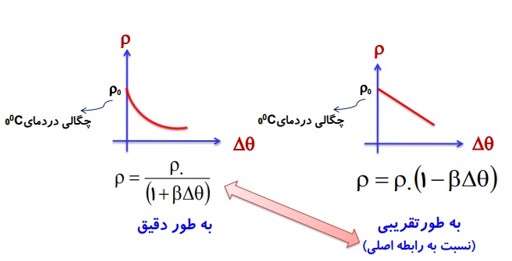
\({\rho _2} = {\rho _1}\left( {1 - \beta \Delta \theta } \right)\)
نمودار تغییرات چگالی بر حسب دما (برای تمام مواد غیر از آب)
مثال
اگر دمای الکل را \(50{}^0C\) افزایش دهیم چگالی آن چقدر می شود؟
(\({\beta _{Alc}} = 1/1 \times {10^{ - 3}}{\textstyle{1 \over {{}^0C}}}\) و \({\rho _{Alc}} = 800\frac{{Kg}}{{{m^3}}}\) )
\(\begin{array}{l}\Delta \theta = 50{}^0C\\{\rho _2} = ?\\{\rho _1} = 800\frac{{Kg}}{{{m^3}}}\\\beta = 1/1 \times {10^{ - 3}}{\textstyle{1 \over {{}^0C}}}\\{\rho _2} = {\rho _1}\left( {1 - \beta \Delta \theta } \right)\\{\rho _2} = 800 \times \left( {1 - 0/0011 \times 50} \right) = 800 \times \left( {1 - 0/055} \right)\\{\rho _2} = 756\frac{{Kg}}{{{m^3}}}\end{array}\)
درصد تغیرات چگالی:
\(\frac{{\Delta \rho }}{{{\rho _1}}} \times 100\% \)
انبساط غیر عادی آب
حجم بیشتر مایع ها با کاهش دما، کاهش می یابد ولی آب، رفتاری متفاوت دارد.
وقتی مقدار مشخصی از آب را سرد می کنیم تا دمای آن به \(4{}^0C\) برسد، حجم آن طبق روال عادی کاهش می یابد.
آب از دمای 4 درجه تا صفر درجه افزایش حجم پیدا می کند و در دمای \(4{}^0C\) حجم آن کمترین مقدار را دارد.
تغیرات چگالی با دما
با افزایش دما جرم جسم ثابت می ماند.
با توجه به اینکه افزایش دما، حجم جسم را افزایش می دهد، می توان گفت افزایش دما چگالی را کاهش می دهد زیرا؛ چگالی با حجم رابطه وارون دارند.
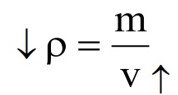
تغیرات چگالی آب با دما
حجم آب در \(4{}^0C\) کمترین مقدار خود را دارد، در نتیجه چگالی آب در \(4{}^0C\) نیز به بیشترین مقدار خود می رسد.
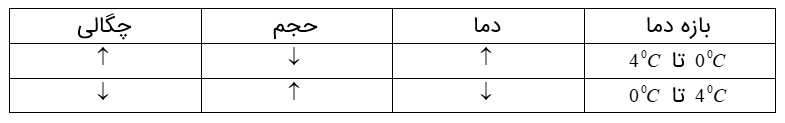
دلیل رفتار غیر عادی آب در محدوده دمایی \(4{}^0C\) تا \(4{}^0C\) :
آرایش مولکولی آب در بلور یخ به گونه ای است که در بعضی از نقاط مولکول به هم نزدیک و در بعضی نقاط از هم دور اند و بین آنها فضای خالی وجود دارد. در \(4{}^0C\) تقریبا تمام ساختار مولکولی بلور یخ از بین می رود و فضای خالی پر و آرایش مولکول های یکنواخت می شود. که این رفتار منجر به کاهش حجم و افزایش چگالی می شود. در محدوده \(0{}^0C\) تا \(4{}^0C\) بقایای ساختار مولکولی یخ هنوزوجود دارد و این باعث می شود آب، رفتاری غیر عادی داشته باشد.
گرما و دمای تعادل
فصل 4 : دما و گرما
گرما و دمای تعادل
گرما Q
به انرژی انتقال یافته بر اثر اختلاف دمای دو جسم، گرما گفته می شود.
عبارت گرمایی که جسم دارد، نادرست است. گرما مربوط به انرژی در حال گذار (انرژی انتقال یافته) است.
گرما از جنس انرژی است. بنابراین یکای آن در SI ژول است.
علت انتقال گرما، اختلاف دما است.
دمای جسم A از دمای B بیشتر است؛ پس گرما از A به B منتقل می شود.
هنگام کاهش دمای جسم گرم، میانگین انرژی جنبشی و پتانسیل ذرات آن کاهش و باعث بالا بردن، میانگین انرژی جنبشی و پتانسیل ذرات جسم سرد و در نتیجه افزایش دمای آن می شود تا آنکه دو جسم به تعادل گرمایی برسند.
ظرفیت گرمایی
با نماد C (بزرگ) نمایش داده می شود.
مقدار گرمایی است که دمای جسم را \(1{}^0C\) یا \(1K\) افزایش می دهد.
یکای ظرفیت گرمایی \(\frac{J}{K}\) است.
ظرفیت گرمایی اجسام به جنس جسم و جرم آن ها بستگی دارد.
محاسبه گرما با استفاده از ظرفیت گرمایی:
\(Q = C\Delta T\)
(\(Q\)) به معنای گرما و بر حسب ژول
(C) به معنای ظرفیت گرمای جسم و بر حسب ژول بر کلوین
(\(\Delta T\)) به معنای تغییر دما و برحسب کلوین
گرمای ویژه:
با نماد c (کوچک) نمایش داده می شود.
ظرفیت گرمایی واحد جرم اجسام را گرمای ویژه آن جسم می گویند.
\(c = \frac{C}{m}\)
یکای آن \(\frac{J}{{Kg.K}}\) است.
گرمای ویژه یک جسم به جنس ماده تشکیل دهنده آن بستگی دارد.
گرمای ویژه، مقدار گرمایی است که، باید به یک کیلوگرم از هر جسم داده شود تا دمای آن یک درجه سلسیوس (یا یک کلوین) افزایش یابد.
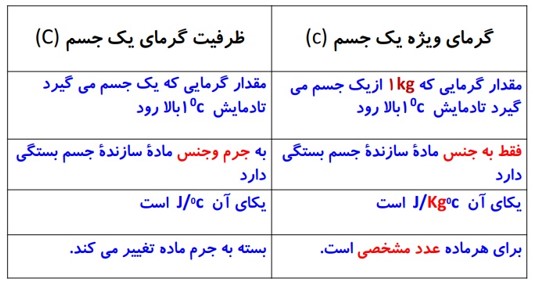
مقایسه گرمای ویژه با ظرفیت گرمایی
فرمول مقدار گرمای لازم برای تغییر دما یک جسم:
\(Q = C\Delta T = mc\Delta T\)
1 رابطه \(Q = mc\Delta \theta \) تا هنگامی برای یک جسم صادق است که، حالت جسم در اثر مبادله گرما تغییر نکند، یعنی جامد تبدیل به مایع نشود، مایع تبدیل به گاز نشود و ... .
2 گرما، کمیتی نرده ای است، اما برای آن علامت مثبت و منفی تعریف می شود.
دمای جسم بعد از مبادله ی گرما:
اگر دما افزایش یابد (\({\theta _2}\rangle {\theta _1}\) ):
بنابراین \(\Delta \theta \rangle 0\) و مقداری که برای Q به دست می آید، مثبت است و جسم گرما گرفته است.
اگر دما کاهش یابد (\({\theta _2}\langle {\theta _1}\) ):
بنابراین \(\Delta \theta \langle 0\) و مقداری که برای Q به دست می آید، منفی است و جسم گرما از دست داده است.
یک مول: n
شامل \(6/02 \times {10^{23}}\) از اجزای سازنده آن ماده (اتم یا مولکول) است.
\(\frac{{1mol}}{n} = \frac{{{N_A} = 6/02 \times {{10}^{23}}}}{N}\)
(n) تعداد مول های یک جسم
(N) تعداد مولکول
(\({{N_A}}\) ) عد آووگادرو
جرم مولی: M
جرم یک مول از هر ماده را جرم مولی می گویند.
تعداد مول ها را نیز می توان از رابطه ی زیر به دست آورد:
\(n = \frac{m}{M}\)
(n) تعداد مول های جسم (mol)
(m) جرم جسم و برحسب Kg
(M) جرم مولکولی و برحسب \(\frac{{Kg}}{{mol}}\)
گرمای ویژه مولی:
مقدار گرمایی است که دمای یک مول از ماده را \(1K\) افزایش می دهد.
گرمای ویژه مولی فلزات همگی یکسان و تقریبا برابر \(25\frac{J}{{mol.K}}\) است.
قاعده دولن و پتی
گرمای لازم برای بالا بردن دمای یک مول از هر فلز برابر است و به جنس آن ها بستگی ندارد.
\(Q = n{c_m}\Delta \theta \to Q \propto n\)
دمای تعادل: \({\theta _e}\)
هرگاه دو یا چند جسم در تماس با یکدیگر قرار گیرند بعد از مبادله انرژی، دمای تمام جسم ها یکسان می شود. به این دما (دمای تعادل) می گوییم.
قانون پایستگی انرژی در تعادل گرمایی:
همان قدر که اجسام گرم انرژی از دست می دهند، اجسام سرد انرژی می گیرند. یعنی جمع جبری این Q ها صفر است:
\(\begin{array}{l}{Q_1} + {Q_2} + ... + {Q_n} = 0\\m{}_1{c_1}\left( {{\theta _e} - {\theta _1}} \right) + {m_2}{c_2}\left( {{\theta _e} - {\theta _2}} \right) + {m_3}{c_3}\left( {{\theta _e} - {\theta _3}} \right) + ... = 0\end{array}\)
(\({{\theta _e}}\)) دمای تعادل (نهایی)
(\({{\theta _2}}\)) دمای اولیه جسم دوم
(\({{\theta _3}}\)) دمای اولیه جسم سوم
شرط تعادل گرمایی:
دمای نهایی جسم های در تماس با هم برابر شوند.
\(Cold\langle {\theta _e}\langle Warm\)
Cold به معنای سرد و Warm به معنای گرم است.
گرما سنج (کالری متر):
ظرفی فلزی و درپوش دار است که به خوبی عایق بندی گرمایی شده است.
مجموعه فلاسک و همزن و دما سنج درون آن را گرما سنج می نامند.
این ظرف در آزمایشگاه برای تعیین گرمای ویژه اجسام به کار می رود.
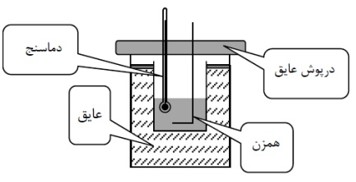
پیدا کردن ظرفیت گرمایی گرماسنج:
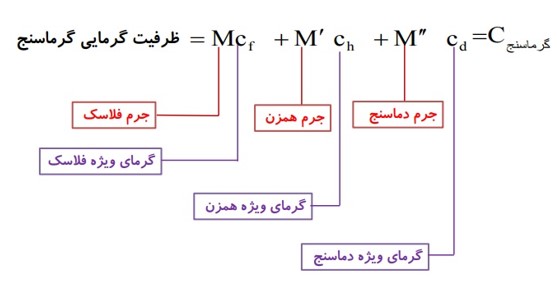
توان گرمایی: P
مقدار گرمایی را که یک گرمکن برقی در هر ثانیه تولید می کند.
\(P = \frac{Q}{{\Delta t}}\)
واحد توان برابر ژول بر ثانیه (\(\frac{J}{s}\)) یا وات است.
از رابطه ی \({Q_1} + {Q_2} + ... + {Q_n} = 0\) می توان رابطه ی زیر را به دست آورد. در این رابطه، \({{\theta _e}}\) دمای تعادل است.
\({\theta _e} = \frac{{m{}_1{c_1}{\theta _1} + {m_2}{c_2}{\theta _2} + {m_3}{c_3}{\theta _3} + ...}}{{m{}_1{c_1} + {m_2}{c_2} + {m_3}{c_3} + ...}}\)
تا زمانی می توان از رابطه دمای تعادل استفاده کرد که در اثر مبادله گرما حالت جسم تغییر نکند. (گرماسنج و ظرفیت گرمایی گرماسنج داخل مسئله نباشد.)
1 اگر تبادل گرمایی بین دو یا چند جسم با دماهای اولیه متفاوت ولی یک جنس انجام شود، دمای تعادل از رابطه زیر بدست می آید:
\(\begin{array}{l}{c_1} = {c_2} = {c_3} = ...\\{\theta _e} = \frac{{m{}_1{\theta _1} + {m_2}{\theta _2} + {m_3}{\theta _3} + ...}}{{m{}_1 + {m_2} + {m_3} + ...}}\end{array}\)
2 اگر تبادل گرمایی بین دو یا چند جسم مشابه و فقط دمای اولیه شان متفاوت است، انجام شود، دمای تعادل از رابطه زیر بدست می آید:
\(\begin{array}{l}{c_1} = {c_2} = {c_3} = ...\\{m_1} = {m_2} = {m_3} = ...\\{\theta _e} = \frac{{{\theta _1} + {\theta _2} + {\theta _3} + ...}}{{1 + 1 + 1 + ...}} = \frac{{{\theta _1} + {\theta _2} + {\theta _3} + ...}}{n}\end{array}\)
یعنی در واقع در این حالت یک عملیات میانگین گیری بین دماهای اولیه باید انجام داد.
- آزمون آنلاین تمامی دروس پایه ریاضی
- گام به گام تمامی دروس پایه ریاضی
- ویدئو های آموزشی تمامی دروس پایه ریاضی
- گنجینه ای از جزوات و نمونه سوالات تمامی دروس پایه ریاضی
- فلش کارت های آماده دروس پایه ریاضی
- گنجینه ای جامع از انشاء های آماده پایه ریاضی
- آموزش جامع آرایه های ادبی، دستور زبان، قواعد زبان انگلیسی و ... ویژه پایه ریاضی
حالات ماده و گرمای نهان ذوب
فصل 4 : دما و گرما
حالات ماده و گرمای نهان ذوب
حالت های ماده
ماده به سه حالت جامد، مایع و گاز یافت می شود.
گذار ماده از یک حالت (فاز) به حالت (فاز) دیگر را تغییر حالت (تغییر فاز) می گویند.
تغییر حالت ها معمولا با گرفتن یا از دست دادن گرما همراه اند.
به نمودار زیر توجه کنید:
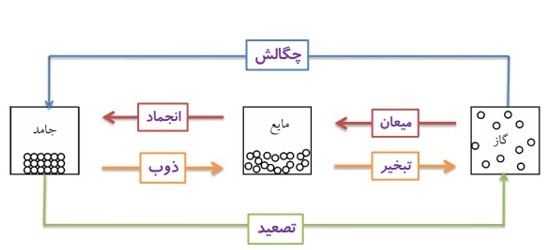
تصعید
تغییر حالت مستقیم جامد به بخار را تصعید می گویند.
مانند نفتالین و یخ خشک بدون این که به مایع تبدیل شوند مستقیما به بخار تبدیل می شوند، بنابراین می گوییم متصاعد شده اند.
وقتی لباس های تر در زمستان یخ زده اند، به هنگام طلوع خورشید بدون این که یخ ذوب شود به بخار تبدیل می شود.
چگالش
تغییر حالت مستقیم بخار به جامد را چگالش گویند.
تشکیل برف، برفک روی چمن ها و برفک درون یخچال، چگالش است.
اگر آب جوش، به هوا در دمای \( - 40{}^0C\) پاشیده شود، مستقیما به یخ تبدیل می شود.
1 ذوب، تبخیر و تصعید گرماگیر هستند.
2 انجماد، میعان و چگالش گرماده (گرمازا) هستند.
3 هر گاه دمای هوا به زیر نقطه انجماد آب برسد، بخار آب موجود در هوا مستقیما به ذره های جامد برف تبدیل می شوند. از آنجا که عمل چگالش گرمازا است، روز بارش برف، هوا کمی گرم می شود.
ذوب
هر جسم جامدی در دمای ثابتی به نام دمای ذوب (نقطه ی ذوب) که به جنس و فشار وارد بر جسم بستگی دارد، شروع به ذوب شدن می کند.
در تمام مدت ذوب، دمای جسم ثابت می ماند.
1 افزایش فشار، سبب بالا رفتن دمای ذوب می شود؛ در بعضی از جسم ها مانند یخ با افزایش فشار، نقطه ی ذوب، پایین می آید.
2 کاهش فشار، سبب بالا رفتن دمای ذوب یخ می شود.
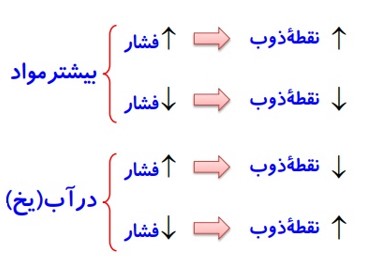
3 افزایش فشار بر روی یخ نقطه ی ذوب یخ را کاهش می دهد زیرا، افزایش فشار باعث می شود که ساختار مولکولی بلور یخ تا حدی از بین برود یعنی فضای خالی پر و آرایش مولکول ها یکنواخت و به هم نزدیک تر شده و به مولکول آب تبدیل شود.

گرمای ذوب: \({Q_F}\)
گرمایی است که هر جسم جامد در نقطه ی ذوب خود می گیرد تا به مایع در همان دما تبدیل شود.
گرمای ذوب جسم به جنس جسم و جرم آن بستگی دارد.
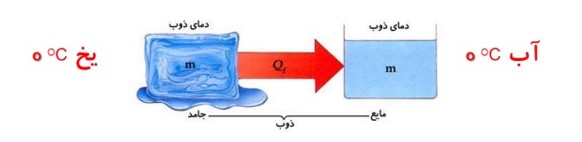
گرمای نهان ذوب: \({L_F}\)
گرمایی است که باید به یک کیلوگرم جسم جامد در دمای ذوب داده شود تا به مایع در همان دما تبدیل شود.
گرمای ذوب واحد جرم اجسام را گرمای نهان ذوب گویند. \({L_F} = \frac{{{Q_F}}}{m}\)
اگر به یخ \(0{}^0C\) گرما دهیم دمای آن افزایش نمی یابد بلکه به آب \(0{}^0C\) تبدیل می شود.
گرمای نهان ذوب اجسام فقط به جنس جسم آنها بستگی دارد.
فرمول گرمای ذوب:
\({Q_F} = m{L_F}\)
(\({Q_F}\) ) گرمای ذوب و برحسب ژول
(m) جرم جسم جامد و بر حسب کیلوگرم
(\({L_F}\) ) گرمای نهان ذوب و برحسب ژول بر کیلوگرم (\(\frac{J}{{Kg}}\) )
مثال
گرمای ذوب 3 کیلوگرم یخ صفر درجه ی سلسیوس چند ژول است؟ (\({L_F} = 334\frac{{KJ}}{{Kg}}\) )
\(\begin{array}{l}{L_F} = 334\frac{{KJ}}{{Kg}}\\m = 3Kg\\{Q_F} = ?\\{Q_F} = m{L_F} \to {Q_F} = 3 \times 334000 = 1002000J = 1002KJ\end{array}\)
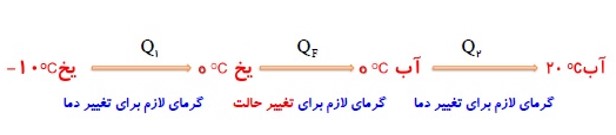
هر چه \({L_F}\) بزرگتر باشد ذوب کردن نیاز به گرمای بیشتری دارد.
انجماد
فرآیند انجماد وارون فرآیند ذوب است، یعنی در این فرآیند مایع تبدیل به جامد می شود.
دمای نقطه ذوب با دمای نقطه ی انجماد برابر است، به طور مثال دمای ذوب یخ و دمای انجماد آب هر دو صفر درجه می باشد.
1 هر گاه از مایعی در دمی انجمادش گرما بگیریم، کاهش دما رخ نداده و مایع تبدیل به جامد می شود.
2 مقدار گرمایی که جسم از دست می دهد تا انجماد یابد برابر مقدار گرمایی است که جسم می گیرد تا ذوب شود.
گرمای نهان انجماد: \( - {L_F}\)
گرمای نهان انجماد، منفی گرمای نهان ذوب است.
فرمول گرمای انجماد: \({Q_F}\)
\({Q_F} = - m{L_F}\)
(\({Q_F}\) ) گرمای انجماد و بر حسب ژول
(m) جرم جسم مایع و برحسب کیلوگرم
(\({L_F}\) ) گرمای نهان ذوب و برحسب ژول بر کیلوگرم
جوش و میعان
فصل 4 : دما و گرما
جوش و میعان
تبخیر سطحی
بخار شدن مایع ها از سطح آزاد آنها در دمای محیط، را تبخیر سطحی می گوییم.
تا پیش از رسیدن به نقطه جوش مایع، تبخیر به طور پیوسته ای از سطح مایع رخ می دهد.
در تبخیر سطحی گرمای لازم برای تبخیر از مولکول های سطح از محیط پیرامون و در اغلب مواقع از مولکول های زیرین دریافت می کنند.
1 تا زمانی که دمای مایع به نقطه جوش نرسیده حبابی تشکیل نخواهد شد.
2 عمل تبخیر گرماگیر است، مولکول های بخار شده، انرژی گرمایی لازم جهت تبخیر را از مولکول های باقی مانده می گیرند. در نتیجه، انرژی درونی مایع باقی مانده کاهش یافته و دمای آن نیز کاهش می یابد.
شباهت تبخیر سطحی و جوش:
- در هر دو مایع به بخار تبدیل می شود.
- هر دو گرما گیرند.
تفاوت تبخیر سطحی و جوش:
- تبخیر سطحی در هر دمایی صورت می گیرد، ولی جوشیدن مایع در نقطه ی جوش صورت می گیرد.
- در تبخیر سطحی فقط مولکول های سطح مایع به بخار تبدیل می شوند، ولی در جوش مولکول های زیرین مایع نیز بخار شده و از سطح مایع خارج می شوند.
- در تبخیر سطحی با حباب (قل زدن) همراه نیست، ولی در جوش با قل زدن و صدای غلغل همراه است.
آهنگ تبخیر سطحی بنا به شرایط زیر افزایش می یابد:
- افزایش دمای محیط
- افزایش مساحت سطح آزاد مایع
- وزش باد
- کاهش رطوبت
- کاهش فشار هوا
نقطه جوش
هر مایعی در دمای ثابتی به نام دمای جوش که به جنس و فشار وارد بر آن بستگی دارد، به جوش آمده و تبدیل به بخار می شود.
1 افزایش فشار، سبب بالا رفتن دمای جوش آب می شود.
2 کاهش فشار، سبب پایین آمدن نقطه ی جوش آب می شود.
گرمای تبخیر
مقدار گرمایی است که هر مایع در نقطه ی جوش خود می گیرد تا به بخار در همان دما تبدیل شود.
گرمای تبخیر جسم به جنس جسم و جرم آن بستگی دارد.
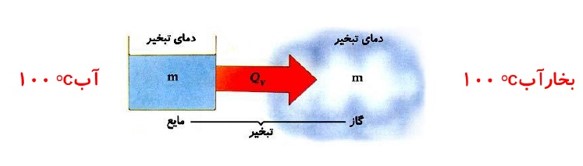
گرمای نهان تبخیر: \({L_V}\)
گرمایی است که به یک کیلو گرم از مایع در نقطه ی جوش می دهیم تا به بخار در همان دما تبدیل شود.
گرمای تبخیر واحد جرم اجسام را گرمای نهان تبخیر می گویند. \({L_V} = \frac{{{Q_V}}}{m}\)
گرمای نهان تبخیر اجسام فقط به جنس آنها بستگی دارد.
فرمول گرمای تبخیر:
\({Q_V} = m{L_V}\)
با افزایش دما جنبش مولکول ها افزایش یافته در نتیجه پیوند بین آنها سست تر می شود و مولکول ها برای جدا شدن از سطح به انرژی کمتری نیاز دارد.
میعان
فرآیند میعان وارون فرآیند تبخیر است یعنی در این فرآیند بخار به مایع در همان دما تبدیل می شود.
دمای نقطه ی میعان یک ماده با دمای نقطه ی جوش آن برابر است، به طور مثال دمای نقطه ی میعان آب \(100{}^0C\) است.
هر بخار هنگام میعان همان قدر گرما از دست می دهد که به هنگام تبخیر می گیرد.
گرمای نهان میعان منفی گرمای نهان تبخیر است.
فرمول گرمای میعان: \({Q_V}\)
\({Q_V} = - m{L_V}\)
(m) جرم گاز است.
مثال
گرمکنی در هر ثانیه \(200j\) انرژی فراهم می کند. چه مدت طول می کشد تا این گرمکن \(0/1Kg\) آب \(100{}^0C\) را به بخار \(100{}^0C\) تبدیل کند؟ (\({L_V} = 2256\frac{{KJ}}{{Kg}}\) )
\(\begin{array}{l}P = 200w\\t = ?\\m = 0/1Kg\\{L_F} = ?\\Q = pt\\{Q_V} = mL{}_V\\ \to pt = mL{}_V \to t = \frac{{mL{}_V}}{p} = \frac{{0/1 \times 2256 \times {{10}^3}}}{{200}} \to t = 1128s\end{array}\)
روش های انتقال گرما
فصل 4 : دما و گرما
روش های انتقال گرما
انتقال گرما
اختلاف دما باعث شارش گرما از جسم با دمای بالاتر به جسم با دمای پایین تر می شود. این شارش گرما به سه صورت انجام می شود:
1) رسانش

2) همرفتی
3) تابش
رسانش گرمایی در فلزات بیشتر از غیر فلزات است زیرا، در غیر فلزات گرما فقط از طریق ارتعاش اتم ها انتقال می یابد.
اما در فلزات، افزون بر ارتعاش اتم ها، الکترون های آزاد (درون فلز) هم در انتقال گرما نقش دارند. در واقع این الکترون های آزاد که نسبت به اتم ها بسیار کوچک هستند، در اثر دریافت گرما، سرعت گرفته و به سایر الکترون ها و اتم ها برخورد می کنند و به این ترتیب رسانندگی گرمایی فلزات را افزایش می دهند.
روش های انتقال گرما
الف) رسانش گرمایی:
در این روش به دلیل ارتعاش اتم ها و حرکت الکترون های آزاد در قسمت های گرم تر و گسترش این حرکت و ارتعاشات به سراسر جسم، گرما منتقل می شود، مانند انتقال گرما در فلزات
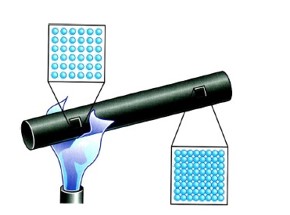
یکای رسانندگی گرمایی در SI طبق زیر است:
\(K = \frac{{J.m}}{{{m^2}.s.K}} = \frac{J}{{m.s.K}} = \frac{W}{{m.K}}\)
در پدیده ی رسانش:
گرما از یک بخش جسم به بخش دیگر آن شارش می کند، بدون آنکه مولکول های جسم جا به جا شوند.
به جسم هایی که می توانند گرما را (در زمان کوتاهی) به این روش منتقل کنند، رسانای گرما گفته می شود.
پدیده ی همرفت:
انتقال گرما همراه با انتقال ماده را همرفت می گویند. که مختص مایعات و گازها است.
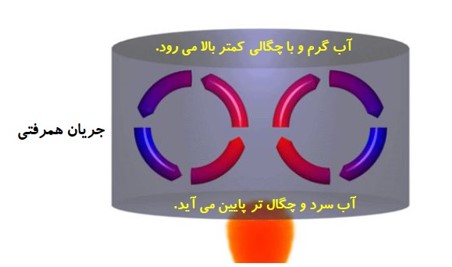
انواع جریان همرفتی
همرفت طبیعی
در این روش، به دلیل اختلاف چگالی شاره گرم و سرد به صورت خود به خود اتفاق می افتد. شاره با چگالی کمتر به طرف بالا حرکت می کند.
مانند گرم شدن آب درون قابلمه و هوای داخل اتاق و جریان های باد ساحلی و ... .
همرفت واداشته
شاره به کمک یک تلمبه (مصنوعی) به حرکت واداشته می شود تا با این حرکت انتقال گرما انجام شود.
سیستم گرم کننده ساختمان ها (شوفاژ)، سیستم خنک کننده موتور اتومبیل، دستگاه گردش خون در بدن جانوران خونگرم و ... .
همرفت طبیعی هوا
در شرایط عادی هوای اطراف سطح زمین گرم و هوای لایه های بالاتر سرد است. در این شرایط در اثر پدیده همرفت هوای گرم با چگالی کمتر به بالا رفته و هوای سرد تر با چگالی بیشتر جای آن را می گیرد و بدین ترتیب چرخش هوا در سطح زمین ایجاد می شود.
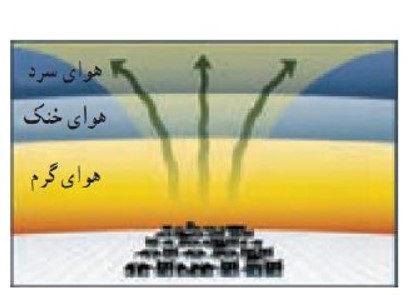
وارونگی هوا (وارونگی دما)
در روز های سرد زمستانی هوای اطراف سطح زمین سرد و چگالی آن زیاد و هوای لایه های بالاتر، گرم تر و چگالی آنها کمتر است. تحت این شرایط همرفت طبیعی هوا متوقف می شود که به آن وارونگی هوا می گویند.
وارونگی دما باعث انباشت آلاینده های موجود در لایه هوای سرد سطح زمین و در نتیجه آلودگی هوا در شهر های صنعتی می شود.
تابش گرمایی:
به انتقال گرما از طریق امواج الکترومغناطیسی که از اجسام منتشر می شود، تابش گرمایی می گویند.
1 اجسام در هر دمایی تابش الکترومغناطیسی گسیل می کنند.
2 در تابش گرمایی، انرژی برای انتقال نیازی به محیط مادی ندارد و گرمای تابش شده بسیار سریع (با سرعت نور) در خلاء نیز منتشر می شود.
3 در دماهای زیر حدود پانصد سانتی گراد عمدتا به صورت تابش فروسرخ است که نامرئی است.
4 بخشی از تابش گرمایی منتشر شده از اجسام، تابش نامرئی فروسرخ است که برای آشکار سازی آن از ابزاری به نام دمانگار استفاده می شود.
تابش گرمایی از سطح هر جسم به عوامل زیر بستگی دارد:
- دما: هرچه دمای جسم بیشتر باشد، آهنگ تابش آن نیز بیشتر است.
- مساحت: هرچه مساحت جسم بیشتر باشد، میزان تابش آن نیز بیشتر است.
- رنگ: هر قدر رنگ جسم مات و تیره تر و سطحش ناصاف تر باشد، جذب و تابش بهتری دارد.
- میزان صیقلی بودن: جسم هایی که سطح صیقلی و درخشان تری دارند، تابش کمتری دارند و بخش کمتری از گرمای دریافتی را جذب می کنند.
تف سنج
تف سنج وسیله ای برای اندازه گیری دما برای اجسام داغ است. اساس کار این وسیله، تابش گرمایی گسیل شده از سطح جسم است.
انواع تف سنج و ویژگی های مهم تف سنج:
تف سنج تابشی و تف سنج نوری
1) بدون تماس با جسم دمای آن را اندازه گیری می کند.
2) برای اندازه گیری دماهای بالای \(1100{}^0C\) بسیار مناسب اند.
اساس کار تف سنج نوری:
مقایسه رنگ و شدت نور تابیده از کوره با رنگ و شدت نور یک لامپ رشته ای است. همچنین این دماسنج به عنوان دماسنج معیار برای اندازه گیری این دماها انتخاب شده است.
از کاربرد های تابش گرمایی در پدیده های زیستی می توان به مار زنگی و کلم اسکانک اشاره کرد.
- آزمون آنلاین تمامی دروس پایه ریاضی
- گام به گام تمامی دروس پایه ریاضی
- ویدئو های آموزشی تمامی دروس پایه ریاضی
- گنجینه ای از جزوات و نمونه سوالات تمامی دروس پایه ریاضی
- فلش کارت های آماده دروس پایه ریاضی
- گنجینه ای جامع از انشاء های آماده پایه ریاضی
- آموزش جامع آرایه های ادبی، دستور زبان، قواعد زبان انگلیسی و ... ویژه پایه ریاضی
قانون گاز ها
فصل 4 : دما و گرما
قانون گاز ها
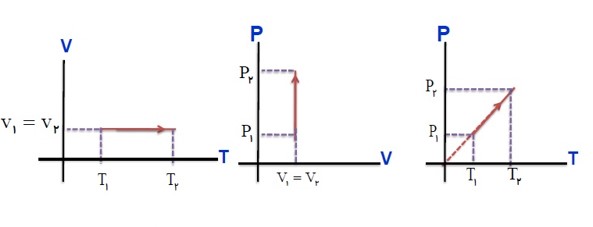
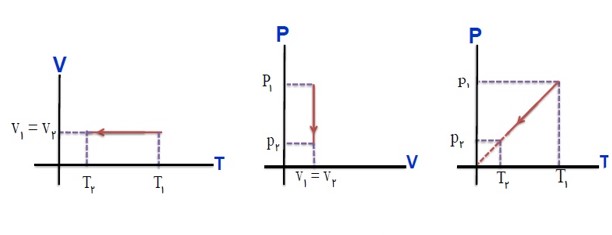
برسی گاز در فشار ثابت (قانون شارل):
در فشار ثابت، حجم گاز با دمای آن در مقیاس کلوین نسبت مستقیم دارد.
در فشار ثابت، نسبت حجم به دمای مطلق مقداری گاز کامل، مقداری ثابت است.
(فشار و جرم ثابت):
\(V \propto T \to \frac{V}{T} \to \frac{{{V_1}}}{{{T_1}}} = \frac{{{V_2}}}{{{T_2}}} = ...\)
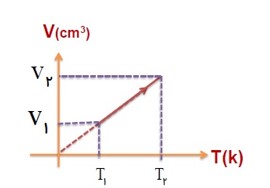
برسی گاز در حجم ثابت (قانون گی لوساک):
در حجم ثابت، فشار گاز با دمای آن در مقیاس کلوین نسبت مستقیم دارد.
(حجم و جرم ثابت):
\(P \propto T \to \frac{P}{T} \to \frac{{{P_1}}}{{{T_1}}} = \frac{{{P_2}}}{{{T_2}}} = ...\)
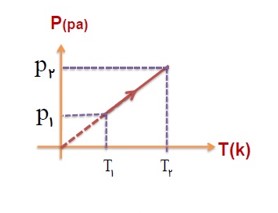
دماسنج گازی حجم ثابت:
اساس کار یک دماسنج گازی، تغیرات فشار با دما، در حجم ثابت است. در این دماسنج مقداری گاز (معمولا هیدروژن یا هلیم است) درون یک مخزن با حجم معین قرار می گیرد که این مخزن به لوله U شکلی که محتوی جیوه متصل است. وقتی مطابق شکل مخزن محتوی گاز در محیط مورد اندازه گیری قرار می گیرد، گاز درون آن منبسط یا منقبض می شود. حال با بالا یا پایین بردن بخش سمت راست لوله U شکل، سطح جیوه را در سمت چپ در یک سطح مرجع معین ثابت نگه می داریم، تا حجم گاز ثابت بماند. اگر لوله سمت راست روی یک خط کش مدرج قرار داده شود، می توان با یادداشت کردن مقادیر فشار در دماهای مختلف، نمودار P-T آن را رسم کنیم.
اگر این خط راست به کمک برون یابی در فشار های پایین تر ادامه می دهیم، در دمای \( - 273/15{}^0C\) محور دما را قطع خواهد کرد.
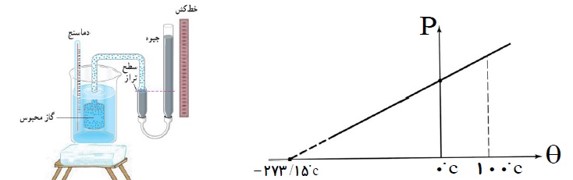
نمودار فشار بر حسب دما در حجم ثابت:
در واقع هیچ گازی (از هیدروژن و هلیم که در این دما سنج به کار می روند) تا این دما سرد نمی شود، زیرا قبل از رسیدن به این دما همه گاز ها مایع می شوند. برای انواع متفاوت گاز ها می تان این نمودار را به دست آورد، که در همه موارد، نقطه برخورد با محور دما همان \( - 273/15{}^0C\) خواهد بود که این همان صفر مطلق است. با یک تغییر مقیاس از درجه سلسیوس به کلوین دماهای منفی نیز حذف خواهند شد و از رابطه \(\frac{{{P_1}}}{{{T_1}}} = \frac{{{P_2}}}{{{T_2}}}\) نیز فشار منفی به دست نخواهد آمد.
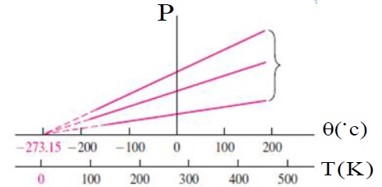
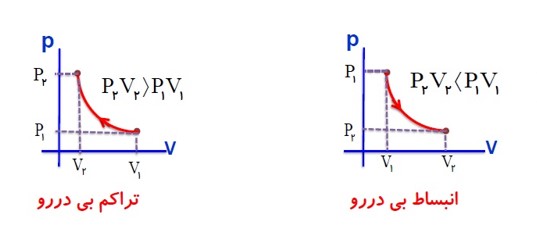
برسی گاز در دمای ثابت (قانون بویل و ماریوت):
در دمای ثابت، حجم مقدار معینی از گاز با فشار آن نسبت وارون دارد.
برای یک گاز کامل در دمای ثابت، حاصل ضرب حجم در فشار آن مقداری ثابت است.
\(T = T \to V \propto \frac{1}{P} \to {P_1}{V_1} = {P_2}{V_2} = ...\)
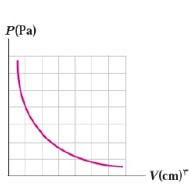
قانون آووگادرو
در دما و فشار یکسان، نسب حجم گاز V به تعداد مولکول های آن N ثابت است.
جرم گاز و یا به طور معادل n تعداد مول گاز است.
(دما و فشار یکسان)
\(\frac{V}{N} = \) فشار ثابت
\(n = \frac{N}{{{N_A}}}\)
\(\frac{V}{n} = \) مقدار ثابت
قانون گاز های آرمانی کامل:
- هنگامی که گاز ها بسیار رقیق یا چگالی آن به حد کافی کم باشد.
- گازی که مولکول های آن ها به حدی از هم دورند که برهم تاثیر چندانی نمی گذارند.
در گاز های کامل، معادله ی حالت آن ها ساده و مستقل از نوع گاز است. در این حالت گاز کامل نامیده می شوند.
از ترکیب چهار قانون فوق رابطه زیر حاصل می شود.
\(\frac{{PV}}{{nT}} = \) فشار ثابت \( \to PV = nRT\)
فرمول گاز های کامل
\(PV = nRT\)
در این فرمول
(P) فشار گاز و بر حسب (pa)
(V) حجم گاز و بر حسب (\({m^3}\) )
(n) تعداد مول های گاز و بر حسب مول
(R) ثابت گاز و بر حسب (\(\frac{J}{{mol.K}}\) )
(T) دمای گاز و بر حسب (K)
در صورتی که با تغییر شرایط یک گاز، مقدار آن تغییر نکند. \({n_1} = {n_2}\)
\(\begin{array}{l}PV = nRT \to n = \frac{{PV}}{{RT}} \to {n_1} = {n_2} \to \frac{{{P_1}{V_1}}}{{{T_1}R}} = \frac{{{P_2}{V_2}}}{{{T_2}R}}\\ \to \frac{{{P_1}{V_1}}}{{{T_1}}} = \frac{{{P_2}{V_2}}}{{{T_2}}}\end{array}\)
در استفاده از رابطه ی بالا فشار و حجم باید در در دو طرف تساوی هم واحد باشند اما باید دما تنها بر حسب کلوین باشد.
رابطه گاز کامل، در فرم مقایسه ای آن (برای دو گاز مختلف) به شکل زیر نوشته می شود:
\(\frac{{PV}}{{nT}} = R \to \frac{{{P_1}{V_1}}}{{{n_1}{T_1}}} = \frac{{{P_2}{V_2}}}{{{n_2}{T_2}}}\)
در نوشتن روابط نسبی فوق فشار و حجم هر واحدی می توانند باشند ولی برای نوشتن نسبت، دما باید بر حسب کلوین باشند.
رابطه چگالی گاز های کامل
به طور کلی چگالی یک گاز کامل با فشار آن نسبت مستقیم و با دمای مطلق آن نسبت عکس دارد.
\(\begin{array}{l}\rho = \frac{m}{v} \to \frac{{{\rho _2}}}{{{\rho _1}}} = \frac{{{v_1}}}{{{v_2}}}\\\frac{{{P_1}{V_1}}}{{{T_1}}} = \frac{{{P_2}{V_2}}}{{{T_2}}} \to \frac{{{V_1}}}{{{V_2}}} = \frac{{{P_2}{T_1}}}{{{P_1}{T_2}}}\\ \to \frac{{{\rho _2}}}{{{\rho _1}}} = \frac{{{P_2}}}{{{P_1}}} \times \frac{{{T_1}}}{{{T_2}}}\end{array}\)
معادله حالت، فرآیند های ترمودینامیک
فصل 5 : ترمودینامیک
معادله حالت، فرآیند های ترمودینامیک
ترمودینامیک
شاخه ای از علم فیزیک که رابطه بین گرما و کار تبدیل گرما به کار مکانیکی را مورد مطالعه قرار می دهد، ترمودینامیک نام دارد.
دستگاه:
ماده خاصی که معمولا به شکل گاز یا مایع است و با محیط پیرامون خود مبادله گرما و کار می کند و در فرآیند های ترمودینامیکی شرکت می کند، دستگاه می گوییم.
محیط:
اجسام پیرامون دستگاه را که می توانند با آن تبادل انرژی داشته باشند، محیط می نامیم.
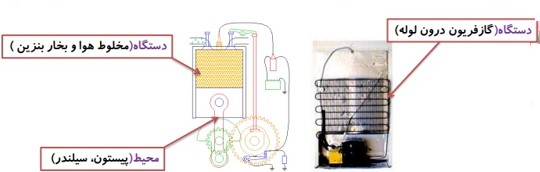
مثال
در این مثال گاز درون سیلندر، دستگاه نامیده می شود. پیستون، سیلندر و مکانی که سیلندر در آن واقع است، محیط نامیده می شوند.
انواع کمیت های ترمودینامیکی
کمیت های ماکروسپیک (مشاهده پذیر):
کمیت هایی که وضعیت ماده را در مقیاس بزرگ توصیف می کنند بدون آنکه درگیر جزئیات رفتار تک تک مولکول های گاز شود.
مانند فشار، حجم، دما، گرما، گرمای ویژه و ... .
کمیت های میکروسکوپیک:
کمیت هایی که به جزئیات رفتار تک تک مولکول ها مربوط می شوند.
مانند: سرعت، مکان، انرژی جنبشی، شتاب نیروی بین ذرات و ....
متغیر های ترمودینامیکی:
کمیت های ماکروسکوپی مانند فشار، دمای مطلق و حجم که حالت تعادل با آن ها توصیف می شوند، متغیر های ترمودینامیکی نامیده می شوند.
1 دستگاه موقعی در حالت تعادل ترمودینامیکی است که متغیر های ترمودینامیکی آن به طور خود به خودی تغییر نکند.
2 متغیر های ترمودینامیکی از یکدیگر مستقل نیستند.
حالات دستگاه
1) حالت تعادل:
متغیر های ترمودینامیکی گاز (دما، فشار و حجم) مقدار های ثابت و مشخصی دارند و به طور خود به خود تغییر نمی کنند.
2) حالت ناپایدار:
در تمام متغیر های ترمودینامیکی (دما، فشار و حجم) یکسان نباشد و حالت گاز ثابت و پایدار نباشد.
معادله حالت
رابطه ی بین متغیر های ترمودینامیکی، معادله ی حالت دستگاه نامیده می شود.
(رابطه بین سه کمیت P، V و T)
اگر گاز آرمانی (کامل) باشد، معادله حالت آن ساده و مستقل از نوع گاز است و با قانون گاز کامل معادله \(PV = nRT\) داده می شود.
1 برای نمایش حالت گاز باید از سه محور عمود بر هم P، V و T استفاده کرد، ولی حل مسئله ها با نمایش حالت در صفحه مختصات ساده تر می شود.
2 هنگامی که دو کمیت از معادله حالت معلوم باشد، می گوییم ه حالت دستگاه مشخص است.
3 از رابطه قانون گاز های کامل می توان کمیت سوم را که مجهول است را پیدا کرد.
فرآیند های ترمودینامیکی
به تحول هایی که در آنها دستگاه از یک حالت تعادل (\({T_1},{V_1},{P_1}\) ) به حالت تعادل دیگر (\({T_2},{V_2},{P_2}\) ) می رود.
برای مثال وقتی هوای درون سرنگی را متراکم کنیم، می گوییم گاز یک فرآیند ترمودینامیکی را پیموده است.
فرآیند ایستاوار:
هرگاه در طول فرآیند، دستگاه همواره بسیار نزدیک به حالت تعادل بوده (و گرمای داده شده به دستگاه در هر مرحله بسیار کوچک باشد) و سریع به تعادل برسد. چنین فرآیندی را فرایند ایستاوار می نامند.
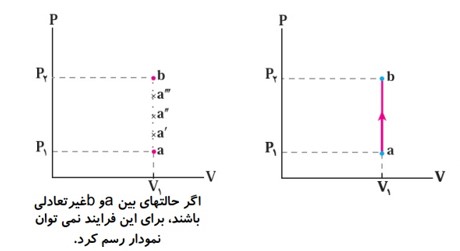
نمودار های مختلف فرآیند آرمانی:
در فرآیند های ترمودینامیکی یک دستگاه از یک حالت ابتدایی (i) به یک حالت نهایی (f) می رود می توان همه مراحل فرآیند را در نمودار های (P-V) یا (P-T) یا (V-T) نمایش داد.
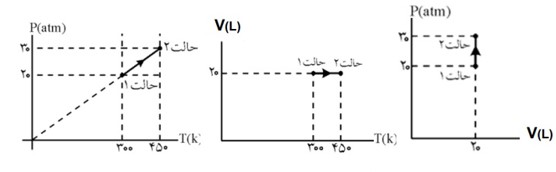
از رابطه زیر می توان یکی از کمیت های مجهول در نقاط (i) یا (f) را پیدا کرد.
\(\frac{{{P_1}{V_1}}}{{{T_1}}} = \frac{{{P_2}{V_2}}}{{{T_2}}}\)
تبادل انرژی، قانون اول ترمودینامیک
فصل 5 : ترمودینامیک
تبادل انرژی، قانون اول ترمودینامیک
انواع تبادل انرژی بین محیط و دستگاه:
گرما: نوعی انرژی است که به علت اختلاف دما بین دستگاه و محیط مبادله می شود.
بنا به قرارداد:
گرمایی که دستگاه می گیرد را با علامت مثبت نشان می دهیم. \(Q = mc\Delta \theta \)
گرمایی که دستگاه از دست می دهد با علامت منفی نشان می دهیم.
کار: عبارت است از حاصل ضرب نیرو در جا به جایی پیستون در کسینوس زاویه بین نیرو و جا به جایی \(W = F \times d \times \cos \theta \)
1 در شکل زیر، نیرویی را که پیستون به گاز وارد می کند با F و نیرویی را که گاز به پیستون اثر می دهد با \(F'\) نشان داده ایم.
چه پیستون ثابت بماند و چه نماند، جهت این نیرو ها تغییر نمی کند.
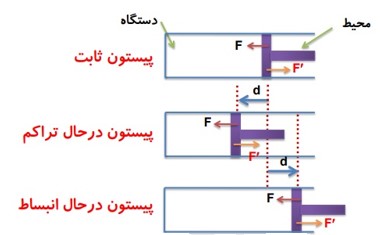
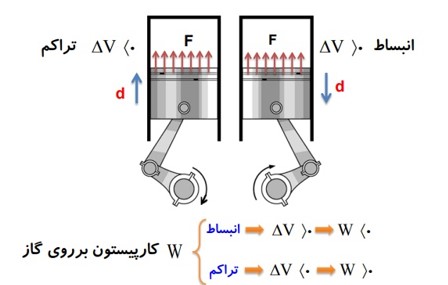
2 کاری را که محیط روی دستگاه انجام می دهد با W نشان می دهیم، در واقع کاری است که نیروی F روی گاز انجام می دهد.
3) همزمان با کاری را که محیط روی دستگاه انجام می دهد W، دستگاه هم روی محیط کار انجام می دهد که آن را با نماد \(W'\) نشان می دهیم.
با توجه به عمل و عکس العمل بودن نیرو هایی که محیط و دستگاه به هم وارد می کنند میفهمیم که همیشه \(W = - W'\) است.
کار پیستون روی گاز = منفی کار گاز روی پیستون
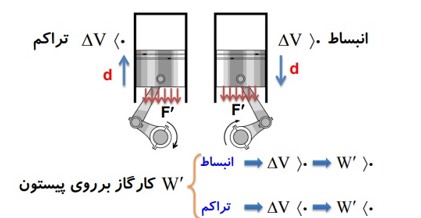
منبع گرمایی:
جسمی است که جرم آن در مقابل جرم دستگاهی که با آن تبادل گرما دارد، چنان بزرگ است که می تواند مقدار گرمای زیادی بگیرد، یا از دست بدهد، بی آنکه تغییر دمای محسوسی بکند.
مثلا سوزن را حرارت دهیم و داخل یک استخر بزرگ حاوی آب بیاندازیم، آب استخر منبع گرمایی برای سوزن محسوب می شود.
انرژی درونی:
به مجموع انرژی های جنبشی و پتانسیل مولکول های یک دستگاه انرژی درونی آن نامیده می شود.
1 تغییر انرژی درونی گاز کامل فقط تابع دمای مطلق گاز است.
2 طبق معادله حالت چون T دمای مطلق یک گاز متناسب با PV (حاصل ضرب فشار گاز در حجم گاز) است.
اصل پایستگی انرژی برای هر دستگاه:
گرمای افزوده شده به دستگاه = کار انجام شده توسط دستگاه + افزایش انرژی درونی دستگاه
\(Q = \Delta U + W'\)
قانون اول ترمودینامیک
تغییر انرژی درونی دستگاه برابر است با مجموع گرمایی که دستگاه دریافت می کند و کاری که بر روی آن انجام می شود.
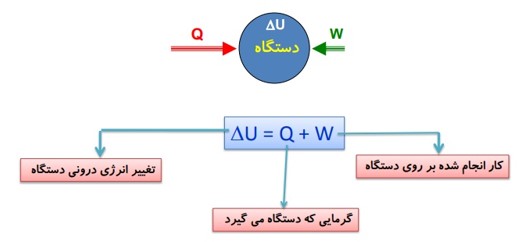
کار انجام شده و گرمای مبادله شده در فرآیند های ترمودینامیکی یک دستگاه، به نوع فرآیند ها در مسیر بستگی دارد.
\(\Delta U = Q + W\)
سوخت ساز بدن و قانون اول ترمودینامیک:
انرژی درونی بدن ما از انرژی شیمیایی ذخیره شده در مواد غذایی تامین می شود. با انجام فعالیت های مختلف، انرژی درونی بدن طبق قانون اول ترمودینامیک به کار و گرما تبدیل می شود.
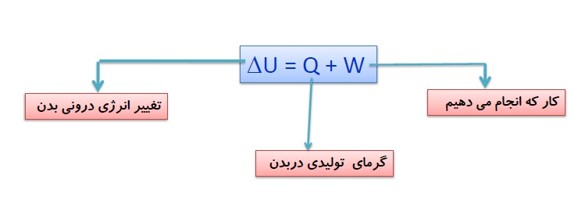
آهنگ سوخت و ساز بدن
آهنگ تبدیل انرژی شیمیایی مواد غذایی به انرژی درونی بدن را آهنگ سوخت و ساز بدن می نامند.
این آهنگ برحسب کیلو کالری بر ساعت یا بر حسب وات بیان می شود.
- آزمون آنلاین تمامی دروس پایه ریاضی
- گام به گام تمامی دروس پایه ریاضی
- ویدئو های آموزشی تمامی دروس پایه ریاضی
- گنجینه ای از جزوات و نمونه سوالات تمامی دروس پایه ریاضی
- فلش کارت های آماده دروس پایه ریاضی
- گنجینه ای جامع از انشاء های آماده پایه ریاضی
- آموزش جامع آرایه های ادبی، دستور زبان، قواعد زبان انگلیسی و ... ویژه پایه ریاضی
فرآیند هم حجم
فصل 5 : ترمودینامیک
فرآیند هم حجم
انواع فرآیند های ترمودینامیکی:
- فرایند هم حجم \({V_1} = {V_2}\)
- فرایند هم فشار \({P_1} = {P_2}\)
- فرایند هم دما \({T_1} = {T_2}\)
- فرایند بی در رو \(Q = 0\)
1) فرایند هم حجم
تحولی از یک گاز که در طول آن، حجم گاز ثابت است را فرآیند هم حجم می نامند.
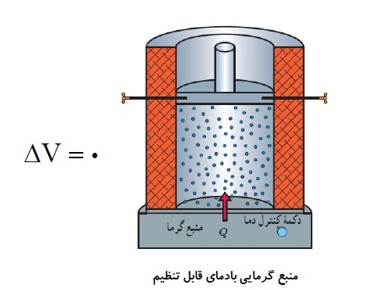
نمونه ای از یک فرایند هم حجم:
اتومبیل هنگام طی یک مسیر، حجم لاستیک اش تغییر نمی کند.
در یک فرایند هم حجم، گاز در حین گرفتن گرمای \({Q_V}\) از چشمه، دما و فشارش افزایش می یابد.
کار انجام شده در فرایند هم حجم
در این فرایند کار انجام شده صفر، فقط بین دستگاه و محیط گرما مبادله می شود.
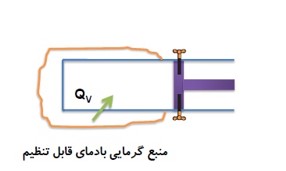
\(W = 0J\)
نمودار های مختلف فرایند هم حجم موقعی که دستگاه گرما می گیرد.
\(PV = nRT \to P = \left( {\frac{{nR}}{V}} \right)T \to P \propto T\)
نمودار های مختلف فرایند هم حجم موقعی که دستگاه گرما از دست می دهد.
گرمایی ویژه مولی یک گاز در حجم ثابت: \({C_V}\)
مقدار گرمایی است که در حجم ثابت به یک مول گاز داده می شود تا دمای آن یک کلوین بالا رود.
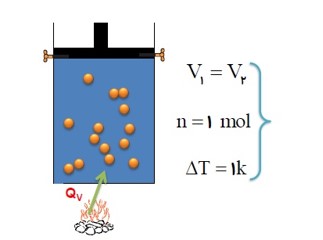
با تقریب خوبی می توان نشان داد که گرمای ویژه مولی در حجم ثابت به جنس گاز بستگی ندارد، برای گاز های کامل:
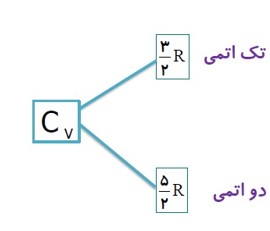
فرآیند هم فشار
فصل 5 : ترمودینامیک
فرآیند هم فشار
تحولی را که در طی آن فشار گاز ثابت بماند، فرآیند هم فشار می نامند.
در این فرآیند دستگاه با دریافت گرما از چشمه گرم منبسط می شود و با از دست دادن گرما متراکم می گردد. (با فرض این که اصطکاک بین پیستون و استوانه ناچیز باشد.)
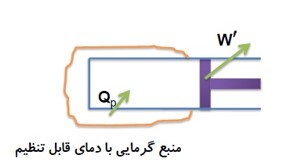
شرایط ایجاد فرایند هم فشار
- باید اصطکاک بین پیستون و استوانه ناچیز باشد.
- مبادله گرما بین منبع گرم و دستگاه خیلی آهسته صورت گیرد تا هم دستگاه در هر لحظه نزدیک به وضعیت تعادل باشد و هم پیستون خیلی آرام حرکت کند.
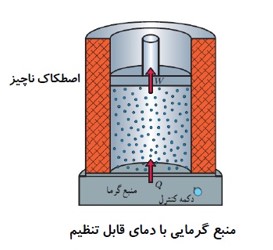
رسم نمودار های فرایند هم فشار: (انبساط)
در فرایند انبساط هم فشار، اگر دستگاه گرمای \({Q_P}\) را بگیرد. کار \(W'\) را انجام می دهد.
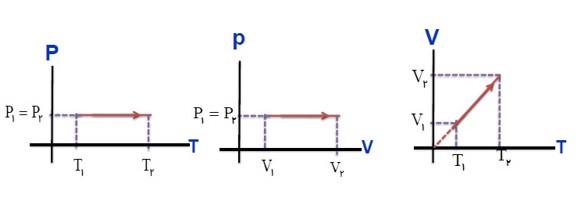
\(PV = nRT \to V = \left( {\frac{{nR}}{P}} \right)T \to V \propto T\)
رسم نمودار های فرایند هم فشار: (تراکم)
در تراکم هم فشار، محیط کار W انجام داده و دستگاه گرمای \({Q_P}\) را از دست می دهد.
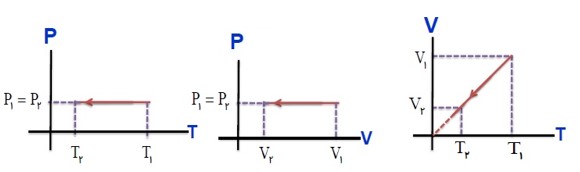
محاسبه کار در یک تحول انبساطی (هم فشار):
کاری که دستگاه (گاز) بر روی محیط (پیستون) انجام می دهد. (انبساط گاز) \(W'\)
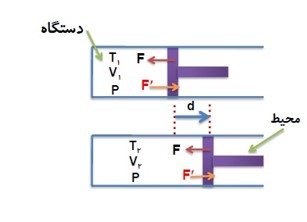
\(\begin{array}{l}1)W' = P.Ad\\Ad = \Delta V\\ \to W' = P.\Delta V\\2)W = - P.Ad\\Ad = \Delta V\\ \to W = - P.\Delta V\end{array}\)
کار انجام شده در فرایند هم فشار
کار انجام شده بر روی دستگاه \(W = - P.\Delta V\)
کار انجام شده بر روی محیط \(W' = P.\Delta V\)
طبق معادله حالت می توان کار را از رابطه ی زیر نیز بدست آورد.
\(W = - nR\Delta T\)
محاسبه ی کار به کمک نمودار:
سطح زیر نمودار (P-V) برابر قدر مطلق کار مبادله شده بین دستگاه و محیط است.
کار انجام شده بر روی گاز در تراکم (\(W\rangle 0\) ) و در انبساط (\(W\langle 0\) )
\(\left| W \right| = S = \left| { - P.\Delta V} \right|\)
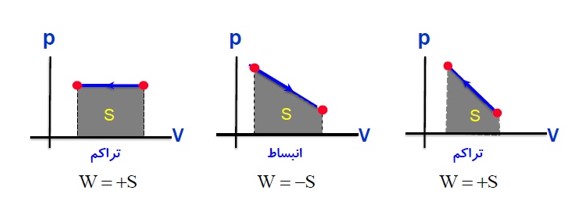
فرایند هم دما و بی در رو
فصل 5 : ترمودینامیک
فرایند هم دما و بی در رو
فرآیند هم دما
دمای دستگاه در حین این فرایند ثابت می ماند.
در فرایند هم دما با وجود ثابت ماندن دما، بین محیط و دستگاه گرما مبادله می شود.
برای گاز آرمانی که انرژی درونی آن فقط تابعی از دماست، تغییر انرژی درونی صفر است.
\(\Delta U = Q + W \to \Delta U = 0 \to Q = - W \to Q\langle 0\)
رسم نمودار های فرایند هم دما: (تراکم)
در یک فرایند هم دما، با انجام کار W، دستگاه گرمای Q را از دست می دهد.
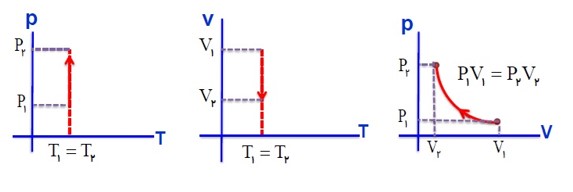
\(PV = nRT \to P = \frac{{nRT}}{V} \to P \propto \frac{1}{V}\)
رسم نمودار های فرایند هم دما: (انبساط)
در یک فرایند هم دما، اگر گاز گرمای Q را بگیرد کار \(W'\) را روی محیط انجام می دهد.
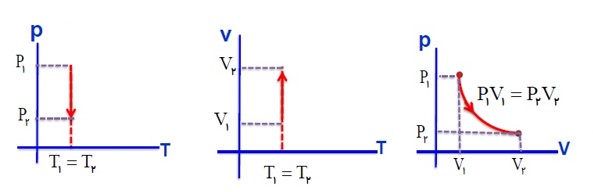
به طور کلی نمودار های فرآیند هم دما به صورت زیر است.
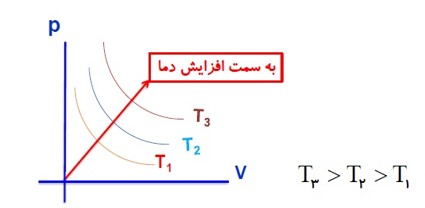
فرآیند بی در رو
در این فرایند بین دستگاه و محیط گرما مبادله نمی شود.
برای انجام فرایند بی در رو
- باید دستگاه را عایق بندی کنیم و عمل تراکم یا انبساط را به آهستگی انجام دهیم.
- گاز چنان با سرعت کم متراکم یا منبسط شود که فرصت مبادله گرما با محیط را پیدا نکند. بنابراین در فرایند بی در رو Q=0 است.
از فرایند بی در رو می توان به دهانه ی تلمبه ی دوچرخه اشاره کرد که دهانه دوچرخه مسدود شده است و پیستون با سرعت به پایین رانده می شود.
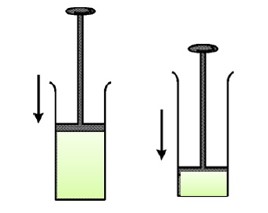
در فرایند تراکم بی در رو که با انجام کار W بر روی گاز، حجم V آن کاهش پیدا کرده فشار و دما افزایش می یابند.
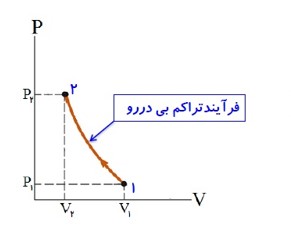
\(\Delta U = Q + W \to Q = 0 \to W\rangle 0 \to \Delta U\rangle 0 \to \Delta T\rangle 0\)
در فرایند انبساط بی در رو که با انجام کار W بر روی گاز، حجم آن افزایش پیدا کرده، فشار و دما کاهش می یابند.
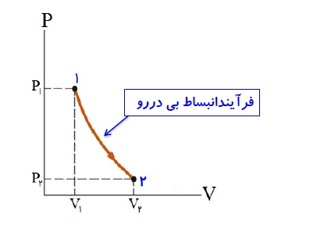
\(\Delta U = Q + W \to Q = 0 \to W\langle 0 \to \Delta U\langle 0 \to \Delta T\langle 0\)
نمودار فرایند بی در رو
مقایسه تراکم بی در رو و هم دما
در تراکم گاز، فشار و دمای گاز افزایش می یابد. در فرایند هم دما، برای ثابت نگه داشتن دمای گاز باید از آن گرما گرفت ولی در فرایند بی در رو، از گاز گرما گرفته نمی شود و از این رو در انتهای مسیر، فشار و دمای گاز در فرایند بی در رو بیش از فرایند هم دما است.
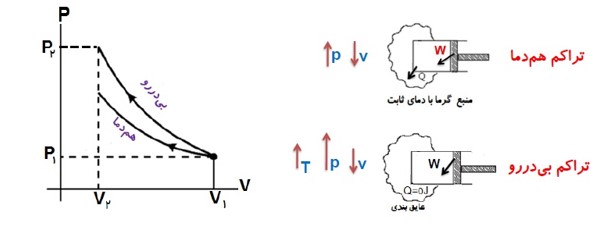
شیب نمودار در فرایندی در رو بیشتر از شیب نموار هم دما است.
مقایسه انبساط بی در رو و هم دما
در انبساط گاز، فشار و دمای گاز کاهش می یابد. در فرایند هم دما، برای ثابت نگه داشتن دمای گاز باید به گاز، گرما دهیم؛ ولی چون در انبساط بی در رو، گاز هیچ گونه گرمایی دریافت نمی کند، در انتهای مسیر، فشار و دمای گاز در فرایند بی در رو پایین تر از فشار و دمای گاز فرایند هم دما خواهد بود.
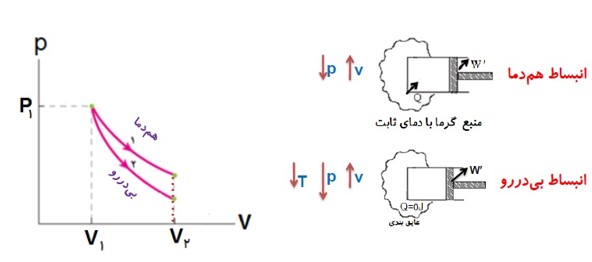
مقایسه کار انجام شده روی دستگاه در سه فرایند هم فشار، هم دما و بی در رو
در انبساط یکسان قدر مطلق کار انجام شده روی دستگاه در فرایند هم فشار از بقیه فرایند ها بیشتر و قدر مطلق تغییرات فشار و دما در فرایند بی در رو از بقیه بیشتر است.
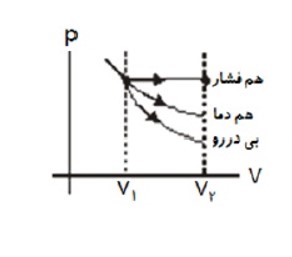
در تراکم یکسان، مقدار کار انجام شده روی دستگاه، در فرایند بی در رو از بقیه فرایند ها بیشتر و دما ی نهایی گاز نیز در فرایند بی در رو از بقیه فرایند ها بیشتر است.
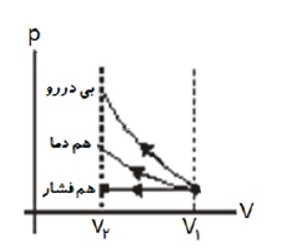
نمودار P-T:
در فرایند ab، V ثابت است و داریم:
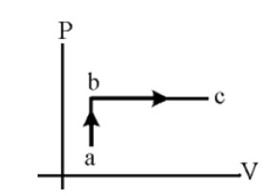
\(PV = nRT \to P = \left( {\frac{{nR}}{V}} \right)T \to P \propto T\)
چون فشار افزایش یافته بنابراین دما نیز افزایش یافته است. در فرایند bc فشار ثابت مانده است و حجم افزایش یافته است، بنابراین دمای گاز نیز افزایش یافته است.
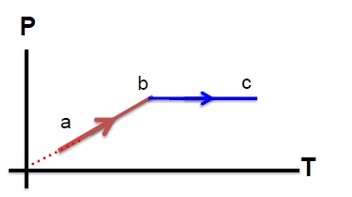
1 تغییر انرژی درونی دستگاه به نوع فرآیند ها بستگی ندارد.
2 تغییر انرژی درونی دستگاه (\(\Delta U\) ) با جرم ثابت فقط بستگی به تغییر دمای مطلق (\(\Delta T\)) دستگاه دارد.
مثال
مقدار معینی از یک گاز کامل در یک فرایند بی در رو 100 ژول کار انجام می دهد، تغییر انرژی درونی گاز چند ژول است؟
\(\begin{array}{l}Q = 0J\\W' = 100J \to W = - 100J\\\Delta U = ?\\\Delta U = Q + W \to \Delta U = 0 - 100 = - 100J\end{array}\)
- آزمون آنلاین تمامی دروس پایه ریاضی
- گام به گام تمامی دروس پایه ریاضی
- ویدئو های آموزشی تمامی دروس پایه ریاضی
- گنجینه ای از جزوات و نمونه سوالات تمامی دروس پایه ریاضی
- فلش کارت های آماده دروس پایه ریاضی
- گنجینه ای جامع از انشاء های آماده پایه ریاضی
- آموزش جامع آرایه های ادبی، دستور زبان، قواعد زبان انگلیسی و ... ویژه پایه ریاضی
چرخه ترمودینامیکی
فصل 5 : ترمودینامیک
چرخه ترمودینامیکی
مجموعه چند فرایند مختلف که دستگاه پس از طی کردن فرایند ها به حالت اولیه خود باز می گردد.
مشخصه اصلی یک چرخه:
بی تغییر ماندن انرژی درونی کل در آن است. (\(\Delta T = 0\) )
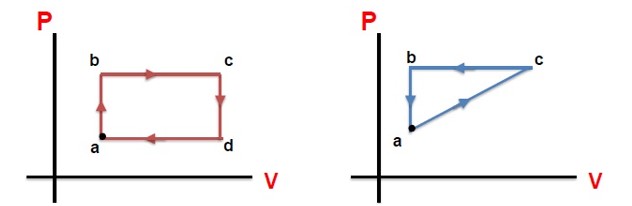
قدر مطلق کار انجام شده در چرخه:
برابر سطح محصور بین فرآیند ها است. \(W = S\)
گرمای مبادله شده در چرخه:
\(\Delta U = 0 \to Q + W = 0 \to Q = - W\)
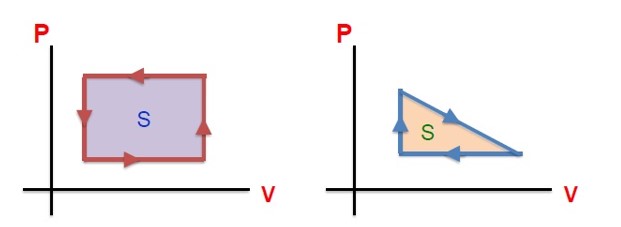
1 اگر جهت چرخه ساعتگرد باشد، کل کار انجام شده روی دستگاه در چرخه منفی و در کل چرخه، گاز گرما دریافت می کند، یعنی:
\(W\langle 0 \to Q = - W \to Q\rangle 0\)
2 اگر جهت چرخه پادساعتگرد باشد، کل کار انجام شده روی دستگاه در چرخه مثبت و در کل چرخه، گاز گرما از دست می دهد، یعنی:
\(W\rangle 0 \to Q = - W \to Q\langle 0\)
خلاصه ای از قانون اول ترمودینامیک برای چهار حالت زیر:

ماشین گرمایی
فصل 5 : ترمودینامیک
ماشین گرمایی
وسیله ای است که با استفاده از فرایند های ترمودینامیکی گرمای حاصل از سوخت را به کار تبدیل می کند.
هر ماشین گرمایی یک چرخه ی معین را تکرار می کنند.
انواع ماشین گرمایی
ماشین گرایی برون سوز:
دستگاه با دو منبع با دمای بالا و دمای پایین در تماس است و گرما از منبع گرم تر در بیرون دستگاه به آن داده شود و کار خالصی توسط دستگاه در طی چرخه انجام می شود.
مانند ماشین نیوکامن، ماشین استرلینگ و ماشین بخار وات
ماشین گرمایی درون سوز:
گرما در اثر آتش گرفتن ماده سوختی (دستگاه) که در داخل سیلندر قرار دارد تامین می شود.
مانند موتور های بنزینی و دیزلی
تحلیل دقیق چرخه ی یک ماشین بخار دشوار است. اما با برخی ساده سازی ها می توان به نحلیل این ماشین ها پرداخت و به چرخه ی آرمانی موسوم به چرخه رانکین رسید.
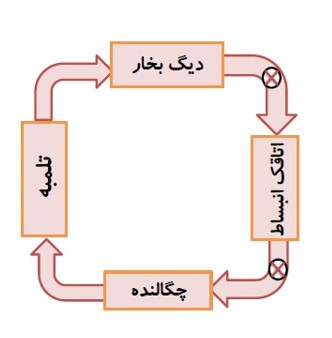
در چرخه ماشین بخار:
- دستگاهی که چرخه را می پیماید، آب است.
- کوره، منبع دمای بالا و گرمای \({Q_H}\) را به دستگاه (آب) می دهد.
- دستگاه روی محیط ار انجام می دهد و باعث انبساط دستگاه می شود.
- منبع دمای پایین چگالنده و لوله های آب سرد است و گرمای \({Q_L}\) را از دستگاه می گیرد.
فرایند هایی که آب در ماشین بخار وات طی می کند، به چهار مرحله اصلی تقسیم می کنیم:
الف) مرحله اول:
در این مرحله آب درون دیگ بخار در فشار ثابت از کوره گرما می گیرد و به بخار تبدیل می شود.
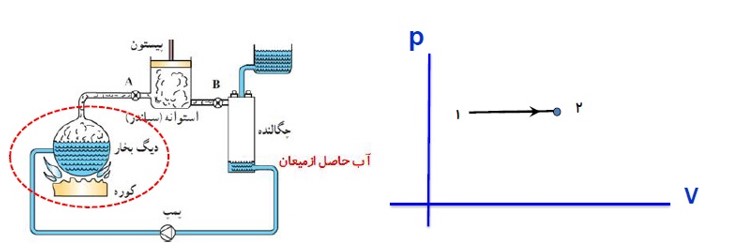
ب) مرحله دوم:
شیر ورودی باز می شود. بخار آب که دما و فشار آن بسیار زیاد است وارد اتاقک انبساط می شود و دما و فشار آن کاهش می یابد در این مرحله بخار آب بر روی محیط کار انجام می دهد.
(چون این انبساط بسیار سریع است این فرایند را بی در رو می توان در نظر گرفت.)
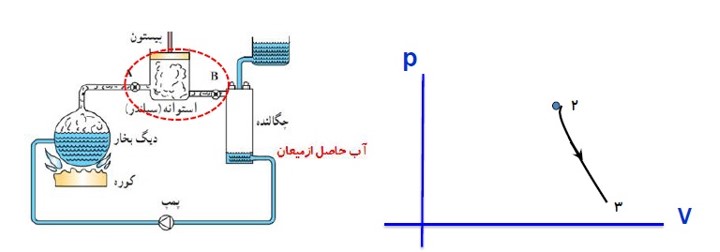
ج) مرحله سوم:
در چگالنده بخار آب در فشار ثابت گرما از دست می دهد و به مایع تبدیل می شود. در این فرایند دما و حجم بخار آب کاهش می یابد.
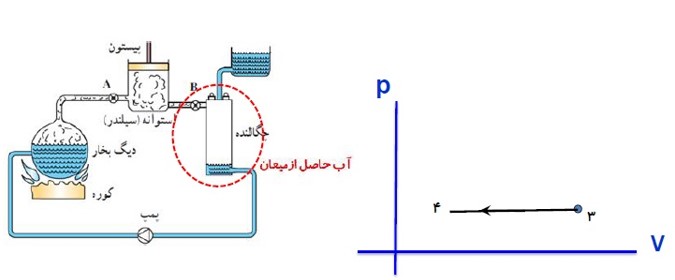
د) مرحله چهارم:
تلمبه (پمپ)، آب حال از میعان را به دیگ بخار بر میگرداند و فشار آن را به طور بی در رو به فشار اولیه می رساند (فقط تغییرات کوچکی در دما و حجم مایع رخ می دهد)
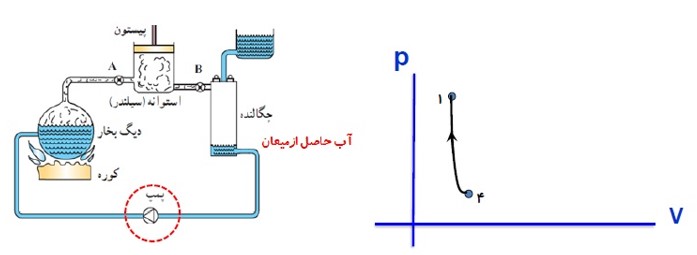
چرخه رانکین
1 در حین کار با ماشین بخار این چرخه دائما تکرار می شود.
2 دستگاه در این چرخه به طور عمده با دو منبع گرما (کوره و چگالنده) تبادل گرما می کند.
3 کوره را که در دمای بالاتری قرار دارد منبع گرم و چگالنده را منبع سرد می نامیم.
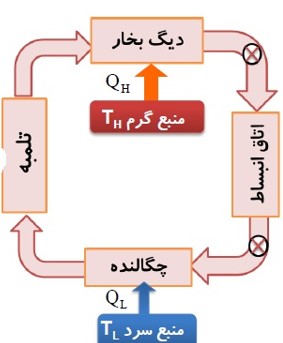
مرحله های کار ماشین گرمایی درون سوز
1) ضربه ی مکش
2) ضربه ی تراکم
3) آتش گرفتن
4) ضربه ی قدرت
5) تخلیه
6) ضربه ی خروج گاز
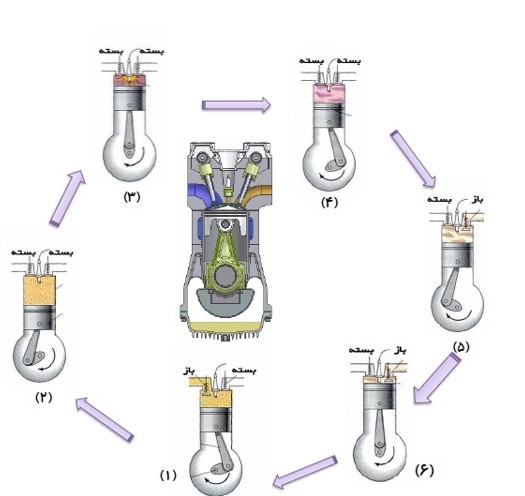
1) ضربه ی مکش
با پایین آمدن پیستون مخلوط بنزین و هوا از طریق دریچه ورودی وارد استوانه می شوند.
وقتی پیستون به پایین ترین وضعیت خود رسید، این دریچه بسته می شود.

2) ضربه ی تراکم
پیستون بالا می آید و مخلوط را متراکم می کند و به حجم اولیه می رساند در این وضعیت دمای مخلوط بسیار بالا می رود.
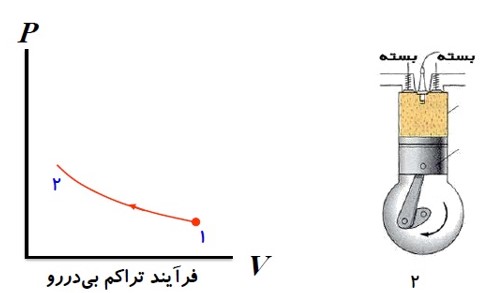
3) آتش گرفتن
هنگامی که پیستون به بالا ترین وضعیت خود رسید، شمع جرقه می زند، مخلوط آتش می گیرد و دما و فشار آن تا مقدار زیادی بالا می رود.
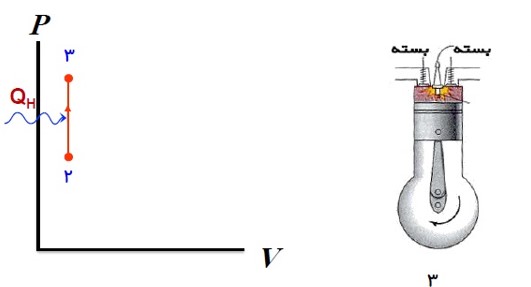
4) ضربه ی قدرت
در این مرحله در اثر فشار زیاد دستگاه منبسط می شود و پیستون را به طرف پایین می راند. کاری که دستگاه بر روی محیط انجام می دهد در این مرحله حاصل می شود.
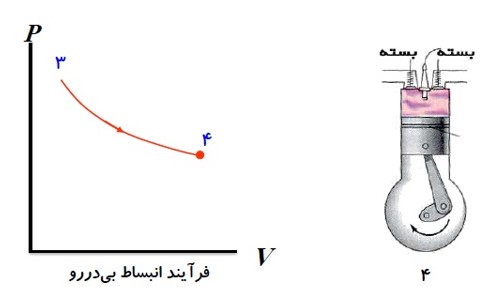
5) تخلیه
در حالی که پیستون در پایین ترین وضعیت حجمی قرار دارد، سوپاپ درچه خروجی باز می شود و قسمتی از محصولات احتراق به صورت دود از دریچه خروجی خارج می شود. به این ترتیب مقدار زیادی گرما به بیرون رانده می شود.
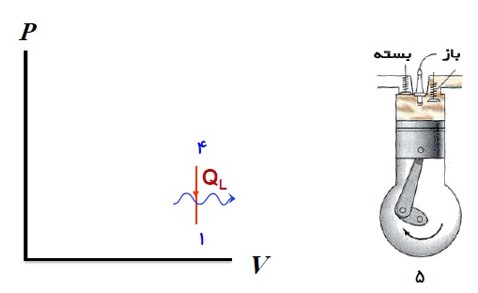
6) ضربه ی خروج گاز
پیستون بالا می آید و بقیه محصولات احتراق را بیرون می راند و حجم فضای بالای پیستون از بیشترین به مقدار اولیه می رسد
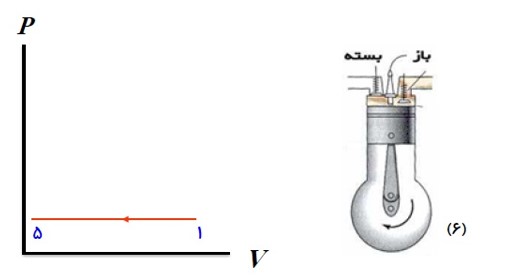
بازده، قانون دوم ترمودینامیک
فصل 5 : ترمودینامیک
بازده، قانون دوم ترمودینامیک
بازده ماشین گرمایی: \(\eta \) (اتا)
نسبت کار بدست آمده \(\left| W \right|\) به مقدار گرمای گرفته شده \({Q_H}\) از چشمه ی گرمایی را بازده ماشین گرمایی می گویند.
\(\eta = \frac{{\left| W \right|}}{{{Q_H}}}\)
مفهوم بازده ماشین گرمایی:
نشان می دهد که چه کسری از گرمای حاصل از سوخت به انرژی مفید خروجی تبدیل می شود.
علامت کار و گرمای مبادله شده در ماشین گرمایی
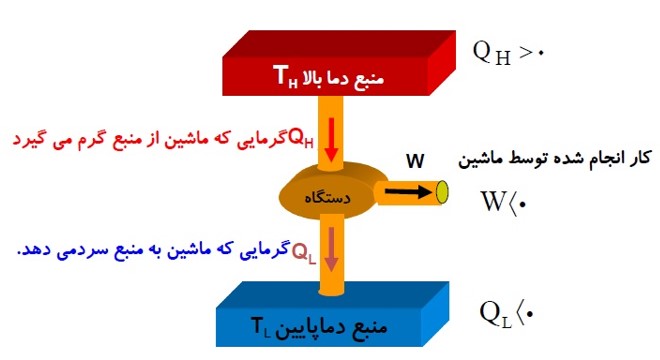
قانون اول ترمودینامیک برای ماشین گرمایی
چون ماشین یک چرخه را طی می کند، \(\Delta U = 0\) است.
\(\begin{array}{l}\Delta U = Q + W\\ \to \Delta U = 0,Q = {Q_H} - \left| {{Q_L}} \right|,W = - \left| W \right|\\ \to 0 = {Q_H} - \left| {{Q_L}} \right| - \left| W \right| \to {Q_H} = \left| W \right| + \left| {{Q_L}} \right|\end{array}\)
رابطه ی بازده ماشین گرمایی با قانون اول ترمودینامیک:
بازدهی ماین گرمایی همواره کوچک تر از یک است زیرا \(\left| W \right|\langle {Q_H}\)
\(\begin{array}{l}\left| W \right| = {Q_H} - \left| {{Q_L}} \right|\\\eta = \frac{{\left| W \right|}}{{{Q_H}}}\\ \to \eta = \frac{{{Q_H} - \left| {{Q_L}} \right|}}{{{Q_H}}} \to \eta = 1 - \frac{{\left| {{Q_L}} \right|}}{{{Q_H}}}\end{array}\)
1 بازده ماشین گرمایی واقعی از بازده ماشین های آرمانی کمتر است.
2 بازده تقریبی ماشین های گرمایی به صورت زیر است:
- بازده ماشین های درون سوز بنزینی: در حدود 20 تا 30 درصد
- بازده ماشین های درون سوز دیزلی: در حدود 30 تا 35 درصد
- بازده ماشین های برون سوز بخار: در حدود 30 تا 40 درصد
روش های افزایش بازده ماشین گرمایی:
- کاهش اصطکاک میان پیستون و سیلندر
- با عایق بندی مناسب، می توانیم تا حدی از اتلاف گرمای کوره جلوگیری کنیم.
- دمای منبع گرم را افزایش و دمای منبع سرد را کاهش دهیم.
هر ماشین گرمایی بخشی از انرژی گرمایی دریافتی از منبع گرم را تبدیل به کار می کند و بقیه را به منبع سرد می سپارد.
ماشین گرمایی نمی تواند تمام گرما را تبدیل به کار کند.
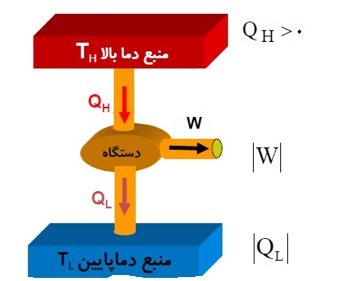
قانون دوم ترمودینامیک (به بیان ماشین گرمایی)
ممکن نیست دستگاه چرخه ای را بپیماید که در طی آن مقداری گرما را از منبع دما بالا جذب و تمام آن را به کار تبدیل کند.
یعنی ممکن نیست بازده یک ماشین گرمایی برابر 100 درصد باشد.
- آزمون آنلاین تمامی دروس پایه ریاضی
- گام به گام تمامی دروس پایه ریاضی
- ویدئو های آموزشی تمامی دروس پایه ریاضی
- گنجینه ای از جزوات و نمونه سوالات تمامی دروس پایه ریاضی
- فلش کارت های آماده دروس پایه ریاضی
- گنجینه ای جامع از انشاء های آماده پایه ریاضی
- آموزش جامع آرایه های ادبی، دستور زبان، قواعد زبان انگلیسی و ... ویژه پایه ریاضی
یخچال
فصل 5 : ترمودینامیک
یخچال
بیان قانون دوم ترمودینامیک (به بیان یخچالی)
ممکن نیست گرما به طور خود به خود از جسم با دمای پایین تر به جسم با دمای بالاتر منتقل شود.

ساختمان یخچال
سرد سازی به وسیله دستگاه (گاز فریون)
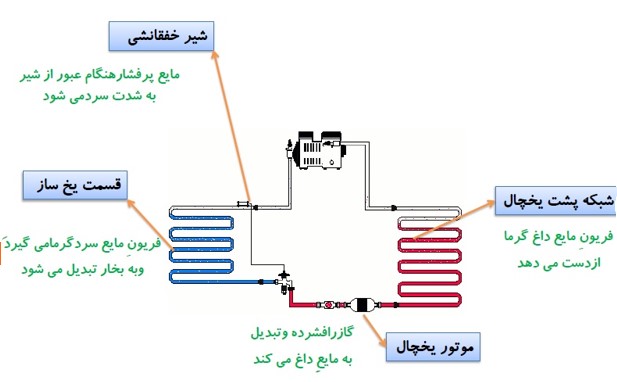
ساز و کار یخچال
اصول کار یخچال
این است که باید از جسمی که درون آن گذاشته ایم مقداری گرما بگیرد (\({Q_L}\) ) و سپس با انجام مقداری کار W (که همان موتور یخچال است) مقداری گرمای گرفته شده را به منبع با دمای بالا بدهد (\({Q_H}\) ).
طرز کار کولر گازی
مانند یخچال است. در کولر گازی منبع دما پایین هوای اتاق و منبع دمای بالا هوای بیرون است. کولر با انجام این کار، گرما را از داخل اتاق می گیرد و به هوای بیرون می دهد.
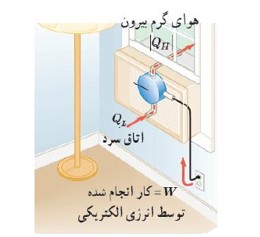
از نظر اقتصادی بهترین یخچال، یخچالی است که با انجام کار کمتر گرمای بیشتری را از درون یخچال به بیرون یخچال منتقل کند.
علامت کار و گرمای مبادله شده در یخچال
یخچال: نوعی ماشین گرمای است که در جهت وارون کار می کند.
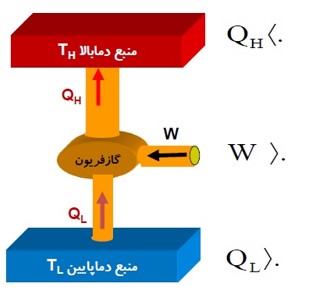
قانون اول ترمودینامیک برای یخچال
چون یخچال یک چرخه را تکرار می کند، در هر چرخه \(\Delta U = 0\) است، داریم:
\(\begin{array}{l}\Delta U = Q + W\\\Delta U = 0\\Q = {Q_L} - \left| {{Q_H}} \right|\\ \to 0 = {Q_L} - \left| {{Q_H}} \right| + W \to \left| {{Q_H}} \right| = {Q_L} + W\end{array}\)
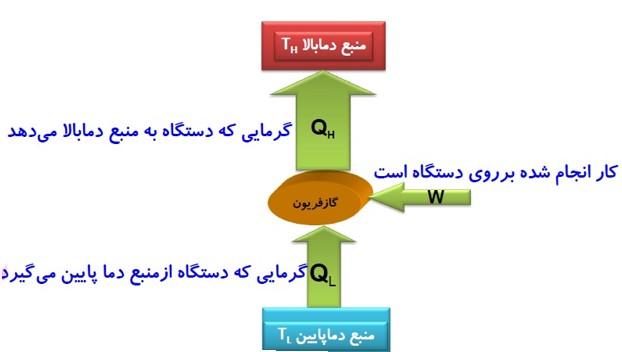
فرق ماشین گرمایی با یخچال
قانون های ترمودینامیک
به بیان ماشین گرمایی
قانون اول ترمودیناک: \({Q_H} = \left| {{Q_L}} \right| + \left| W \right|\)
قانون دوم ترمودینامیک: \({Q_L} \ne 0,\eta \ne 1\)
ممکن نیست دستگاه چرخه ای را بپیماید که در طی آن مقداری گرما را از منبع با دمای بالا جذب و تمام آن را به کار تبدیل کند.
به بیان یخچال
قانون اول ترمودینامیک: \({Q_H} = {Q_L} + W\)
قانون دوم ترمودینامیک: \(W \ne 0\)
ممکن نیست گرما به طور خود به خود از جسم با دمای پایین تر به جسم با دمای بالا تر منتقل شود.
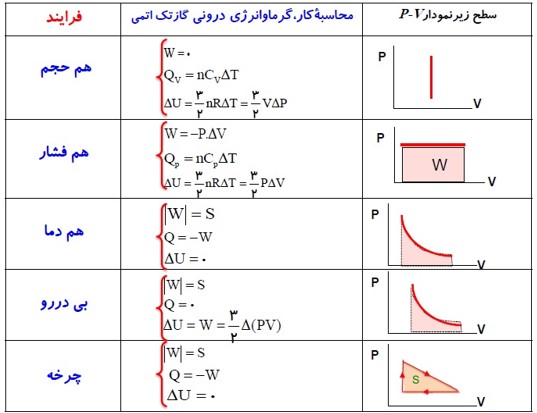



1736019749.png)