جواب با هم بیندیشیم صفحه 98 درس 4 شیمی دوازدهم (شیمی، راهی به سوی آینده ای روشن تر)
تعداد بازدید : 84.74Mپاسخ با هم بیندیشیم صفحه 98 شیمی دوازدهم
-گام به گام با هم بیندیشیم صفحه 98 درس شیمی، راهی به سوی آینده ای روشن تر
-با هم بیندیشیم صفحه 98 درس 4
-شما در حال مشاهده جواب با هم بیندیشیم صفحه 98 شیمی دوازدهم هستید. ما در تیم مای درس، پاسخنامههای کاملاً تشریحی و استاندارد را مطابق با آخرین تغییرات کتاب درسی 1404 برای شما گردآوری کردهایم. اگر به دنبال بهروزترین پاسخها برای این صفحه هستید و میخواهید بدون نیاز به اتصال به اینترنت، علاوه بر پاسخهای گام به گام، به گنجینهای از مطالب درسی دسترسی پیدا کنید، حتماً اپلیکیشن مایدرس را نصب نمایید.
📥 دانلود اپلیکیشن مایدرس
برای دسترسی آفلاین، سریع و بدون نیاز به اینترنت به گنجینهای از گامبهگامها و نمونه سوالات، اپلیکیشن را نصب کنید.
1- جدول زیر برخی داده ها برای واکنش میان گازهای هیدروژن و اکسیژن را در شرایط گوناگون نشان می دهد ، با توجه به آن به پرسش ها پاسخ دهید.
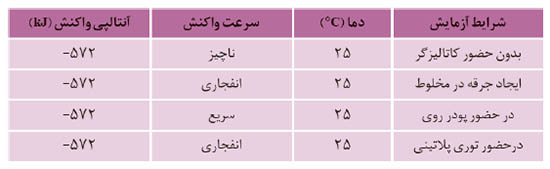
آ) توضیح دهید چرا این واکنش در دمای اتاق بدون حضور کاتالیزگر انجام نمی شود؟
ب) نقش جرقه در انجام واکنش چیست؟
پ) نقش پودر روی و توری پلاتینی در این واکنش چیست؟
ت) کدام کمیت برای این واکنش در هر شرایطی ثابت می ماند؟
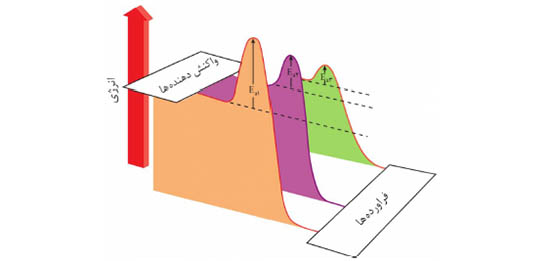
2- هر یک از نمودارها را به کدام شرایط واکنش می توان نسبت داد؟ توضیح دهید.
3- با خط زدن واژه نادرست در هر مورد، عبارت داده شده را کامل کنید.
کاتالیزگر در هر واکنش شیمیایی با (کاهش / افزایش) انرژی فعال سازی، سرعت واکنش را (کاهش / افزایش) میدهد، اما آنتالپی واکنش (ثابت میماند / افزایش مییابد).
1- آ) انجام واکنش میان گازهای هیدروژن و اکسیژن نیاز به انرژی فعالسازی زیادی دارد که دمای اتاق نمیتواند آن را تأمین کند.
ب) تأمین انرژی فعالسازی برای شروع واکنش
پ) هر دو به عنوان کاتالیزگر عمل کرده و سبب میشوند که واکنش در دمای پایین (دمای اتاق) انجام پذیر شود. به عبارت دیگر باعث میشوند تا انرژی فعالسازی کاهش یابد.
ت) آنتالپی واکنش
2- Ea1: واکنش با ایجاد جرقه، Ea2: واکنش با کاتالیزگر روی، Ea3: واکنش در حضور توری پلاتینی
کاتالیزگر با کاهش انرژی فعالسازی سبب افزایش سرعت واکنش میشود. از طرفی هرچه سطح تماس کاتالیز با واکنشدهنده را بیشتر کنیم سرعت واکنش نیز بیشتر میشود.
3- کاتالیزگر در هر واکنش شیمیایی با (کاهش) انرژی فعال سازی، سرعت واکنش را (افزایش) میدهد، اما آنتالپی واکنش (ثابت میماند)
مای درس ، برترین اپلیکیشن کمک درسی ایران
پوشش تمام محتواهای درسی پایه چهارم تا دوازدهم- آزمون آنلاین تمامی دروس
- گام به گام تمامی دروس
- ویدئو های آموزشی تمامی دروس
- گنجینه ای از جزوات و نمونه سوالات تمامی دروس
- فلش کارت های آماده دروس
- گنجینه ای جامع از انشاء های آماده
- آموزش جامع آرایه های ادبی، دستور زبان، قواعد زبان انگلیسی و ... ویژه



1736019749.png)















