جواب تمرین های دوره ای صفحه 48 درس 1 شیمی یازدهم (قدر هدایای زمینی را بدانیم)
تعداد بازدید : 84.73Mپاسخ تمرین های دوره ای صفحه 48 شیمی یازدهم
-گام به گام تمرین های دوره ای صفحه 48 درس قدر هدایای زمینی را بدانیم
-تمرین های دوره ای صفحه 48 درس 1
-شما در حال مشاهده جواب تمرین های دوره ای صفحه 48 شیمی یازدهم هستید. ما در تیم مای درس، پاسخنامههای کاملاً تشریحی و استاندارد را مطابق با آخرین تغییرات کتاب درسی 1404 برای شما گردآوری کردهایم. اگر به دنبال بهروزترین پاسخها برای این صفحه هستید و میخواهید بدون نیاز به اتصال به اینترنت، علاوه بر پاسخهای گام به گام، به گنجینهای از مطالب درسی دسترسی پیدا کنید، حتماً اپلیکیشن مایدرس را نصب نمایید.
📥 دانلود اپلیکیشن مایدرس
برای دسترسی آفلاین، سریع و بدون نیاز به اینترنت به گنجینهای از گامبهگامها و نمونه سوالات، اپلیکیشن را نصب کنید.
1) یون سولفات موجود در 2.45 گرم از نمونه ای كود شیمیایی را با استفاده از یون باریم، جداسازی كرده و 2.18 گرم باریم سولفات به دست آمده است. درصد خلوص كود شیمیایی را بر حسب یون سولفات حساب كنید.
2) از واكنش 8.1 گرم فلز آلومینیم با خلوص 90 درصد با محلول مس (II) سولفات مطابق واكنش زیر، چند گرم فلز مس آزاد می شود؟
2Al (s) + 2CuSO4 (aq) → 3Cu (s) + Al2(SO4)3 (aq)
3) سیلیسیم عنصر اصلی سازندۀ سلول های خورشیدی است كه از واكنش زیر تهیه می شود.
2SiO2 (s) + 2C(s) → Si (l) + 2Co (g)
الف) واكنش پذیری كربن را با سیلیسیم مقایسه كنید.
ب) مقدار ناخالصی در 100 گرم سیلیسیم مصرفی در صنایع الكترونیك 0.0001 گرم است. درصد خلوص آن را حساب كنید.
4) نمودار زیر روند كلی تغییر واكنش پذیری عنصرهای دورۀ دوم جدول دوره ای را نشان می دهد.

الف) چرا واكنش پذیری عنصرهای گروه 18 در حدود صفر است؟
ب) روند تغییر واكنش پذیری را توضیح دهید.
5) هر یك از هیدروكربن های زیر را به روش آیوپاک نام گذاری كنید.

6) با توجه به واكنش های زیر به پرسش های مطرح شده پاسخ دهید.
1- TiCl4 + Mg → Ti + MgCl2
2- Fe2O3 + Ti → Fe + TiO2
الف) هر یك از آنها را موازنه كنید.
ب) ترتیب واكنش پذیری عنصرهای Fe ، Mgو Tiرا مشخص كنید.
پ) برای تهیه فلز تیتانیم، باید واکنش شماره (١) را در حضور گاز آرگون انجام داد. چرا وجود گازهای اکسیژن و نیتروژن در محیط واکنش مانع از انجام واکنش می شود؟ (توجه: گاز نیتروژن به جو بی اثر معروف است)
ت) پیش بینی كنید آیا واكنش زیر در شرایط مناسب انجام می شود چرا؟ (درصورت انجام شدن واكنش را كامل و موازنه كنید.)
Mg + Fe2O3 → … + …
ث) تیتانیم فلزی محكم، با چگالی كم و مقاوم در برابر خوردگی است. یكی از كاربردهای آن استفاده در بدنه دوچرخه است. اگر در كارخانه ای از مصرف 7^10×3/54 گرم تیتانیم (IV) كلرید، 6^10×7/91 گرم فلز تیتانیم به دست آید، بازده درصدی واكنش را حساب كنید.
7) معدن مس سرچشمۀ كرمان، یكی از بزرگترین مجتمع های صنعتی معدنی جهان به شمار می رود و بزرگترین تولیدكنندۀ مس است. برای تهیۀ مس خام از سنگ معدن آن، واكنش زیر انجام می شود.
Cu2S + O2 → Cu + SO2 (موازنه نشده)
الف) با مصرف 400kg مس (I) سولفید با خلوص 85 درصد حدود 190/54kg مس خام تهیه می شود. بازده درصدی واكنش را حساب كنید.
ب) چرا این واكنش روی محیط زیست تأثیر زیان باری دارد؟
8) هگزان (C6H14) و 1- هگزن (C6H12) دو مایع بی رنگ هستند.
الف) روشی برای تشخیص این دو مایع پیشنهاد كنید.
ب) جای خالی را در واكنش زیر پر كنید.
C6H12 (l) + … → C6H14 (l)
9) هیدروکربنی به فرمول CxHy شناسایی شده است. افزودن چند قطره از آن به مقدار کمی از محلول برم در یک حلال آلی، سبب بی رنگ شدن محلول می شود.
الف) این هیدروکربن جزو آلکان ها، آلکن ها یا سیکلوآلکان هاست؟ چرا؟
ب) نسبت جرمی کربن به هیدروژن در آن برابر با ٦ و جرم مولی آن برابر با 140/2 گرم است. فرمول مولکولی آن را بیابید.
پ) با مراجعه به نمودار صفحه 36 ، حالت فیزیکی این هیدروکربن را پیش بینی کنید.
1) پاسخ به صورت زیر خواهد بود: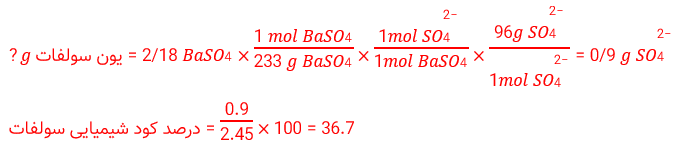
2)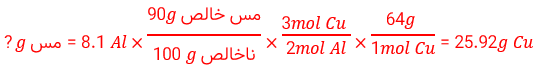
3) الف) واکنش پذیری کربن بیش تر از سیلیسیم است.
ب)
100 - 0.0001 = 99.9999 gSi
چون نمونه صد گرم است پس عدد به دست آمده همان درصد خلوص است.
4) الف) گازهای نجیب به دلیل داشتن لایه ظرفیت کامل تمایلی برای شرکت در واکنش ندارند
ب) در یک دوره واکنش پذیری فلزات کم و واکنش پذیری نافلزات زیاد می شود
5) الف) 2، 3، 4، 6-تترا متیل هپتان
ب) 3، 6-دی متیل اکتان
پ) 3-اتیل هپتان
ت) 2، 4-دی متیل هگزان
ث) 2، 4-دی متیل پنتان
ج) 2، 4، 5 – تری متیل هپتان
6) الف)
1- TiCl4 + 2Mg → Ti + 2MgCl2
2- 2Fe2O3 + 3Ti → 4Fe + 3TiO2
ب) Mg > Ti > Fe
پ) تیتانیوم (Ti) یک فلز بسیار واکنش پذیر است که تمایل زیادی به ترکیب شدن با اکسیژن و نیتروژن دارد؛ بنابراین هر زمان که در معرض هوا یا محیط های دیگر حاوی اکسیژن و نیتروژن باشد˓ یک سطح نازک از واکنش این عنصر با دو عنصر دیگر بر روی سطح آن تشکیل میشود که این لایه موجب افزایش مقاومت تیتانیوم در برابر خوردگی میگردد.
ت) واکنش انجام می شود زیرا واکنش پذیری منیزیم از آهن بیشتر است
Mg + Fe2O3 → 3MgO + 2Fe
ث)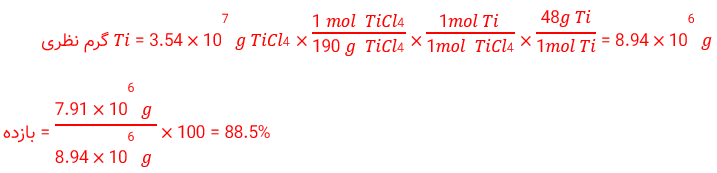 7) الف)
7) الف)
ب) زیرا گاز SO2 یک آلاینده است و تولید باران اسیدی نموده به محیط زیست آسیب می رساند
8) الف) هگزان یک آلکان و 1-هگزن یک آلکن با پیوند دو گانه است. لذا می توان از برم مایع استفاده نمود آلکن ها رنگ قرمز برم را بی رنگ می کند
ب)
C6H12 (l) + H2 (l) → C6H14 (l)
9) الف) با توجه به اینکه افزودن هیدروکربن به محلول برم سبب بی رنگ شدن محلول میشود، می توان نتیجه گرفت که هیدروکربن مورد نظر یک هیدروکربن سیر نشده است که در اینجا نوعی آلکن است. در واقع، آلکن ها بیشترین واکنش پذیری را دارند و با تمام حلالهای آلی قابل مخلوط شدن هستند و باعث بی رنگ شدن محلول برم می شوند.
ب) چون هیدروکربن مورد نظر نوعی آلکن است، بنابراین:
y=2x
در نتیجه داریم:
\(\begin{array}{l}{C_x}{H_y} = {C_x}{H_{2x}}\\\\\frac{{x.{m_C}}}{{2x.{m_H}}} = 6 \Rightarrow x.{m_C} = 12x.{m_H}\\\\x.{m_C} + 2x.{m_H} = 140/2 \Rightarrow 12x.{m_H} + 2x.{m_H} = 140/2\\\\14x.{m_H} = 140/2 \Rightarrow x = \frac{{140/2}}{{14{m_H}}} = \frac{{140/2}}{{14 \times 1/01}} \simeq 10\\\\ \Rightarrow {C_x}{H_y} = {C_{10}}{H_{20}}\end{array}\)
پ) این هیدروکربن مایع می باشد.
مای درس ، برترین اپلیکیشن کمک درسی ایران
پوشش تمام محتواهای درسی پایه چهارم تا دوازدهم- آزمون آنلاین تمامی دروس
- گام به گام تمامی دروس
- ویدئو های آموزشی تمامی دروس
- گنجینه ای از جزوات و نمونه سوالات تمامی دروس
- فلش کارت های آماده دروس
- گنجینه ای جامع از انشاء های آماده
- آموزش جامع آرایه های ادبی، دستور زبان، قواعد زبان انگلیسی و ... ویژه



1736019749.png)















