درسنامه کامل فیزیک دوازدهم تجربی فصل 4 آشنایی با فیزیک اتمی و هسته ای
تعداد بازدید : 7.59Mخلاصه نکات فیزیک دوازدهم تجربی فصل 4 آشنایی با فیزیک اتمی و هسته ای - درسنامه شب امتحان فیزیک دوازدهم تجربی فصل 4 آشنایی با فیزیک اتمی و هسته ای - جزوه شب امتحان فیزیک دوازدهم تجربی نوبت اول فصل 4 آشنایی با فیزیک اتمی و هسته ای
فوتو الکتریک
فوتو الکتریک
اثر فوتو الكتريک
وقتی نوری با بسامد مناسب مانند نور فرابنفش به سطحی فلزی بتابد الكترون هايی از آن گسيل می شوند. اين پديده را اثر فوتو الكتريک والكترون های جداشده از سطح فلز را فوتو الكترون می نامند.
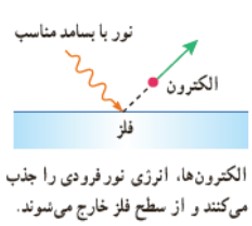
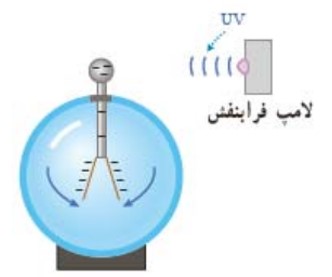
1 برهم كنش نور فرودی فرابنفش با كلاهک برق نما سبب می شود تا ورقه های آن به سرعت به هم نزديک شوند.
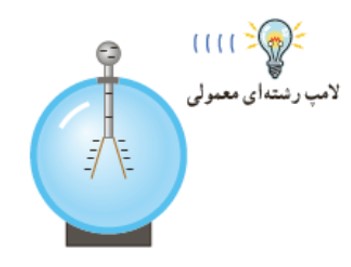
2 برهم كنش نور مرئی گسيل شده از يک لامپ رشته ای تغييری در انحراف ورقه های برق نما به وجود نمی آورد.
فوتون
حداقل انرژی موج الكترومغناطيس با يک بسامد معين فوتون ناميده می شود و انرژی آن برابر \(E = h{\textstyle{c \over \lambda }}\) یا \(E = hf\) است.
انرژی امواج الكترومغناطيس
انرژی امواج الكترومغناطيس مضرب صحيحی از انرژی يک فوتون (hf) است:
\(E = nhf\) یا \(E = nh{\textstyle{c \over \lambda }}\)
(n) تعداد فوتون ها
(h) ثابت پلانک (\(6/6 \times {10^{ - 34}}j.s\) )
(c) سرعت امواج الکترومغناطیس (\(3 \times {10^8}\frac{m}{s}\) )
E انرژی امواج الکترومغناطیس
الكترون-ولت
انرژی الكترون تحت ولتاژ يک ولت است و الكترون-ولت يكای غير SI انرژی در فيزيک اتمی و فيزيک هسته ای است. الكترون-ولت به صورت زير به ژول تبديل می شود:
\(1ev = 1/6 \times {10^{ - 19}}j\)
در رابطه های \(E = nhf\) اگر ثابت پلانک (h) بر حسب \(j.s\) باشد E بر حسب ژول (J) به دست می آید و در صورتی که ثابت پلانک (h) بر حسب \(ev.s\) باشد E بر حسب الکترون-ولت (ev) به دست می آیند.
بررسی اثر پديده ی فوتو الكتريک
برای بررسی اثر فوتوالكتريک دستگاهی به صورت زير طراحی می شود:
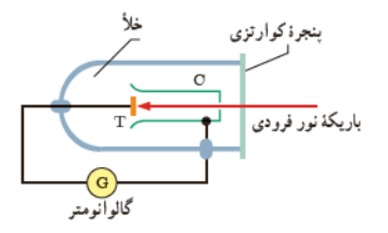
در اين دستگاه صفحه ی فلزی هدف T و جمع كننده ی فلزی C درون يک محفظه شيشه ای خلأ قرار دارند كه از بيرون به يک گالوانومتر (آمپرسنج حساس) متصل شده اند. نور تكفام (تک بسامد) كه بسامد آن به قدر كافی بالا است بر صفحه T فرود می آيد و فوتو الكترون ها را آزاد می كند. اين فوتو الكترون ها به جمع كننده ی C می رسند و در نتيجه گالوانومتر كه در مدار قرار دارد جريانی را آشكار می كند. در اين آزمايش به نكات زير بايد توجه كنيد:
1) با افزايش شدت اين نور چون تعداد فوتوالكترون های جدا شده افزايش می يابد، جريان بيشتر شده و گالوانومتر عدد بزرگتری را نشان می دهد .
2) اگر بسامد نور فرودی از مقدار معينی كم تر باشد، هر چه قدر هم كه شدت نور فرودی افزايش يابد پديده فوتو الكتريک رخ نمی دهد و گالوانومتر عبور جريانی را نشان نمی دهد.
تناقض های فيزيک كلاسيک با نتايج تجربی در پديده ی فوتو الكتريک
1) بر اساس ديدگاه فيزيک كلاسيک هنگام بر هم كنش موج الكترومغناطيسی (نور فرودی) با سطح فلز، ميدان الكتريكی اين موج، نيروی \(f = - eE\) به الكترون های فلز وارد می كند و آن ها را به نوسان در می آورد. به اين ترتيب، وقتی دامنه نوسان برخی از الكترون ها به قدر كافی بزرگ شود انرژی جنبشی لازم را برای جدا شدن از سطح فلز پيدا می كنند. بنابراين پديده ی فوتوالكتريک بايد در هر بسامدی رخ دهد در حالی كه اين نتيجه با تجربه سازگار نيست.
2) براساس نظريه ماكسول شدت نور با مربع دامنه ی ميدان الكتريكی موج الكترومغناطيسی متناسب است (\(I\alpha {E^2}\) )، به اين ترتيب انتظار می رود به ازای يک بسامد معين، اگر شدت نور فرودی بر سطح فلز را افزايش دهيم بايد الكترون ها با سرعت و انرژی جنبشی بيش تری از فلز خارج شوند، اما چنين نتيجه ای در تجربه مشاهده نمی گردد.
نظريه اينشتين در رابطه با پديده ی فوتوالكتريک
1) اينشتين با توجه به نظريه ی پلانک فرض كرد نور با بسامد f را می توان به صورت مجموعه ای از بسته های انرژی در نظر گرفت. هر بسته ی انرژی بعدها فوتون نام گرفت، انرژی هر فوتون از رابطه زير به دست می آيد:
\(\begin{array}{l}E = hf\\E = \frac{{hc}}{\lambda }\end{array}\)
(h) ثابت پلانک (\(6/6 \times {10^{ - 34}}j.s\) )
(f) بسامد (Hz)
(\(\lambda \)) طول موج (m)
(c) سرعت امواج الکترومغناطیس (\(3 \times {10^8}\frac{m}{s}\) )
E انرژی هر فوتون (J)
2) هر فوتون صرفاً با يک الكترون بر هم كنش دارد.
3) بسامدی كه در آن الكترون بدون هيچ انرژی جنبشی ای در آستانه ی ترک فلز است بسامد آستانه ناميده می شود و با \({f_0}\) نمايش داده می شود. (بسامد آستانه حداقل بسامد برای انجام پديده ی فوتوالكتريک است و در كم تر از آن پديده ی فوتوالكتريک انجام نمی شود)
4) طول موجی كه در آن الكترون بدون هيچ انرژی جنبشی ای در آستانه ی ترک فلز است طول موج آستانه ناميده می شود و با \({\lambda _0}\) نمايش داده می شود. (طول موج آستانه حداكثر طول موج برای انجام پديده ی فوتوالكتريک است و در بالاتر از آن پديده ی فوتوالكتريک انجام نمی شود)
5) انرژی لازم برای خارج كردن يک الكترون از سطح يک فلز تابع كار ناميده می شود و با \({W_0}\) نمايش داده می شود.
\(\begin{array}{l}{W_0} = h{f_0}\\{W_0} = \frac{{hc}}{{{\lambda _0}}}\end{array}\)
(h) ثابت پلانک (\(6/6 \times {10^{ - 34}}j.s\) )
(\({f_0}\)) بسامد (Hz)
(\({\lambda _0}\) ) طول موج (m)
(\({W_0}\) ) (J)
6) تابع کار (\({W_0}\) )، بسامد آستانه (\({f_0}\)) و طول موج آستانه (\({\lambda _0}\) ) هر سه به جنس فلز بستگی دارند.
7) اگر فوتون تابشی انرژی كافی داشته باشد، بخشی از انرژی صرف گسيل الكترون از فلز می شود و مابقی آن به انرژی جنبشی الكترون خارج شده تبديل می شود، انرژی جنبشی سريع ترين فوتوالكترون های گسيل شده از رابطه زير به دست می آيد:
\({K_{\max }} = hf - {W_0}\)
8) بيشينه انرژی جنبشی فوتو الكترون ها (\({K_{\max }}\) ) به بسامد نور فرودی و جنس فلز بستگی دارد.
نمودار بيشينه انرژی جنبشی فوتوالكترون ها بر حسب بسامد نور فرودی:
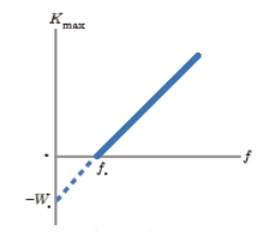
شیب نمودار : \(\tan \alpha = h\)
شرط انجام پديده فوتو الكتريک
اگر يكی از شرط های زير در پديده فوتو الكتريک برقرار باشد پديده فوتو الكتريک رخ می دهد و در غير اينصورت الكترونی از سطح فلز جدا نمی شود.
1) انرژی فوتون تابشی بيش تر از تابع كار باشد. (\(hf\rangle {W_0}\) )
2) بسامد نور فرودی بيش تر از بسامد آستانه باشد. (\(f\rangle {f_0}\) )
3) طول موج نور فرودی كم تر از طول آستانه باشد. (\(\lambda \rangle {\lambda _0}\) )
1 افزايش يا كاهش شدت نور فرودی تنها بر تعداد فوتون های تابشی و تعداد الكترون های جدا شده تأثير می گذارد و بر بيشينه انرژی جنبشی الكترون ها (\({K_{\max }}\) ) و بسامد آستانه (\({f_0}\)) بی تاثیر است.
2 در رابطه با بررسی ويژگی های نور هم مدل موجی و هم مدل ذره ای جايگاه خود را دارد به طور مثال بررسی پديده ی فوتو الكتريک با كمک مدل ذره ای و بررسی آزمايش يانگ با مدل موجی صورت می گيرد.
1شکل (1) بیانگر کدام پدیده در فیزیک جدید است؟
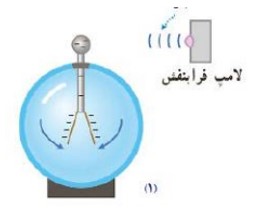
پدیده فوتوالکتریک
2در پدیده فوتوالکتریک، تابع کار یک فلز تحت تابش \(3/8ev\) است.
الف) طول موج آستانه برای گسیل فوتوالکترون ها از سطح این فلز چند نانو متر است؟ (\(hc = 1240ev.nm\) )
\(\frac{{hc}}{{{\lambda _0}}} = {W_0} \to {\lambda _0} = \frac{{hc}}{{{W_0}}} \approx 326/3nm\)
ب) اگر طول موج فرودی بر سطح این فلز \(155nm\) باشد، بیشینه انرژی جنبشی فوتوالکترون ها چقدر است؟
\({K_{\max }} = \frac{{hc}}{\lambda } - {W_0} \to {K_{\max }} = \frac{{1240}}{{155}} - 3/8 = 4/2ev\)
مای درس ، برترین اپلیکیشن کمک درسی ایران
پوشش تمام محتواهای درسی پایه تجربی- آزمون آنلاین تمامی دروس پایه تجربی
- گام به گام تمامی دروس پایه تجربی
- ویدئو های آموزشی تمامی دروس پایه تجربی
- گنجینه ای از جزوات و نمونه سوالات تمامی دروس پایه تجربی
- فلش کارت های آماده دروس پایه تجربی
- گنجینه ای جامع از انشاء های آماده پایه تجربی
- آموزش جامع آرایه های ادبی، دستور زبان، قواعد زبان انگلیسی و ... ویژه پایه تجربی
طیف
طیف
انواع طیف
1) طیف پیوسته (مانند طیف تابش گرمایی)
2) طیف گسسته
الف) طیف گسیلی
ب) طیف جذبی
1) طیف پیوسته
طيفی كه در آن بين طول موج های متوالی فاصله ای نباشد طيف پيوسته ناميده می شود.
2) طیف گسسته
طيفی كه در آن تمام طول موج های متوالی وجود نداشته باشد؛ ( بين آن ها فاصله وجود داشته باشد) طيف گسسته ناميده می شود. تصاوير زير مثال هايی از طيف گسسته را نشان می دهد:
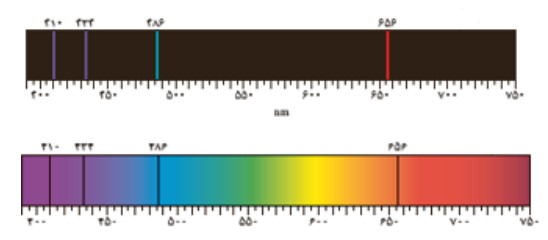
تابش گرمايی
اجسام در هر دمايی موج الكترومغناطيس گسيل (نشر) می كنند كه به آن تابش گرمايی گفته می شود.
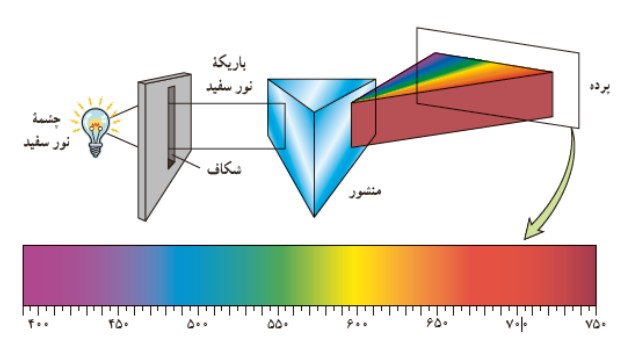
1 تابش گرمايی طيف گسيلی پيوسته محسوب می شود.
2 طول موج تابش گرمايی بستگی به دمای جسم دارد. به طور مثال اجسام در دماهای بالا از سطح خود نور مرئی گسيل می كنند (مانند آهن گداخته) و در دماهای معمولی اجسام در ناحيه ی فروسرخ تابش می كنند (مانند بدن انسان)
3 تشكيل طيف پيوسته توسط جسم جامد، ناشی از برهم كنش قوی بين اتم های سازنده ی آن است.
طيف گسيلی خطی (طيف خطی)
گازهای كم فشار و رقيق كه اتم های منفرد آن ها از برهم كنش های قوی موجود در جسم جامد آزادند به جای طيف پيوسته، طيفی گسسته را گسيل می كنند كه شامل طول موج های معينی است و به آن طيف خطی گفته می شود. (اين طيف زمينه ی تاريک و خطوط رنگی دارد)
نحوه توليد طيف خطی هيدروژن
برای ايجاد اين طيف از يک لامپ باريک و بلند شيشه ای كه حاوی مقداری گاز رقيق و كم فشار است استفاده می شود. دو الكترود به نام های آند و كاتد در دوطرف اين لامپ قرار دارد كه به ترتيب به پايانه های مثبت و منفی که منبع تغذيه با ولتاژ بالا وصل اند. اين ولتاژ بالا، سبب تخليه ی الكتريكی در گاز می شود و اتم های درون گاز درون لامپ شروع به گسيل نور می كنند. طيف خطی ايجاد شده و همچنين رنگ نور گسيل شده، به نوع گاز درون لامپ بستگی دارد. تصوير زير مربوط به توليد طيف خطی اتم هيدروژن است.
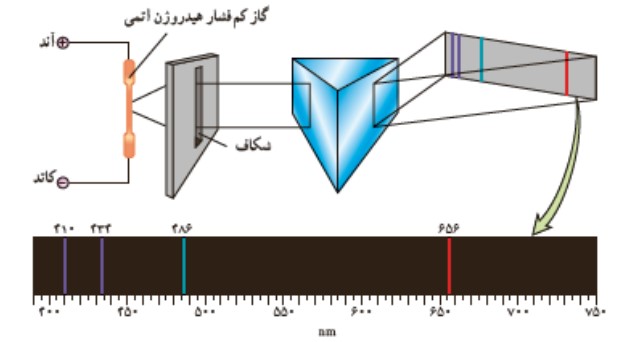
طيف جذبی
اگر نور سفيد از داخل گاز عنصری عبور كند و سپس طيف آن تشكيل شود، درآن طيف خط های تاريكی تشكيل می شود زيرا برخی طول موج های نور سفيد توسط گاز جذب شده و از طيف نور سفيد حذف می گردند. به اين طيف طيف جذبی گفته می شود. (اين طيف زمينه ی رنگی با خطوط تاريک دارد)
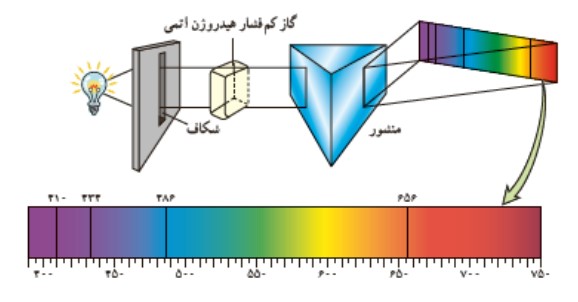
نحوه توليد طيف جذبی اتم هيدروژن
برای ايجاد اين طيف باريكه ی نور سفيد ابتدا از گاز كم فشار هيدروژن عبور می كند و سپس از منشور عبور داده می شود. اتم های هيدروژن در اين فرايند برخی طول موج های نور سفيد را جذب می كنند و به جای آن ها روی پرده خطوط تاريک مشاهده می شود.
1 طيف خطی برای اتم های هر گاز منحصر به فرد هستند و سرنخ های مهمی را درباره نوع و ساختار اتم های آن گاز می دهند.
2 طول موج های مرئی خاصی كه اتم های نئون و جيوه گسيل می كنند به تابلو های نئونی و لامپ های جيوه ای رنگ های مشخصی می دهند.
دو ويژگی مهم طيف های گسيلی و جذبی
- هم در طيف گسيلی و هم در طيف جذب اتم های گازی هر عنصر، طول موج های معينی وجود دارد كه از مشخصه های آن عنصر است. (يعنی طيف گسيلی و جذبی هيچ دو عنصری همانند يكديگر نيست و از اين ويژگی برای شناسايی عناصر استفاده می شود)
- اتم های هر گاز دقيقاً همان طول موج هايی را از نور سفيد جذب می كنند كه اگر دمای آن ها به اندازه ی كافی بالا رود يا به هر صورت ديگر برانگيخته شوند، آن ها را تابش می كنند.
خطوط فرانهوفر
طيف خورشيد يک طيف جذبی خطی گسسته است كه خط های نازک تاريكی در آن به علت جذب برخی طول موج ها توسط گازهای جو خورشيد و گازهای جو زمين ديده می شود كه به اين خطوط تاريک خطوط فرانهوفر گفته می شود.
معادله ی ريدبرگ-بالمر
يک رابطه رياضی به صورت زير است كه برای محاسبه ی طول موج های طيف خطی هيدروژن از آن استفاده می شود:
\(\frac{1}{\lambda } = R(\frac{1}{{{{n'}^2}}} - \frac{1}{{{n^2}}})\)
R ثابت ریدربرگ (\(n{m^{ - 1}}\) )
مقادیر n و \(n'\) با توجه به جدول رشته ی خط های طيفی گسيل هيدروژن از جدول زير تعيين می شود:
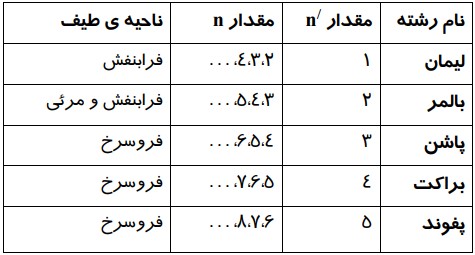
به طور مثال سومين خط رشته ی بالمر دارای \(n' = 2\) و \(n = 5\) است.
1 هرچه اختلاف n و \(n'\) بيش تر باشد، انرژی خط طيفی و بسامد آن بيش تر و طول موج آن كوتاه تر است.
2 با توجه به نكته قبل در يک رشته معين با \(n'\) مشخص، برای بلندترين طول موج كم ترين مقدار n كوتاه ترين طول موج بيش ترين مقدار n (یعنی \(\infty \)) قرار می دهيم. به طور مثال:

3 برای امواج الكترومغناطيس تابش شده توسط اتم هيدروژن، طول موج های 400 تا 700 نانومتر مرئی، كم تر از 400 نانو متر فرابنفش و بالاتر از 700 نانومتر فروسرخ است.
4 برای اتم هيدروژن منظور از حالت پايه وضعيتی است كه الكترون در لايه ی \(n = 1\) قرار دارد و منظور از حالت برانگيخته وضعيتی است كه الكترون در تراز بالاتر قرار گرفته باشد.
5 هنگامی كه اتمی يونش انجام می دهد فرض می شود الكترون به لايه ی \(n = \infty \) می رسد.
گستره طول موج های يک رشته
اختلاف كوتاه ترين و بلندترين طول موج در هر رشته را، گستره ی طول موج های آن رشته می نامند.
شکل زیر، طیف جذبی گازهای هیدروژن و جیوه را نشان می دهند:
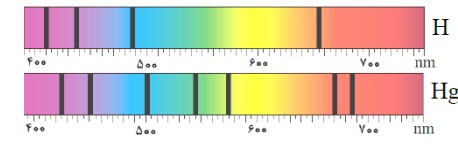
الف خط های تیره در زمینه طیف معرف چیست؟
معرف طول موج های جذب شده توسط اتم های گاز هستند.
ب از مقایسه این دو طیف چه نتیجه مهمی می گیریم؟
طیف گسیلی و جذبی هیچ دو گازی مانند هم نیست.
جزوات جامع پایه تجربی
جزوه جامع فیزیک دوازدهم تجربی فصل 1 حرکت بر خط راست
جزوه جامع فیزیک دوازدهم تجربی فصل 2 دینامیک
جزوه جامع فیزیک دوازدهم تجربی فصل 3 نوسان و امواج
جزوه جامع فیزیک دوازدهم تجربی فصل 4 آشنایی با فیزیک اتمی و هسته ای
مدل های اتمی
مدل های اتمی
مدل اتمی تامسون
بنابر مدل اتمی تامسون اتم همچون كره ای است كه بار مثبت به طور همگن در سرتاسر آن گسترده شده است و الكترون ها كه سهم ناچيزی در جرم اتم دارند در جاهای مختلف آن پراكنده شده اند. اين مدل را گاهی مدل كيک كشمشی هم می گويند.
ناسازگاری مدل تامسون با نتايج تجربی
مدل تامسون قادر به پيش بينی بسامدهای تابش گسيل شده از اتم نبود.
آزمايش پراكندگی رادرفورد
اين آزمايش باعث شد مدل اتمی تامسون كنار گذاشته شود. اين آزمايش به صورت زير انجام شد.
رادرفورد و همكارانش باريكه ای از ذره های دارای بارمثبت را (از جنس هسته ی هليم كه به آن ذرات آلفا گفته می شود) بر سطح ورقه ای نازک از جنس طلا تاباندند. رادرفورد بنابر مدل تامسون انتظار داشت كه تمامی ذره های آلفا، با انحراف بسيار اندكی از ورقه ی طلا عبور كنند. در عمل نيز بيش تر اين ذره ها بدون انحراف يا انحراف اندكی از ورقه ی طلا می گذشتند و در برخورد با صفحه ی فلوئورسان، در پشت آن، جرقه های نورانی توليد می كردند. با وجود اين، برخی از ذره های آلفا در هنگام خروج از ورقه ی نازک طلا، در زاويه های بزرگ منحرف و پراكنده می شدند و حتی تعدادی به عقب برمی گشتند. رادرفورد پس از انجام اين آزمايش و بر اساس مدل تامسون و شناختی كه از باريكه ی ذرات آلفا داشت، گفت: مثل آن بود كه گلوله ی توپی را به ورقه ی نازكی از كاغذ شليک كنيد و با شگفتی مشاهده كنيد كه پس از برخورد گلوله ی توپ با سطح كاغذ، گلوله بازگردد. اين ذره ها بايد چيز پر جرمی برخورد كرده باشد. رادرفورد استدلال كرد كه ذره های بدون انحراف بايد از قسمت هايی از ورقه گذشته باشند كه تهی بوده باشد، در حالی كه ذره های با انحراف شديد از مركزهايی بسيار چگال و دارای بار مثبت منحرف شده اند. وی سرانجام نتيجه گرفت بايد هسته ای چگال و دارای بار مثبت در مركز هر اتم باشد كه با مدل اتمی تامسون به طور آشكار مغايرت داشت.
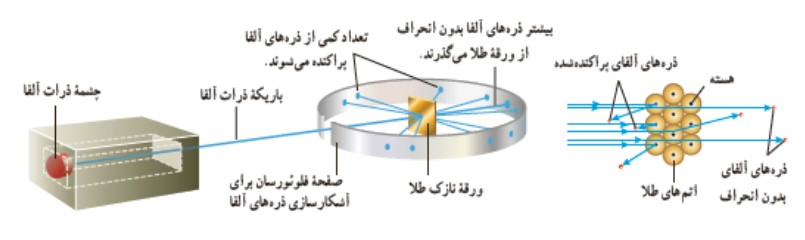
خلاصه مشاهدات و نتايج آزمايش پراكندگی رادفورد
پرتوهای 1و 2 انحرافی ندارند و يا انحراف اندک نشان می دهند اين موضوع نشان می دهد بيش تر فضای اتم خالی است. پرتوهای 3 انحراف بسيار زيادی داشته است كه نشان می دهد كه يک هسته ی كوچک و متراكم و پرجرم در مركز اتم وجود دارد.
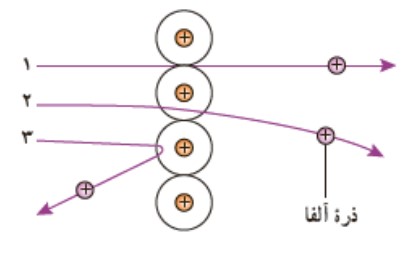
مدل اتمی هسته ای رادرفورد
مطابق اين مدل اتم دارای يک هسته ی بسيار چگال و كوچک و با بار مثبت است كه با تعدادی الكترون در فاصله هايی به نسبت دور احاطه شده است.
ناسازگاری های مدل اتمی رادرفورد با نتايج تجربی
1) عدم توجيه پايداری اتم
اگر الكترون ها را نسبت به هسته ساكن فرض كنيم، بايد تحت تأثير نيروی ربايشی الكتريكی بين هسته و الكترون، روی هسته سقوط كنند و در نتيجه اتم ناپايدار باشد، و اين با واقعيت سازگار نيست. همچنين اگر الكترون به دور هسته گردش داشته باشد باز هم اين حركت پايدار نمی ماند، زيرا حركت مداری الكترون به دور هسته، شتابدار است. بنابر فيزيک كلاسيک، اين حركت شتابدار الكترون سبب تابش امواج الكترومغناطيسی می شود. (زيرا در اينجا الكترون يک ذره ی باردار شتابدار است) كه بسامد آن با بسامد حركت مداری (دايره ای) الكترون برابر است. با تابش موج الكترومغناطيسی توسط الكترون، از انرژی آن كاسته می شود اين كاهش انرژی باعث می شود كه شعاع مدار الكترون به دور هسته به تدريج كوچک تر شده و در نهايت روی هسته فرو افتد. و بسامد حركت آن به تدريج بيش تر شود.
2) عدم توجيه طيف گسسته اتمی
با تابش موج الكترومغناطيسی توسط الكترون، از انرژی آن كاسته می شود و اين كاهش انرژی باعث می شود كه شعاع مدار الكترون به دور هسته به تدريج كوچک تر شده و بسامد تابش ها بيش ترگردد. اين افزايش تدريجی بسامد حركت مداری الكترون ها به اين معنی است كه طيف امواج الكترومغناطيسی گسيل شده بايد پيوسته باشد و اين مطلب نيز با واقعيت سازگار نيست.
مدل اتمی بور
بور توانست مسأله ی ناپايداری اتم در مدل رادرفورد را حل كند و توجيهی برای طيف خطی اتم هيدروژن در معادله ی ريدبرگ مطرح نمود. پيشنهاد بور اين بود كه (در مقياس اتمی، قوانين مكانيک كلاسيک و الكترومغناطيس بايد توسط قوانين ديگری جايگزين يا تكميل شود) مهمترين اصول بور برای اتم هيدروژن به شرح زير است:
1) مدارها و انرژی های الكترون در هر اتم كوانتيده اند، يعنی فقط مدارها و انرژی های گسسته ی معينی مجاز هستند. (يعنی الكترون در مدارهايی با شعاع های معين و ثابت در گردش است) شعاع و انرژی مدارهای هيدروژن به صورت زير به دست می آيد:
\(\begin{array}{l}{r_n} = {a_0}{n^2}\\{E_n} = \frac{{ - {E_R}}}{{{n^2}}}\end{array}\)
\({a_0}\) شعاع كوچک ترين مدار در اتم هيدروژن (\(5/29 \times {10^{ - 11}}m\) )
\({E_R}\) انرژی الكترون در اولين مدار (\(13/6ev\) )
(n) شماره ی مدار
\({r_n}\) شعاع مدار nام
\({E_n}\) انرژی مدار n ام (ev)
\({a_0}\) شعاع بور اتم هيدروژن، \({E_R}\) يک ريدبرگ و n عدد كوانتومی نيز ناميده می شود.
2) حالت مانا
وقتی الكترون در يكی از مدارهای مجاز است، هيچ نوع تابش الكترومغناطيسی گسيل نمی كند. از اين رو گفته می شود الكترون در مدار مانا يا حالت مانا قرار دارد. (اين مطلب برخلاف قوانين فيزيک كلاسيک است)
3) توجيه تابش گسسته ی اتم
الكترون می تواند از يک حالت مانا به حالت مانای ديگر برود. هنگام گذار الكترون از يک حالت مانا با انرژی بيش تر (\({E_U}\) ) به يک حالت مانا با انرژی كم تر (\({E_L}\) )، يک فوتون تابش می شود. در اين صورت انرژی فوتون تابش شده برابر اختلاف انرژی بين دو مدار اوليه و نهايی است. يعنی:
\({E_U} - {E_L} = hf\)
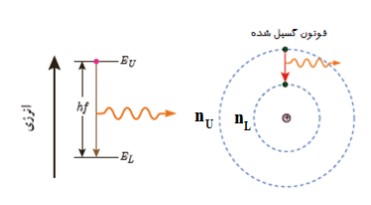
توجيه جذب به وسيله ی الگوی اتمی بور
هنگام گذار الكترون از یک حالت مانا با انرژی كم تر (\({E_L}\) ) به يک حالت مانا با انرژی بيش تر (\({E_U}\) )، يک فوتون تابش می شود. در اين صورت انرژی فوتون تابش شده برابر اختلاف انرژی بين دو مدار اوليه و نهايی است. يعنی:
\({E_U} - {E_L} = hf\)
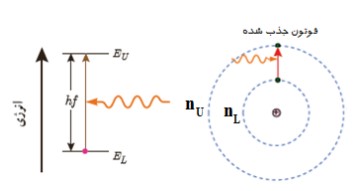
نمودار ترازهای انرژی الكترون برای اتم هيدروژن
1) هرچه از هسته دورتر می شويم انرژی الكترون بيش تر می شود.
2) بالاترين تراز انرژی به \(n = \infty \) مربوط است و در اين لايه، انرژی الكترون ev است. بنابراين انرژی لايه های پايين تر منفی است.
3) پايين ترين تراز انرژی حالت پايه ناميده می شود و انرژی الكترون در ترازهای بالا تر حالت برانگيخته ناميده می شود.
4) هرچه از هسته دورتر می شويم فاصله ی بين لايه های الكترونی كم تر می شود.
5) برای بالا بردن الكترون از حالت پايه (\(n = 1\) ) به بالاترين حالت برانگيخته ممكن (\(n = \infty \)) مقدار \(13/6ev\) انرژی بايد صرف شود. صرف اين مقدار انرژی، الكترون را از اتم خارج می كند. اين كم ترين انرژی لازم برای خارج كردن الكترون از حالت پايه، انرژی يونشالكترون ناميده می شود.
با تلفيق رابطه ی ريدبرگ و رابطه ی بور می توان ثابت كرد:
\(R = \frac{{{E_R}}}{{{h_c}}}\)
اتم هيدروژن گونه
به اتم هايی گفته می شود كه تنها يک الكترون دارند و مدل بور می تواند انرژی يونش و طول موج های طيف خطيی آن ها را با موفقيت پيش بينی كند. (به طور مثال ليتيم سه الكترون دارد و دارای يک الكترون است و اتم هيدروژن گونه محسوب می شود)
نارسايی های مدل اتمی بور
- اين مدل برای وقتی كه بيش از يک الكترون به دور هسته می گردد به كار نمی رود، زيرا در مدل بور، نيروی الكتريكی كه يک الكترون به الكترون ديگر وارد می كند در محاسبات در نظر گرفته نشده است.
- اين مدل نمی تواند متفاوت بودن شدت خط های طيفی گسيلی را توضيح دهد. (برای مثال مدل بور نمی تواند توضيح دهد چرا شدت خط قرمز با شدت خط آبی در طيف گسيلی گاز هيدروژن اتمی با يكديگر متفاوت است)
پديده فلوئورسانی
وقتی نور فرابنفش به بسياری از مواد تابيده شود، تابش مرئی از خود گسيل می كنند. طول موج های گسيل يافته معمولاً برابر همان طول موج نور فرودی يا بزرگ تر از آن است، زيرا الكترون ها با جذب انرژی تابش فرابنفش به لايه های بالاتر می رسند و در بازگشت ممكن است برخی الكترون ها به صورت پلكانی سقوط كنند (يعنی به طور مستقيم به حالت پايه برگشت نمی كنند) و از آنجا كه انرژی فوتون گسيل شده برابر اختلاف انرژی دو لايه ای است كه در آن گذار الكترون رخ داده، فوتون های با انرژی پايين تر و طول موج بلندتر گسيل می شود.
1اتم هیدروژن در حالت برانگیخته \(n = 3\) قرار دارد. کوتاه ترین طول موج تابشی آن چند نانو متر است؟ (\(R = 0/01n{m^{ - 1}}\) )
\(\frac{1}{\lambda } = R(\frac{1}{{{{n'}^2}}} - \frac{1}{{{n^2}}}) \to \frac{1}{\lambda } = \frac{1}{{100}}(\frac{1}{1} - \frac{1}{9}) \to \frac{1}{\lambda } = \frac{1}{{100}}(\frac{8}{9})\)
هر چه اختلاف انرژی دو تراز بیشتر باشد، طول موج گسیلی کوتاه تر است؛ لذا گذار از 3 به 1 است.
2کوتاه ترین طول موج رشته پاشن (\(n' = 3\) ) در اتم هیدروژن را بدست آورید. (\(R = 0/01n{m^{ - 1}}\) )
\(\frac{1}{\lambda } = R(\frac{1}{{{{n'}^2}}} - \frac{1}{{{n^2}}}) \to \frac{1}{\lambda } = \frac{1}{{100}}(\frac{1}{9} - 0) \to \lambda = 900nm\)
گسیل فوتون
گسیل فوتون
انواع روش های گسيل فوتون
1) گسيل خود به خود
وقتی الكترونی در تراز برانگيخته قرار داشته باشد با گسيل فوتون كاتوره ای به تراز پايين تر جهش می كند كه به آن گسيل خود به خود گفته می شود.
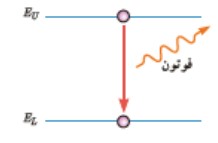
2) گسيل القايی
در اين نوع گسيل، يک فوتون ورودی، الكترون برانگيخته را تحريک يا (القا) می كند تا تراز انرژی خود را تغيير دهد و به تراز پايين تر برود و فوتونی هم سو با فوتون ورودی گسيل می كند.
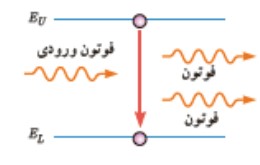
در گسيل خود به خود، گسيل القايی و جذب، انرژی فوتون هايی كه مبادله می شود همواره برابر اختلاف انرژی دو ترازی است كه در آن گذار الكترون اتفاق می افتد.
ويژگی های گسيل القايی
- از آنجا كه يک فوتون وارد و دو فوتون خارج می شود، تعداد فوتون ها را افزايش می دهد و نور را تقويت می كند.
- فوتون گسيل شده در همان جهت فوتون ورودی حركت می كند.
- فوتون گسيل شده با فوتون ورودی همگام يا هم فاز است.
لیزر (Laser): ليزر برگرفته از سرواژه های عبارت زير است:
Light Amplification by Stimulated Emission of Radiation
ليزر، تقويت نور به وسيله ی گسيل القايی تابش است. به عبارت ديگر اگر گسيل القايی را در مجموعه ی زيادی از اتم های برانگيخته انجام دهيم تعداد زيادی فوتون همسو، هم بسامد و هم انرژی ايجاد می شود كه باريكه ای از نور تقويت شده است.
وارونی جمعيت
در گسيل القايی يک چشمه ی خارجی مناسب بايد وجود داشته باشد تا الكترون ها را به ترازهای انرژی بالاتر برانگيخته كند. اين انرژی به روش های متعددی از جمله درخش های شديد نور معمولی يا تخليه های ولتاژ بالا فراهم می شود. اگر انرژی كافی به اتم ها داده شود، الكترون های بيش تری به تراز بالاتر برانگيخته خواهند شد. چنين شرطی وارونی جمعيت ناميده می شود:
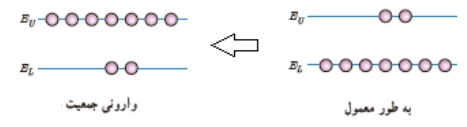
ترازهای شبه پايدار
در وارونی جمعيت الكترون ها در يک محيط ليزری بايد تعداد الكترون ها در ترازهايی موسوم به ترازهای شبه پايدار نسبت به تراز پايين تر بيش تر باشد. در اين ترازها الكترون ها در مدت زمان بسيار طولانی تری (\({10^{ - 3}}s\) ) نسبت به حالت برانگيخته ی معمولی (\({10^{ - 8}}s\) ) باقی می مانند. اين زمان طولانی تر، فرصت بيش تری برای افزايش وارونی جمعيت و در نتيجه تقويت نور ليزر فراهم می كند.
تفاوت های ليزر با نور معمولی
- بسامد و انرژی فوتون های ليزر كاملاً خالص است. يعنی در باريكه ی ليزر فقط يک نوع فوتون مشاهده می شود اما در نور معمولی اغلب طيف وسيعی از بسامدها وجود دارد.
- ليزر به خط راست منتشر می شود اما نور معمولی واگرايی دارد.
به سوالات زیر در مبحث فیزیک اتمی پاسخ دهید.
الف در اتم هیدروژن اگر الکترون از مدار \(n = 4\) به مدار \(n' = 3\) برود، طول موج گسیلی در کدام ناحیه از طیف امواج الکترومغناطیسی قرار دارد؟
فروسرخ
ب فوتون هایی که بر اثر فرآیند گسیل القایی به تراز پایین تر می روند، چه ویژگی های مشترکی دارند؟
هم بسامد، هم جهت و هم فاز
مای درس ، برترین اپلیکیشن کمک درسی ایران
پوشش تمام محتواهای درسی پایه تجربی- آزمون آنلاین تمامی دروس پایه تجربی
- گام به گام تمامی دروس پایه تجربی
- ویدئو های آموزشی تمامی دروس پایه تجربی
- گنجینه ای از جزوات و نمونه سوالات تمامی دروس پایه تجربی
- فلش کارت های آماده دروس پایه تجربی
- گنجینه ای جامع از انشاء های آماده پایه تجربی
- آموزش جامع آرایه های ادبی، دستور زبان، قواعد زبان انگلیسی و ... ویژه پایه تجربی
فیزیک هسته ای
فیزیک هسته ای
شاخه ای از فيزيک است كه در آن با ساختار، بر هم كنش ها و واپاشی هسته های اتمی سرو كار داريم.
نوكلئون
به ذرات تشكيل دهنده ی هسته كه شامل پروتون ها و نوترون ها می باشند نوكلئون گفته می شود.
عدد اتمی (Z)
تعدا پروتون های هسته را عدد اتمی می نامند.
عدد نوترونی (N)
تعداد نوترون های هسته را عدد نوترونی آن می گويند.
عدد جرمی (A)
مجموع تعداد پروتون ها و نوترون های را عدد جرمی ناميده می شود.
\(A = Z + N\)
در يک عنصر خنثی تعداد پروتون ها و الكترون ها برابر است
نماد شيميايی عنصرها
برای يک عنصر با نماد شيميايی X ، نماد هسته به صورت زير نشان داده می شود:
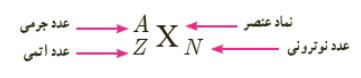
ايزوتوپ ها(هم مكان)
شكل های مختلف يک عنصر كه عدد اتمی يكسان وعدد جرمی متفاوت دارند.
1 ايزوتوپ ها تعداد پروتون های برابر و تعداد نوترون های متفاوت دارند.
2 ايزوتوپ های خواص شيميايی يكسان اما خواص فيزيكی تفاوت دارند.
ايزوتوپ های هيدروژن
هيدروژن دارای سه ايزوتوپ طبيعی است:
هیدروژن \({}_1^1H\) ، \({}_1^2D\) یا دوتریوم و \({}_1^3T\)
ابعاد هسته در مقايسه با ابعاد اتم بسيار كوچک تر است. با اين وجود \(99/9\) درصد جرم اتم در هسته متمركز شده است. (چگالی هسته \({10^{14}}\frac{g}{{c{m^3}}}\) )
جزوات جامع پایه تجربی
جزوه جامع فیزیک دوازدهم تجربی فصل 1 حرکت بر خط راست
جزوه جامع فیزیک دوازدهم تجربی فصل 2 دینامیک
جزوه جامع فیزیک دوازدهم تجربی فصل 3 نوسان و امواج
جزوه جامع فیزیک دوازدهم تجربی فصل 4 آشنایی با فیزیک اتمی و هسته ای
نيروی هسته ای
نيروی هسته ای
نيروی جاذبه بين نوكلئون های هسته كه باعث می شود نوكلئون ها به صورت پايدار در كنار هم باقی بمانند نيروی هسته ای ناميده می شود.
1 نيروی هسته ای بسيار قوی تر از نيروی رانش الكتريكی بين دو پروتون است.
2 نيروی هسته ای با نيروی گرانشی بسيار تفاوت دارد زيرا جاذبه نيروی گرانشی بين نوكلئون ها چنان ضعيف است كه نمی تواند بر نيروی دافعه ی الكتروستاتيكی دو پروتون غلبه كند.
3 نيروی هسته ای كوتاه برد است و تنها در فاصله ای كوچک تر از ابعاد هسته اثر می كند.
4 نيروی هسته ای مستقل از بار الكتريكی است، يعنی نيروی ربايشی هسته ای يكسانی بين دو پروتون، دو نوترون، يا يک پروتون و يک نوترون وجود دارد. (به همين دليل از منظر نيروی هسته ای، تفاوتی بين پروتون و نوترون وجود ندارد و دليل نامگذاری آن ها با نام عام نوكلئون نيز همين است)
شرط پايداری هسته
براي پايداری هسته، بايد نيروی دافعه ی الكتروستاتيكی بين پروتون ها با نيروی جاذبه ی بين نوكلئون ها، كه ناشی از نيروی هسته ای است برابر باشد. ولی به دليل بلند برد بودن نيروی الكتروستاتيكی، يک پروتون تمام پروتون های ديگر درون هسته را دفع می كند، در حالی كه يک پروتون يا يک نوترون فقط نزديک ترين نوكلئون های مجاور خود را با نيروی هسته ای جذب می كند. به همين دليل وقتی تعداد پروتون های درون هسته افزايش يابد، اگر هسته بخواهد پايدار بماند، بايد تعداد نوترون های درون هسته نيز افزايش يابد. شكل زير نموداری از Z بر حسب N را برای عنصرهای مختلف نشان می دهد.
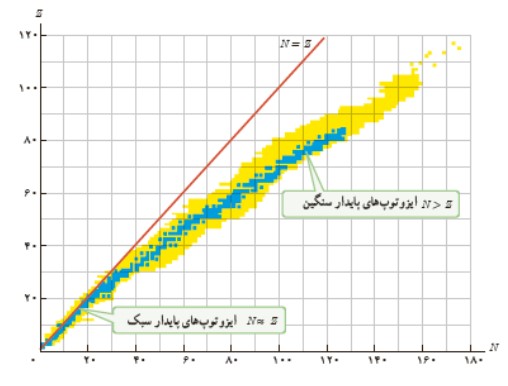
هسته ی پايدار با بيش ترين تعداد پروتون (\(Z = 83\) ) متعلق به بيسوت است. به جز توريم و اورانيوم كه در طبيعت يافت می شوند ساير هسته های سنگين با عدد اتمی بزرگتر از 83 ناپايدارند. اين دو عنصر تنها عنصرهايی اند كه واپاشی آن چنان كند است كه از هنگام تشكيل منظومه ی شمسی، فقط مقدار كمی از آن ها بر اثر واپاشی به عنصرهای سبک تر تبديل شده اند.
برای هسته های پايدار نسبت نوترون به پروتون (\(\frac{N}{Z}\) ) برابر \(1/5\) یا بیش تر است.
انرژی بستگی هسته ای
انرژی لازم برای جدا كردن نوكلئون های هسته انرژی بستگی هسته ای ناميده می شود.
كاستی جرم هسته
جرم هسته از مجموع جرم پروتون ها و نوترون های تشكيل دهنده كم تر است. اين اختلاف جرم كاستی جرم هسته ناميده می شود.
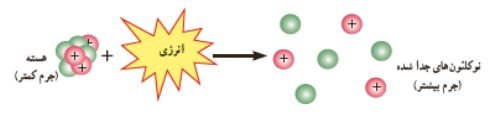
محاسبه ی انرژی بستگی هسته ای
برای به دست آوردن اين انرژی بايد از رابطه معروف اينيشتين در نظريه نسبيت استفاده نمود؛ (البته اين محاسبه خارج از برنامه ی كتاب درسی است)
\(E = m{c^2}\)
ترازهای انرژی هسته
انرژی نوكلئون های وابسته به هسته نيز مانند انرژی الكترون های وابسته به اتم كوانتيده اند و نوكلئون ها درون هسته نمی توانند هر انرژی دلخواهی را اختيار كنند. همچنين همان طور كه الكترون های اتم می توانند با جذب انرژی از تراز پايه به تراز برانگيخته بروند، نوكلئون ها نيز می توانند با جذب انرژی به ترازهای انرژی بالاتر بروند و درنتيجه هسته برانگيخته شود. هسته ی برانگيخته با گسيل فوتون به به تراز پايه بر می گردد. انرژی فوتون گسيل شده، با اختلاف انرژی بين دو تراز برانگيخته و تراز پايه برابر است.
(هسته های برانگيخته را با نماد \({X^ + }\) نمايش می دهند)
تفاوت ترازهای انرژی نوكلئون ها با ترازهای انرژی الكترون
اختلاف بين ترازهای انرژی نوكلئون ها در هسته از مرتبه ی keV تا مرتبه ی MeV است، در حالی كه اختلاف بين ترازهای انرژی الكترون ها در اتم از مرتبه ی ev است. از اين رو، هسته ها در واكنش های شيميايی برانگيخته نمی شود.
1دو ویژگی نیروهای هسته ای را بنویسید.
کوتاه برد، بسیار قوی
2غنی سازی اورانیوم به چه معناست؟
افزایش درصد یا غلظت ایزوتوپ 235 در یک نمونه را می گویند.
پرتوزايی
پرتوزايی
پرتوزايی طبيعی
وقتی يک هسته ی ناپايدار يا پرتوزا به طور طبيعی (خود به خود) واپاشی می كند، نوع معينی از ذرات يا فوتون های پر انرژی آزاد می شوند. اين فرايند واپاشی، پرتوزايی طبيعی ناميده می شود.
انواع پرتوها در پرتوزايی طبيعی و قدرت نفوذ آن ها
در پرتوزايی طبيعی سه نوع پرتو ايجاد می شود:
1) پرتو های آلفا (\(\alpha \))
كم ترين نفوذ را دارند و با ورقه ی نازک سربی با ضخامت ناچيز متوقف می شوند. (حدود \(0/01mm\) در سرب نفوذ دارند)
2) پرتو های بتا (\(\beta \))
اين پرتوها مسافت خيلی بيش تری در سرب نفوذ می كنند. (حدود \(0/1mm\) )
3) پرتو های گاما (\(\gamma \))
اين پرتوها بيش ترين نفوذ را در سرب دارند (حدود \(100mm\) )
تعداد نوكلئون ها در تمام فرايندهای واپاشی هسته ای پايسته است. يعنی تعداد نوكلئون ها، پيش از فرايند با تعداد نوكلئون ها پس از فرآيند مساوی است .
آزمايش مقايسه ی بار و جرم سه نوع ذره ی پرتوزا
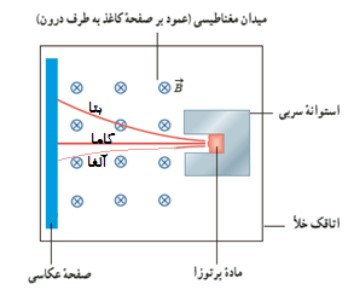
برای انجام اين آزمايش نمونه ی ماده ی پرتوزا داخل استوانه ای سربی قرار می گيرد و پرتوهای آن عمود بر يک ميدان مغناطيسی عبور می كنند كه با توجه به قاعده ی دست راست می توان نوع بارالكتريكی هر ذره را تعيين كرد:
- پرتو ی گاما در ميدان مغناطيسی انحراف ندارد كه نشان می دهد بار الكتريكی ندارد.
- پرتو ی بتا به گونه ای در ميدان مغناطيسی انحراف پيدا کرده است كه نشان می دهد دارای بار الكتريكی منفی است و چون بيش ترين انحراف را دارد نشان می دهد كم ترين جرم را در مقايسه با ساير ذرات واپاشی دارد.
- پرتو ی آلفا به گونه ای در ميدان مغناطيسی انحراف پيدا كرده است كه نشان می دهد دارای بار الكتريكی مثبت است و چون كم ترين انحراف را دارد نشان می دهد بيش ترين جرم را در مقايسه با ساير ذرات واپاشی دارد.
واكنش هسته ای مربوط به واپاشی آلفا (\(\alpha \))
اين نوع پرتوها ذرات با بار مثبت از جنس هسته ی هليم (\({}_2^4He\) ) است، يعنی از دو پروتون و دو نوترون تشكيل شده است. معادله ی اين واپاشی به اين صورت زير است:
\({}_Z^AX \to {}_{Z - 2}^{A - 4}Y + {}_4^2He\)
در اين رابطه X هسته ي مادر و Y هسته ی دختر ناميده می شود.
واكنش هسته ای مربوط به واپاشی بتا (\(\beta \)) اين واپاشی به دوشكل صورت می گيرد.
1) بتای منفی
اين پرتوها از نوع الكترون هستند. الكترون واپاشی شده در هسته ی مادر وجود ندارد و همچنين يكی از الكترون های مداری اتم نيست. اين الكترون وقتی به وجود می آيد كه نوترونی درون هسته، به پروتون و الكترون تبديل شود. معادله ی اين واپاشی به صورت زير است.
\({}_Z^AX \to {}_{Z + 1}^AY + {}_{ - 1}^0{e^ - }\)
در اين رابطه X هسته ی مادر و Y هسته ی دختر ناميده می شود.
2) پوزيترون
اين پرتوها جرم يكسان با الكترون دارند اما به جای بار \( - e\) حامل بار \( + e\) هستند. به اين الكترون مثبت پوزيترون گفته می شود. در اين فرايند يكی از پروتون های درون هسته به يک نوترون و پوزيترون تبديل می شود سپس اين پوزيترون از هسته گسيل می شود. معادله ی اين واپاشی به صورت زير است:
\({}_Z^AX \to {}_{Z - 1}^AY + {}_1^0{e^ + }\)
در اين رابطه X هسته ی مادر و Y هسته ی دختر ناميده می شود.
واكنش هسته ای مربوط به واپاشی گاما (\(\gamma \))
پرتوی گاما يک فوتون پر انرژی است. اغلب هسته ها پس از واپاشی آلفا يا بتا، در حالت برانگيخته قرار می گيرند و با گسيل فوتون های پرانرژی گاما به حالت پايه می رسند. در اين فرايند A و Z تغيير نمی كنند. معادله ی اين واپاشی به صورت زير است:
\({}_Z^A{X^ + } \to {}_Z^AX + \gamma \)
در اين رابطه \({X^ + }\) هسته ی مادر و X هسته ی دختر ناميده می شود.
ذره های آلفا سنگين اند و برد كوتاهی دارند. اين ذرات پس از طی مسافت كوتاهی در هوا ( 1 تا 2 سانتی متر) و يا با عبور از لايه ای نازک از مواد جذب می شوند. اگر اين ذره ها از راه تنفس يا دستگاه گوارش وارد بدن شوند، باعث آسيب شديد به بافت های بدن می شوند.
نیمه عمر (\({T_{1/2}}\) )
نيمه عمر مدت زمانی است كه طول می كشد تا تعداد هسته های مادر موجود در يک نمونه به نصف برسند.
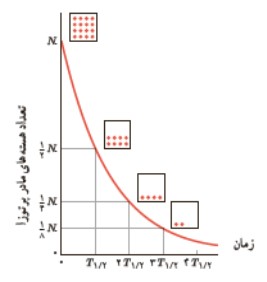
محاسبات جرمی ماده ی پرتوزا با توجه به نيمه عمر آن:
\(\begin{array}{l}n = \frac{t}{{{T_{\frac{1}{2}}}}}\\m = \frac{{{m_0}}}{{{2^n}}}\\{m_0} - m = {m_0}(1 - \frac{1}{{{2^n}}})\end{array}\)
\({T_{1/2}}\) نیمه عمر
(t) كل زمان لازم برای واپاشی ( مدت تجزيه)
(n) تعداد نيمه عمرهای سپری شده
\({m_0}\) مقدار اوليه ی ماده ی پرتوزا
(m) مقدار باقی مانده ی ماده ی پرتوزا (مقدار فعال)
\({m_0} - m\) مقدار واپاشی شده يا تجزيه شده (غير فعال)
به جای جرم در كليه ی روابط بالا می توان تعداد هسته های ماده پرتوزا (N) را قرار داد.
1عنصر (\({}_{92}^{238}U\) ) با گسیل دو ذره الکترون واپاشی می کند. معادله این واکنش را بنویسید.
\({}_{92}^{238}U \to {}_{94}^{238}Y + 2({}_{ - 1}^0{e^ - })\)
2از یک ماده رادیواکتیو پس از گذشت 135 روز، \(\frac{7}{8}\) ماده فعال اولیه، واپاشیده شده است. نیمه عمر این ماده چند روز است؟
\(\begin{array}{l}N = \frac{{{N_0}}}{{{2^n}}} \to \frac{1}{8}{N_0} = \frac{1}{{{2^3}}}{N_0} \to n = 3\\n = \frac{t}{T} \to 3 = \frac{{135}}{T} \to T = 45Day\end{array}\)
3نیمه عمر یک ماده رادیو اکتیو 14 ساعت است. پس از گذشت 56 ساعت، چه کسری از هسته های فعال آن، باقی مانده اند؟
\(\begin{array}{l}n = \frac{t}{T} \to n = \frac{{56}}{{14}} \to n = 4\\N = \frac{{{N_0}}}{{{2^n}}} \to N = \frac{{{N_0}}}{{{2^4}}} \to \frac{1}{{16}}{N_0}\end{array}\)
مای درس ، برترین اپلیکیشن کمک درسی ایران
پوشش تمام محتواهای درسی پایه تجربی- آزمون آنلاین تمامی دروس پایه تجربی
- گام به گام تمامی دروس پایه تجربی
- ویدئو های آموزشی تمامی دروس پایه تجربی
- گنجینه ای از جزوات و نمونه سوالات تمامی دروس پایه تجربی
- فلش کارت های آماده دروس پایه تجربی
- گنجینه ای جامع از انشاء های آماده پایه تجربی
- آموزش جامع آرایه های ادبی، دستور زبان، قواعد زبان انگلیسی و ... ویژه پایه تجربی
شکافت هسته ای
شکافت هسته ای
فرايند تقسيم شدن يک هسته ی سنگين به دو هسته با جرم كم تر، شكافت هسته ای ناميده می شود.
شكافت هسته ی اورانيوم
اورانيوم 235 (\({}_{92}^{235}U\) ) پس از جذب نوترون به دو تكه تقسيم می شود و هر تكه، جرم كم تری از هسته ی اوليه دارد. در فرايند شكافت اورانيوم، تركيب های متفاوتی از هسته های كوچک تر همراه با تعدادی نوترون (بین 2 تا 5) به وجود می آید.
وقتی نوترونی با هسته ی اورانيوم 235 برخورد كند و جذب شود، هسته ی اورانيوم شروع به ارتعاش می كند و تغيير شكل می دهد. ارتعاش تا وقتی ادامه می يابد كه تغيير شكل چنان جدی شود كه نيروی جاذبه ی هسته ای ديگر نتواند با نيروی دافعه ی الكتروستاتيكی بين پروتون های هسته متوازن شود. در اين هنگام، هسته به پاره هايی وا می پاشد كه حامل انرژی (به طور عمده انرژی جنبشی) هستند.
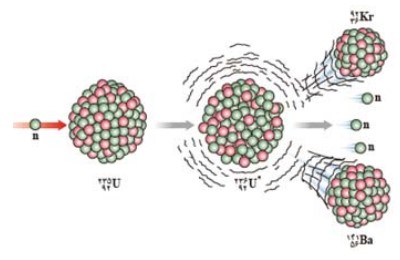
واکنش زنجیره ای
فرايند شكافت اورانيوم 235 با جذب يک نوترون كند آغاز می شود. اگر محصولات شكافت Ba و Kr باشند در اين فرايند 3 نوترون به وجود می آيد. چون نوترون ها بار الكتريكی ندارند، هسته های ديگر آن ها را دفع نمی كنند. نوترون ها پس از كند شدن، توسط هسته های ديگر جذب می شوند و باعث شكافت در 3 هسته ی اورانيوم ديگر می شوند و 9 نوترون آزاد می كنند. اگر هر يک از اين نوترون ها نيز موفق به شكافت يک هسته ی اورانيوم شود، 27 نوترون آزاد می شود به همين ترتيب تا آخر؛ اين واكنش را واكنش زنجيری می نامند.
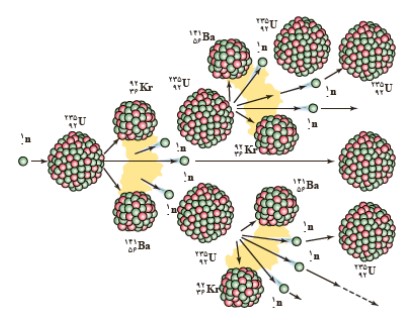
انرژی هسته ای
در واكنش شكافت هسته ای، جرم محصولات شكافت، كم تر از جرم هسته ی مركب است. اين اختلاف جرم بنا به رابطه ی \(E = m{c^2}\) سبب آزاد شدن انرژی گرمايی زيادی می شود. انرژی ای كه توسط محصولات شكافت حمل می شود عمدتاً به شكل انرژی جنبشی است.
علت انجام نشدن واكنش زنجيره ای در معادن
در سنگ معدن اورانيوم، دو ايزوتوپ 235 و 238 وجود دارد، به طوری كه فراوانی ايزوتوپ 235 كه توانايی انجام شكافت را دارد حدود \(0/72\) درصد است (يعنی از هر 140 اتم اورانيوم در سنگ معدن تنها يكی از آن ها ايزوتوپ 235 است) احتمال اينكه اورانيوم 235 نوترونی را گير بيندازد و شكافته شود بسيار كم است و درنتيجه واكنش شكافت را ناممكن می سازد.
غنی سازی اورانيوم
به فرايند افزايش درصد يا غلظت ايزوتوپ 235 در يک نمونه، غنی سازی گفته می شود. (بيش تر راكتورهای تجاری توليد برق تا 3 درصد غنی سازی انجام می دهند(
كندساز نوترون در واكنش شكافت
نوترون هاd آزاد شده در فرايند شكافت اورانيوم 235 (\({}_{92}^{235}U\) )، انرژي 235 جنبشی زيادی دارند. (حدود \(2Mev\) ) و به نوترون های تند معروف اند. اين نوترون ها با احتمال بسيار بيش تری جذب ايزوتوپ اورانيوم 238 (\({}_{92}^{235}U\) ) می شوند. تجربه نشان می دهد اگر بتوان نوترون های تند را به نحوی كند ساخت كه انرژی جنبشی آن ها به حدود \(0/04ev\) برسد، احتمال جذب آن ها توسط ايزوتوپ های اورانيوم 235 افزايش می يابد. اين افزايش احتمال می تواند برای ايجاد واكنش زنجيره ای شكافت كافی باشد. آب معمولی (\({H_2}O\) ) و آب سنگين (\({D_2}O\) ) و گرافيت (اتم های كربن) از جمله موادی هستند كه به عنوان كند ساز نوترون ها در واكنش شكافت هسته ای استفاده می شوند.
راكتور هسته ای
راكتور جايی است كه در آن واكنش زنجيری شكافت به طور كنترل شده رخ می دهد. راكتور ها بيش تر به منظور توليد انرژی الكتريكی در نيروگاه های هسته ای به كار می روند.
ساختمان و نحوه ی كار راكتور هسته ای
راكتور هسته ای افزون بر سوخت هسته ای و ماده ی كند ساز، دارای ميله های كنترل و شاره ای (معمولاً) آب هستند كه گرما را به خارج راكتور انتقال می دهد.
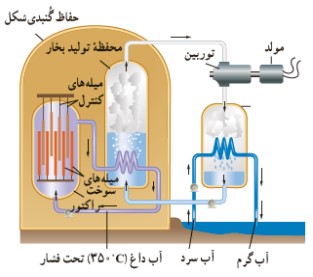
سوخت هسته ای (معمولاً با حدود 3 درصد ايزوتوپ اورانيوم 235) به صورت ميله هايی با قطر حدود \(1cm\) است و هزاران عدد از اين ميله ها در قلب راكتور قرار دارد. با وارد كردن ميله های كنترل به داخل راكتور، آهنگ شكافت، يعنی تعداد نوترون های موجود برای به وجود آوردن شكافت تنظيم می شود. ميله های كنترل معمولاً از مواد جذب كننده ی نوترون مانند كادميم يا بور، ساخته می شوند. در نوعی از رآكتور ها كه به راكتورهای آب تحت فشار (PWR) معروف اند، آبی كه سوخت هسته ای را احاطه كرده است، تحت فشار زياد قرار دارد تا بدون آنكه بجوشد به دماهای بالا برسد. اين آب داغ، به سامانه ی بسته ی ديگری كه محتوی آب كم فشار است، پمپ می شود تا اين آب را گرم كند. گرمای انتقال يافته به سامانه ی دوم، سبب توليد بخار می شود كه توربين و مولد الكتريسيته را به كار می اندازد.
گداخت (همجوشی) هسته ای
يک واكنش هسته ای است كه منشأ توليد انرژی در ستارگان و ازجمله خورشيد است. در اين فرايند دو هسته ی سبک با يكديگر تركيب می شوند و هسته ی سنگين تری به وجود می آورند.
مثالی از واكنش همجوشی هسته ای
واكنش گداخت زير را در نظر بگيريد:
\(D + T \to {}^4He + {}^1n\)
در اين واكنش با همجوشی هسته ای دو ايزوتوپ هيدروژن يعني دوتريم و تريتيم، هسته ی هليم و يک نوترون پر انرژی توليد می شود. در واكنش گداخت، مجموع جرم محصولات فرايند، كم تر از مجموع جرم هسته های اوليه است. در اينجا نيز اين اختلاف جرم با توجه به رابطه ی سبب آزاد شدن مقدار زيادی انرژی می شود.
مشكل ساخت راكتور گداخت
برای انجام واكنش گداخت بايد دو هسته ی كم جرم به حد كافی به هم نزديک شوند تا نيروی كوتاه برد هسته ای بتواند آن ها را كنار هم نگه دارد. ولی هر هسته، بار مثبت دارد و هسته ی ديگر را دفع می كند، برای آنكه هسته ها با وجود اين نيروی رانشی بسيار قوی، بتوانند به هم گداخته شوند، بايد دما بسيار بالا باشد تا هسته ها با انرژی جنبشی زيادی به يكديگر برخورد كنند. به همين دليل، برای انجام اين واكنش بايد مقدار زيادی انرژی صرف كرد. (چنين دمايی در ستارگان و خورشيد وجود دارد)
1کاستی جرم هسته چیست؟
جرم هسته از مجموع جرم پروتون ها و نوترون های تشکیل دهنده اش، اندکی کمتر است. این اختلاف جرم را کاستی جرم هسته گویند.
2چرا واکنش زنجیری به طور طبیعی در معادن اورانیوم رخ نمی دهد؟
چون فراوانی ایزوتوپ 235 حدود \(0/72\) درصد است و احتمال اینکه ایزوتوپ 238 بتواند توسط نوترونی شکافته شود، بسیار کم است.
3شکافت هسته را توضیح دهید.
تقسیم شدن یک هسته سنگین به دو هسته با جرم کمتر
4سه مورد از ویژگی های ایزوتوپ ها را بنویسید.
ایزوتوپ ها هسته هایی هستند که تعداد پروتون های مساوی ولی تعداد نوترون های متفاوت و خواص شیمیایی یکسانی دارند و در یک خانه جدول تناوبی قرار می گیرند.



1736019749.png)















