جواب با هم بیندیشیم صفحه 104 درس 3 شیمی دهم (آب، آهنگ زندگی)
تعداد بازدید : 86.39Mپاسخ با هم بیندیشیم صفحه 104 شیمی دهم
-گام به گام با هم بیندیشیم صفحه 104 درس آب، آهنگ زندگی
-با هم بیندیشیم صفحه 104 درس 3
-شما در حال مشاهده جواب با هم بیندیشیم صفحه 104 شیمی دهم هستید. ما در تیم مای درس، پاسخنامههای کاملاً تشریحی و استاندارد را مطابق با آخرین تغییرات کتاب درسی 1404 برای شما گردآوری کردهایم. اگر به دنبال بهروزترین پاسخها برای این صفحه هستید و میخواهید بدون نیاز به اتصال به اینترنت، علاوه بر پاسخهای گام به گام، به گنجینهای از مطالب درسی دسترسی پیدا کنید، حتماً اپلیکیشن مایدرس را نصب نمایید.
📥 دانلود اپلیکیشن مایدرس
برای دسترسی آفلاین، سریع و بدون نیاز به اینترنت به گنجینهای از گامبهگامها و نمونه سوالات، اپلیکیشن را نصب کنید.
1) شکل زیر مولکول های F2 و HCl با جرم مولی نزدیک به یکدیگر را در یک میدان الکتریکی نشان می دهد.
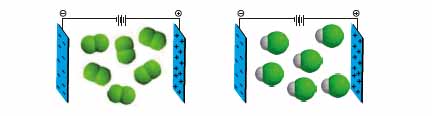
آ) کدام یک دارای مولکول های قطبی است؟ چرا؟
ب) اگر نقطه جوش F2 و HCl به ترتیب برابر با -188 درجه و -85 درجه ساننی گراد باشد، نیروهای بین مولکولی در کدام یک قوی تر است؟ توضیح دهید.
پ) جمله زیر را با خط زدن واژه های نادرست کامل کنید.
در مواد مولکولی با جرم مولی (مشابه / متفاوت) ، ماده با مولکول های (قطبی / ناقطبی)، نقطه جوش بالاتری دارد.
2) جرم مولی گازهای نیتروژن ( N2 ) و کربن مونوکسید (CO) برابر است، بر این اساس:
آ) پیش بینی کنید مولکول های دو اتمی کدام گاز در میدان الکتریکی جهت گیری می کنند؟ چرا؟
ب) کدام یک در شرایط یکسان آسان تر به مایع تبدیل می شود؟ توضیح دهید.
1) آ) HCl زیرا مولکول های آن در میدان الکتریکی جهت گیری کرده اند.
ب) دمای جوش HCl حدود (103 درجه بالاتر از فلور -188) است. این ویژگی نشان می دهد که برای غلبه بر نیرو های بین مولکولی در HCl و تبدیل آن از حالت مایع به بخار , انرژی گرمایی بیشتری نسبت به فلور نیاز است.
ب) در مواد مولکولی با جرم مولی (مشابه) ماده با مولکول های (قطبی) نقطۀ جوش بالاتری دارد.
2) آ) انتظار می رود مولکول 2 اتمی کربن مونو اکسید (بر خلاف نیتروژن) در میدان الکتریکی جهت گیری نماید زیرا مولکول های 2 اتمی که از اتصال اتم های گوناگون تشکیل شده اند , قطبی هستند و در میدان الکتریکی جهت گیری می کنند.
ب) هر چه نیرو های بین مولکولی ماده ای قوی تر باشد آن ماده درشرایط یکسان در دمای بالاتری به جوش می آید. اگر مواد در حالت گاز باشند , هر چه نیرو های بین مولکولی قوی تر باشند مولکول ها بهتر در کنار هم قرار می گیرند؛ زیرا در میان مولکول های قطبی کربن مونو اکسید جاذبه بیشتری نسبت به مولکول های ناقطبی نیتروژن وجود دارد.
مای درس ، برترین اپلیکیشن کمک درسی ایران
پوشش تمام محتواهای درسی پایه چهارم تا دوازدهم- آزمون آنلاین تمامی دروس
- گام به گام تمامی دروس
- ویدئو های آموزشی تمامی دروس
- گنجینه ای از جزوات و نمونه سوالات تمامی دروس
- فلش کارت های آماده دروس
- گنجینه ای جامع از انشاء های آماده
- آموزش جامع آرایه های ادبی، دستور زبان، قواعد زبان انگلیسی و ... ویژه



1736019749.png)















