جواب با هم بیندیشیم صفحه 111 درس 3 شیمی دهم (آب، آهنگ زندگی)
تعداد بازدید : 86.39Mپاسخ با هم بیندیشیم صفحه 111 شیمی دهم
-گام به گام با هم بیندیشیم صفحه 111 درس آب، آهنگ زندگی
-با هم بیندیشیم صفحه 111 درس 3
-شما در حال مشاهده جواب با هم بیندیشیم صفحه 111 شیمی دهم هستید. ما در تیم مای درس، پاسخنامههای کاملاً تشریحی و استاندارد را مطابق با آخرین تغییرات کتاب درسی 1404 برای شما گردآوری کردهایم. اگر به دنبال بهروزترین پاسخها برای این صفحه هستید و میخواهید بدون نیاز به اتصال به اینترنت، علاوه بر پاسخهای گام به گام، به گنجینهای از مطالب درسی دسترسی پیدا کنید، حتماً اپلیکیشن مایدرس را نصب نمایید.
📥 دانلود اپلیکیشن مایدرس
برای دسترسی آفلاین، سریع و بدون نیاز به اینترنت به گنجینهای از گامبهگامها و نمونه سوالات، اپلیکیشن را نصب کنید.
١) با توجه به مقدار گشتاور دو قطبی هر ماده، موارد زیر را توجیه کنید.
آ) انحلال استون در آب
ب) انحلال یُد در هگزان
پ) حل نشدن هگزان در آب
2) آیا جمله «شبیه شبیه را حل می کند» درست است؟ توضیح دهید.
3) آزمایش ها نشان می دهد که فرایند انحلال هنگامی منجر به تشکیل محلول می شود که:
( میانگین جاذبه ها در حلال خالص وحل شونده خالص ) بزرگتر است از ( جاذبه های حل شونده با حالل در محلول )
با این توصیف با توجه به شکل زیر، به پرسش های مطرح شده پاسخ دهید.
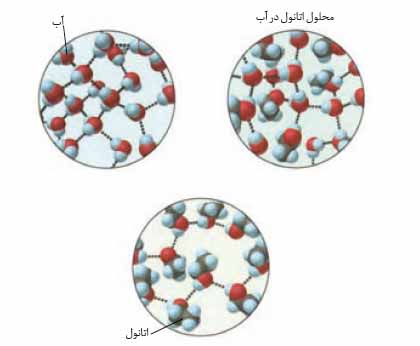
آ) نیروهای بین مولکولی در هریک از چه نوعی است؟ چرا؟
ب) عبارت زیر را با علامت کوچکتر یا بزرگتر کامل کنید.
نیروی جاذبه میان مولکول ها در محلول اتانول در آب ........ میانگین نیروی جاذبه میان مولکول های آب خالص و اتانول خالص
پ) چرا شیمی دان ها انحلال اتانول در آب را انحلال مولکولی می نامند؟ توضیح دهید.
1) آ) آب و استون – هر دو از مولکول های قطبی تشکیل شده اند از این رو استون در آب حل می شود.
ب) ید و هگزان مولکول هایی غیر قطبی هستند، به همین دلیل با یکدیگر حل شده و یک محلول همگن بوجود می آید.
ب) چون هگزان ناقطبی ست نمی تواند بر پیوند های قطبی مولکول های آب غلبه کند از این رو هگزان در آب حل نمی شود و یک مخلوط ناهمگن پدید می آید.
2) بلی – تجربه و آزمایش نشان می دهد که حل شونده های قطبی در حلال های قطبی و حل شونده های ناقطبی در حلال های ناقطبی بهتر حل می شوند.
3) آ) چون هم در مولکول آب و هم در مولکول اتانول پیوند هیدروژنی وجود دارد درمحلول این دو نیز میان ملکول های آب و اتانول پیوند هیدروژنی برقرار می شود.
ب) لازمه انحلال اتانول در آب , شکسته شدن پیوند هیدروژنی میان مولکول های اتانول – اتانول و آب – آب است و چون اتانول در آب حل می شود می توان نتیجه گرفت که در مجموع انرژی حاصل از تشکیل پیوند هیدروژنی جدید میان مولکول های آب و اتانول توانسته است پیوند های هیدروژنی اولیه را بشکند. یعنی میانگین انرژی پیوند آب – اتانول از میانگین انرژی پیوند آب – آب و اتانول – اتانول بیشتر است و چون دمای جوش آب از اتانول بیشتر است می توان گفت انرژی پیوند هیدروژنی در مولکول های آب از انرژی پیوند هیدروژنی در مولکول های اتانول بیشتر است.
پ) با انحلال اتانول در آب , ساختار مولکولی اتانول دچار تغییر نمی شود بلکه مولکول های اتانول میان مولکول های آب پراکنده می شود.
مای درس ، برترین اپلیکیشن کمک درسی ایران
پوشش تمام محتواهای درسی پایه چهارم تا دوازدهم- آزمون آنلاین تمامی دروس
- گام به گام تمامی دروس
- ویدئو های آموزشی تمامی دروس
- گنجینه ای از جزوات و نمونه سوالات تمامی دروس
- فلش کارت های آماده دروس
- گنجینه ای جامع از انشاء های آماده
- آموزش جامع آرایه های ادبی، دستور زبان، قواعد زبان انگلیسی و ... ویژه



1736019749.png)















