درسنامه کامل علوم تجربی هشتم فصل 3 از درون اتم چه خبر
تعداد بازدید : 7.59Mخلاصه نکات علوم تجربی هشتم فصل 3 از درون اتم چه خبر - درسنامه شب امتحان علوم تجربی هشتم فصل 3 از درون اتم چه خبر - جزوه شب امتحان علوم تجربی هشتم نوبت اول فصل 3 از درون اتم چه خبر
ذره های سازنده اتم، الکترون، پروتون و نوترون
ذره های سازنده اتم، الکترون، پروتون و نوترون
ذره های سازنده اتم:
- الكترون (e)
- پروتون (p)
- نوترون (n)
نکته:
جرم الكترون در مقایسه با دو ذره دیگر بسیار ناچیز است.
پروتون و نوترون جرم تقریبا برابری دارند.
سبک ترین ذره:
الكترون
بارهای الکتریکی ذرات:
الکترون دارای بارالکتریکی منفی، پروتون بار مثبت و نوترون بدون بار الکتریکی است.
اتم های مختلف تعداد پروتون های متفاوتی دارند. برای مثال هر اتم کربن 6 پروتون و هر اتم هیدروژن یک پروتون دارد.
از روی تعداد پروتون هر اتم نوع آن اتم را مشخص می کنند.
تعداد ذره های سازنده اتم های سه عنصر هیدروژن، کربن و اورانیوم را با هم مقایسه کنید.
هیدروژن دارای یک الكترون و یک پروتون است ولی نوترون ندارد.
کربن دارای 6 الكترون، 6 پروتون است و 6 نوترون است.
اورانیوم دارای ۹۲ الكترون و ۹۲ پروتون است ۱۴۶ نوترون است.
هر سه عنصر تعداد پروتون و الكترون برابری دارند.
در هر سه عنصر تعداد بار های مثبت و منفی برابر است و اثر یکدیگر را خنثی می کنند مثلا کربن ۶ بار مثبت و ۶ بار منفی دارد که بدون بار می شود.
مای درس ، برترین اپلیکیشن کمک درسی ایران
پوشش تمام محتواهای درسی پایه هشتم- آزمون آنلاین تمامی دروس پایه هشتم
- گام به گام تمامی دروس پایه هشتم
- ویدئو های آموزشی تمامی دروس پایه هشتم
- گنجینه ای از جزوات و نمونه سوالات تمامی دروس پایه هشتم
- فلش کارت های آماده دروس پایه هشتم
- گنجینه ای جامع از انشاء های آماده پایه هشتم
- آموزش جامع آرایه های ادبی، دستور زبان، قواعد زبان انگلیسی و ... ویژه پایه هشتم
نمادهای شیمیایی عناصر و عدد اتمی
نماد های شیمیایی عناصر:
برای نمایش هر عنصر به جای نوشتن نام کامل آن از نمادهای یک یا دو حرفی که بیشتر از نام لاتین عنصرها گرفته شده اند، استفاده می شود. به این نماد ها، نماد شیمیایی می گویند.
نکته:
در نشانه های شیمیایی دو حرفی فقط حرف اول بزرگ نوشته می شود.
- Hydrogen (H)
- (C) Calcium
- (O) Oxygen
عدد اتمی (z):
به تعداد پروتون های هر اتم یا به تعداد بارهای مثبت اتم، عدد اتمی می گویند.
به عنوان مثال اتم سدیم 11 پروتون دارد، پس عدد اتمی سدیم ۱۱ است.

عدد اتمی را گوشه پایین سمت چپ نماد شیمیایی می نویسند.

عناصر بر اساس افزایش عدد اتمی در جدول تناوبی مرتب شده اند، بنابراین عدد اتمی مکان هر عنصر را در جدول تعیین می کند.
نکته:
با تغییر تعداد پروتون ها، نوع اتم نیز تغییر می کند.
در حالت خنثی، تعداد پروتون های یک اتم با تعداد الكترون های آن برابر است.
تعداد الکترون های هر لایه برابر است با 2n2 (n تعداد لایه ها است)
n تعداد لایه ها است که می تواند تعداد الکترون هایی را در خود به گردش بیاورد. در لایه اول فقط دو الكترون قرار می گیرد و در لایه دوم حداکثر ۸ الكترون جای می گیرد.
جزوات جامع پایه هشتم
جزوه جامع علوم تجربی هشتم فصل 1 مخلوط و جداسازی مواد
جزوه جامع علوم تجربی هشتم فصل 2 تغییرهای شیمیایی در خدمت زندگی
جزوه جامع علوم تجربی هشتم فصل 3 از درون اتم چه خبر
جزوه جامع علوم تجربی هشتم فصل 4 تنظیم عصبی
جزوه جامع علوم تجربی هشتم فصل 5 حس و حرکت
جزوه جامع علوم تجربی هشتم فصل 6 تنظیم هورمونی
جزوه جامع علوم تجربی هشتم فصل 7 الفبای زیست فناوری
جزوه جامع علوم تجربی هشتم فصل 8 تولید مثل در جانداران
جزوه جامع علوم تجربی هشتم فصل 9 الکتریسیته
جزوه جامع علوم تجربی هشتم فصل 10 مغناطیس
جزوه جامع علوم تجربی هشتم فصل 11 کانی ها
جزوه جامع علوم تجربی هشتم فصل 12 سنگ ها
جزوه جامع علوم تجربی هشتم فصل 13 هوازدگی
جزوه جامع علوم تجربی هشتم فصل 14 نور و ویژگی های آن
جزوه جامع علوم تجربی هشتم فصل 15 شکست نور
ایزوتوپ ها و عدد جرمی
ایزوتوپ:
به اتم هایی که تعداد پروتون برابری دارند ولی تعداد نوترون آنها برابر نیست، ایزوتوپ می گویند یا به اتم های یک عنصر که تعداد نوترون متفاوت دارند ایزوتوپ های آن عنصر می گویند.
ایزوتوپ های کربن را به صورت کربن-12، کربن-13 و کربن-14 نامگذاری کرده اند. بنابراین عنصر کربن سه ایزوتوپ دارد.
کمترین و بیشترین عدد جرمی ایزوتوپ های کربن:
کمترین عدد جرمی ایزوتوپ: کربن۱۲
بیشترین عدد جرمی ایزوتوپ: کربن ۱۴

ویژگی های ایزوتوپ ها:
- پروتون های یکسانی دارند.
- نوترون های برابری ندارند.
عدد جرمی (A):
به مجموع تعداد پروتون ها و نوترون های یک اتم عدد جرمی گفته می شود.
عدد جرمی در گوشه بالا و سمت چپ نماد شیمیایی نوشته می شود. مثلا اتم کربن در هسته خود و پروتون و ۶ نوترون دارد پس عدد جرمی آن ۱۲ است.


یون ها و انواع آن
اتم خنثی
اتمی است که تعداد الکترون آن با تعداد پروتونش برابر است. به عبارتی مجموع بار الکتریکی آن صفر است.
یون
به اتم هایی که تعداد بارالکتریکی مثبت و منفی آنها یکسان نباشد، یون می گویند. به عبارتی به اتم هایی که تعداد پروتون و الكترون نابرابر دارند.
یون مثبت:
به اتمی که تعداد الکترون های آن از تعداد پروتون های آن کمتر باشد، یون مثبت می گویند.
یون منفی:
به اتمی که تعداد الکترون های آن از تعداد پروتون های آن بیشتر باشد، یون منفی می گویند.
در چه صورتی اتم به يون تبدیل می شود؟
اگر اتمی الکترون به دست آورد یا الکترونی از دست بدهد، دارای بار الکتریکی مثبت یا منفی می شود. به ذرات باردار يون گفته می شود.
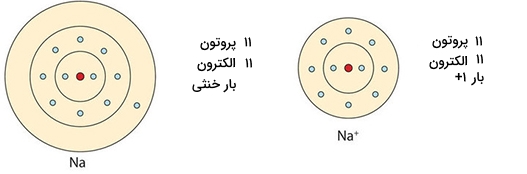
ساختار اتم سدیم و یون سدیم
مثال
از بین نمونه های زیر کدام یک ذره ی مثبت وكدام یک ذره ی منفی است؟ بار را در هر مورد مشخص کنید.
الف) ذره ای که ۱۰ الكترون، ۱۱ پروتون و ۱۰ نوترون دارد.
یون با یک بار مثبت
ب) ذره ای که ۱۰ الكترون، ۱۰ پروتون و ۱۰ نوترون دارد.
اتم خنثی
ت) ذره ای که ۱۰ الكترون، ۹ پروتون و ۱۰ نوترون دارد.
یون با یک بار منفی
مای درس ، برترین اپلیکیشن کمک درسی ایران
پوشش تمام محتواهای درسی پایه هشتم- آزمون آنلاین تمامی دروس پایه هشتم
- گام به گام تمامی دروس پایه هشتم
- ویدئو های آموزشی تمامی دروس پایه هشتم
- گنجینه ای از جزوات و نمونه سوالات تمامی دروس پایه هشتم
- فلش کارت های آماده دروس پایه هشتم
- گنجینه ای جامع از انشاء های آماده پایه هشتم
- آموزش جامع آرایه های ادبی، دستور زبان، قواعد زبان انگلیسی و ... ویژه پایه هشتم



1736019749.png)















